Clear Sky Science · he
בסיס מבני ומולקולרי לוויסות אלוסטרי וקישור קטליטי של האנזים האנושי פוספוריבוזילפורילגליצינאמידין סינתאז
מדוע האנזים הזה חשוב לבריאות
כל תא בגופכם תלוי בפורינים, מולקולות קטנות שמניעות תגובות, מאחסנות אנרגיה ונושאות מידע גנטי. תאי סרטן, המתפצלים במהירות, רעבים במיוחד לפורינים ולעתים משנים את הדרך שבה הם מיוצרים. המחקר הזה מתמקד באנזים האנושי FGAMS, שחקן מרכזי בבניית פורינים מאפס. באמצעות גילוי המבנה התלת‑ממדי של FGAMS ואופן תנועת החלקים שלו ותקשורתם, המחברים חושפים כיצד האנזים נדלק ומכובה וכיצד ניתן לכוונו כדי להאט את גדילת הגידולים.
בלוקי הבנייה של החיים תחת בקרה
תאים מייצרים פורינים דרך קו ייצור תובעני הידוע כנתיב de novo, שמשתמש באנרגיה ובכמה אנזימים לחבר טבעת מורכבת. FGAMS מבצע את השלב הרביעי ברצף הזה ויושב בליבת צביר אנזימים גדול הנקרא פורינוזום, שמסייע לערוץ מרכיבים ביעילות. מכיוון שתאי סרטן גדלים במהירות ומגבירים לעתים קרובות את הנתיב הזה, אנזימים כמו FGAMS מהווים מטרות תרופתיות אטרקטיביות: חסימתם עלולה לרעב גידולים בנוקלאוטידים שהם צריכים בעוד תאים בריאים מסתמכים על מסלולי מיחזור.
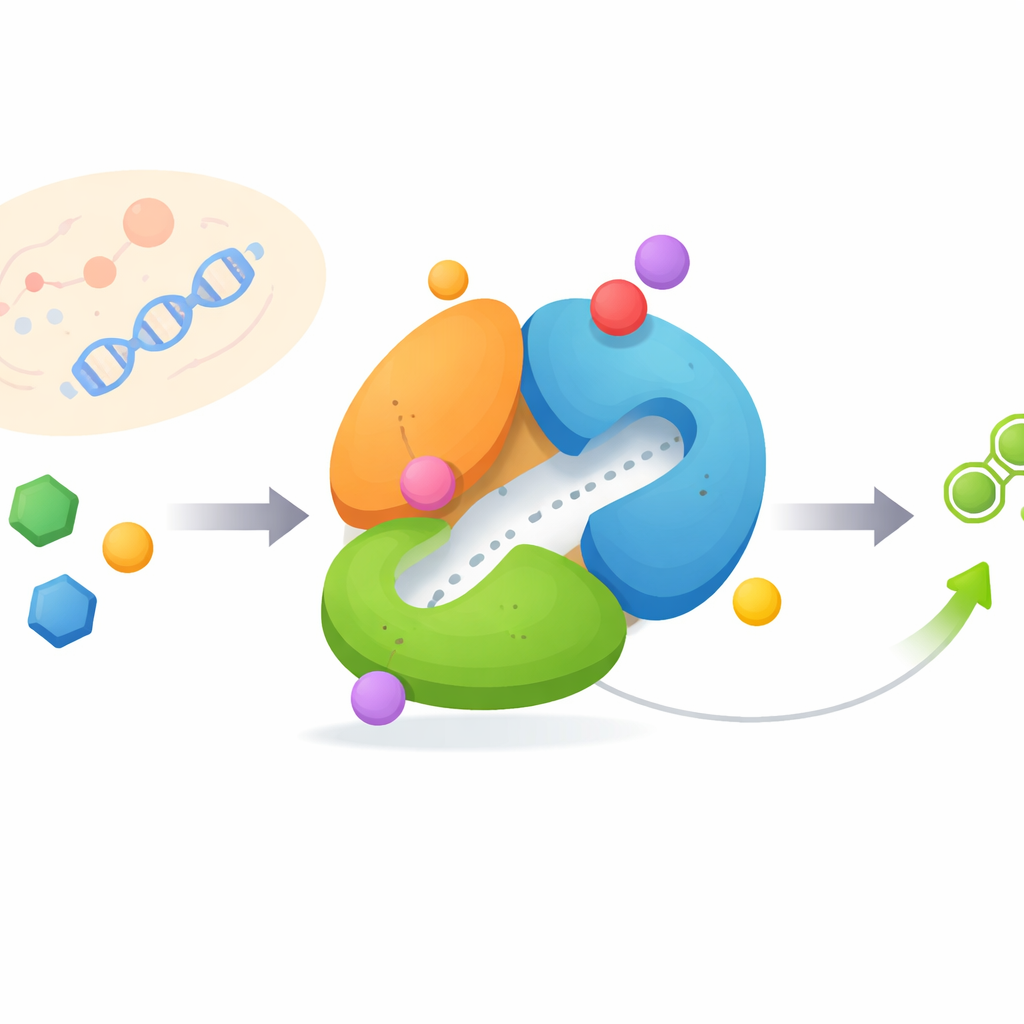
מכונה מולקולרית שמשנה צורה
FGAMS מורכב משלוש חלקות מקושרות, או דומיינים, שלכל אחת תפקיד שונה והן חייבות לשתף פעולה בסדר מדויק. דומיין אחד חותך אמוניה מחומצת האמינו גלוטמין, דומיין נוסף משתמש באמוניה הזו כדי לשנות מולקולה סוכרית קטנה, ודומיין שלישי פועל כמרכז בקרה. בעזרת מיקרוסקופ אלקטרונים בקור ברזולוציה גבוהה תפסו החוקרים את FGAMS בשלוש מצבי עבודה מובחנים: קשור למולקולת נושא־אנרגיה, עם ביניים תגובתי קצר־חיים שנסגר, ועם מספר מצרכים וביניים בו‑זמנית. השוואת המצבים הללו הראתה שמעגלים גמישים ו"זרוע" N‑טרמינלית זזים באופן דרמטי, ומשנים את קונפיגורציית האנזים ככל שהכימיה מתקדמת.
מנהרה נעלמת ושערים מולקולריים
חידה מרכזית הייתה כיצד האמוניה שמשתחררת באחד הדומיינים עוברת בבטחה לאתר המרוחק שבו היא משומשת, מבלי לדלוף ולגרום נזק. המבנים החדשים חושפים מנהרה פנימית שלא נראתה קודם שמחברת בין שני האתרים, יחד עם סדרת "שערים" שנוצרו על ידי חומצות אמינו ספציפיות. כשהמצרכים הנכונים נקשרים והביניים נוצר, לולאה מרכזית מתייצבת במיקום מסודר, מושכת את הדומיין N‑טרמינלי ומעווה לולאות סמוכות בדומיין הקטליטי. כוריאוגרפיה זו פותחת שני שערי כניסה כך שגלוטמין יכול לעבור עיבוד ומעצבנת באופן זמני אזור שמייצב את הביניים בעלי האנרגיה הגבוהה הנדרש לשבירת הקשר.
קישור הכימיה דרך תנועה
כשהתגובה מתקדמת, האנזים לא פשוט ממתין; הוא משתמש בכל שלב כימי כאות. כאשר נוצר ביניים תיאוסטרי קוולנטי בדומיין המפיק אמוניה, התנועות הקודמות מתהפכות חלקית. זה מרפה את הלולאה המרכזית וממקם מחדש את השערים כדי לחסום נתיבי בריחה, בעוד שני שערים נוספים בקצות המנהרה נפתחים. הזזות עדינות בכמה שאריות "צווארי בקבוק" מרחיבות את המעבר הפנימי, ומאפשרות למולקולת אמוניה לנוע דרך המנהרה ישירות אל האתר הפעיל השני, שם היא מגיבה עם הביניים הכלוא ליצירת התוצר הסופי. מוטציות בשאריות השער גורמות לדליפת אמוניה או לניתוק שני חצאי התגובה, ואישרו שמערכת השערים והמנהרה חיונית לקטליזה יעילה.
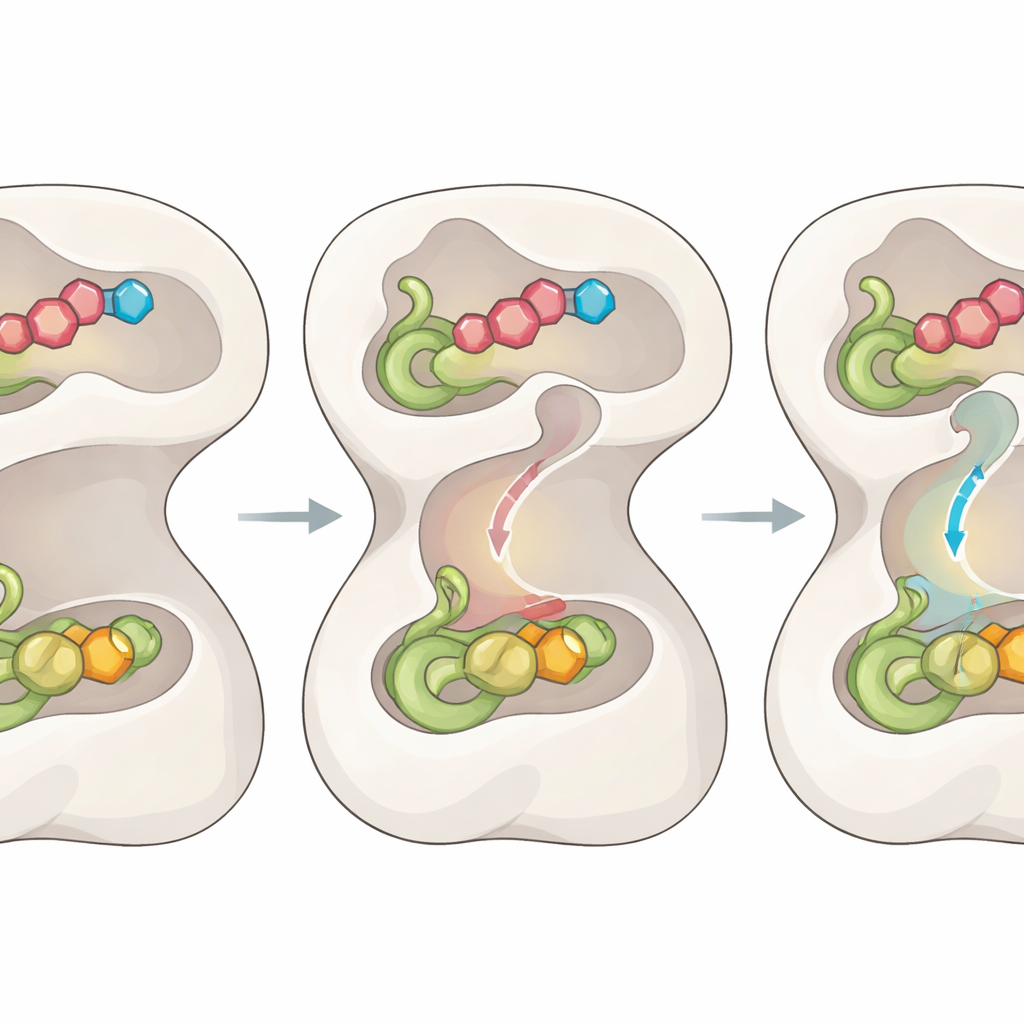
מתובנה מבנית לדרכי טיפול
על ידי מעקב אחר FGAMS במחזור הקטליטי שלו, המחקר מצייר תמונה מפורטת של האופן שבו תנועות דומיינים, לולאות גמישות, שערים פנימיים ומנהרה חולפת כולם מחוברים יחד לתיאום הכימיה. עבור קהל שאינו מומחה, הקו התחתון הוא שהאנזים פועל כמו מפעל זעיר שניתן לתכנות: הוא פותח את דלתותיו והמסלול הפנימי רק כשהרכיבים הנכונים נמצאים במקום, ומבטיח מהירות ובטיחות. מכיוון ש‑FGAMS תומך בייצור פורינים בתאי סרטן ומשויך לתוצא גרוע בגידולי כבד, השרטוטים המבניים ונקודות הבקרה שזוהו זה עתה מציעים מספר דרכי פעולה לעיצוב תרופות שיסתמו את המנהרה, יקפיאו את השערים או יתפסו ביניים מרכזיים, ובכך עשויים להוליד מחלקה חדשה של טיפולים נגד סרטן מוכוונים.
ציטוט: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
מילות מפתח: ביו-סינתזת פורינים, ויסות אלוסטרי, ניסוע אמוניה, מטבוליזם של סרטן, מבנה קריו-EM