Clear Sky Science · he
פגמים מבניים בסיבים של אמילואיד-β מניעים גרעון משני
מדוע פגמים זעירים בחלבוני המוח חשובים
באלצהיימר ומחלות מוח קשורות, חלבונים מסוימים מצטברים וצוברים יחד לצורות ארוכות ודמויות חוט הנקראות סיבי אמילואיד. סיבים אלה אינם רק סימן למחלה; הם גם מסייעים ליצירת חלקיקים חלבוניים חדשים ועתירי רעילות שיכולים לפגוע בתאי מוח. המחקר שואל שאלה פשוטה אך עוצמתית: האם "פגמים" מבניים נדירים בתוך סיבי האמילואיד משמשים כאתרי הצתה עיקריים שמגלים צמיחה מזיקה חדשה? התשובה עשויה להצביע על דרכים חדשות להאט או לעצור את הפרעות אלה על ידי מיקוד בכמה אתרים קריטיים במקום על כל פני השטח של החלבון. 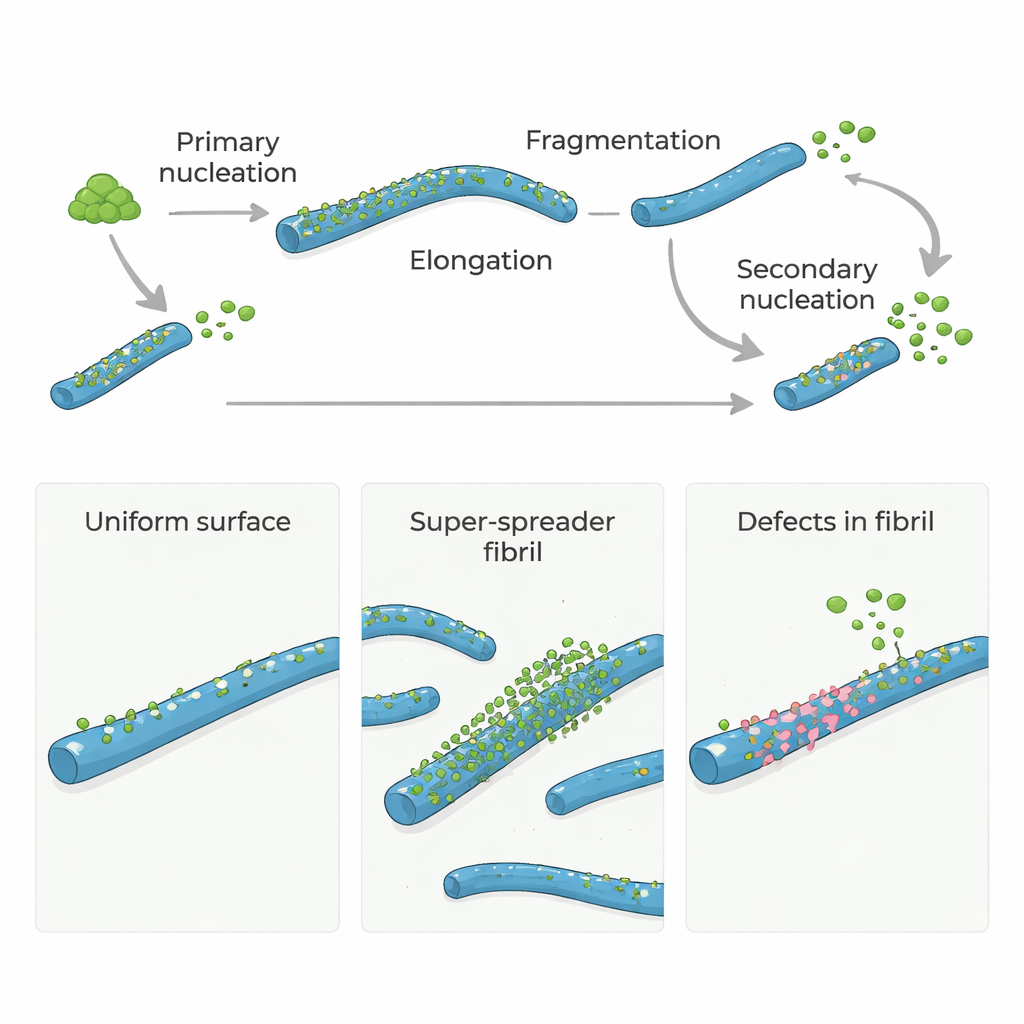
מפני חלבון שקט לתגובת שרשרת מסחררת
חלבוני אמילואיד-β (Aβ), שמרכזיים במחלת אלצהיימר, בדרך כלל לא מצטברים במהירות מעצמם. כדי להתחיל, כמה חד־סוכנים (מונומרים) צריכים להיאסף לאט אל תוך הסיבים הזעירים הראשוניים, שלב שנקרא גרעון ראשוני. ברגע שסיבים ראשוניים אלה קיימים, הם מתארכים במהירות כאשר עוד מונומרים מצטרפים לקצותיהם. חשוב עוד יותר, סיבים קיימים יכולים לעורר הופעה של סיבים חדשים על גבי משטחיהם בתהליך הידוע כגרעון משני. שלב מונחה-משטח זה יכול להציף את המערכת בסיבים חדשים ואוליגומרים רעילים קטנים, ולהפוך זרם איטי לתגובת שרשרת חסרת שליטה.
האם כל פני הסיב מסוכנים באותה מידה?
הרבה מודלים הניחו שכל פני השטח של סיב אמילואיד טובים באותה המידה בקטליזת גרעון משני. עם זאת, ניסויים אחרונים רמזו שרק חלק קטן מהמשטח הוא באמת פעיל. כדי לחקור זאת, החוקרים השתמשו במולקולת "שיירון" טבעית בשם Brichos, הידועה ביכולתה לחסום גרעון משני של Aβ40 ו-Aβ42 (שני צורות מפתח של אמילואיד-β). באמצעות מדידות מדודות של כמה Brichos תויג פלואורסצנטית נותרת מחוברת לסיבים, הם מצאו שהיא נקשרת חזק אך במספרים נמוכים מאוד: בערך מולקולת Brichos אחת על כל 100–150 מולקולות Aβ בסיב. עם זאת, כיסוי דל זה הספיק לדכא יותר מ-90% מהגרעון המשני, כלומר רק אתרי מיקום נדירים ומקומיים — ולא כל פני השטח — שולטים בייצור של צברים רעילים חדשים.
בירור תפקידם של פגמים נסתרים
ממצאים אלה הציעו שאתרי הגרעון הקריטיים עשויים להיות פגמים מבניים — אי־סדירויות קטנות הנוצרות כשהסיבים גדלים, כגון שכבות מיושרות בצורה שגויה או ליבות פנימיות שחלקית חשופות. כדי לבחון רעיון זה ישירות, החוקרים גידלו סיבי Aβ40 בשתי תנאים שונים. קבוצה אחת, סיבי ה"בקרה", נוצרה בתנאים רגילים של רוויה חזקה המעדיפים גדילה מהירה והיתפסות קינטית של פגמים. הקבוצה השנייה נוצרה באמצעות פרוטוקול אשור איטי ומבוקר בטמפרטורה: הסיבים גדלו בכוח דוח פנימי נמוך מאוד, קרוב למגבלת המסיסות שלהם, שם מבנים שגויים יכולים להמוס או להיתקן לפני שיתמקמו. מיקרוסקופיה אלקטרונית בהקפאה ברזולוציה גבוהה הראתה ששתי קבוצות הסיבים דמו במראה הכללי ובפיתול, מה שמעיד שהתהליך האשירי לא שינה את המורפולוגיה הבסיסית. 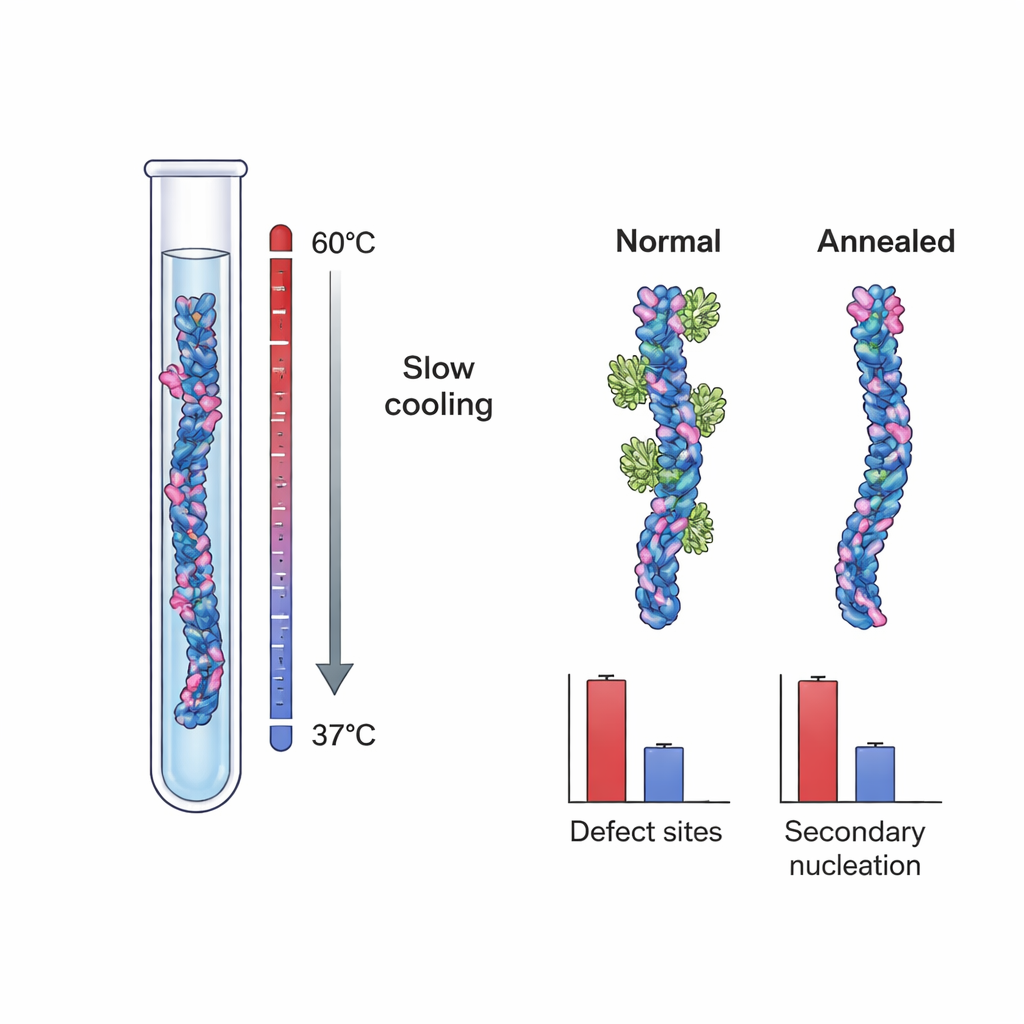
פחות פגמים, פחות אתרים מסוכנים לצמיחה
כאשר הצוות מדד את קשירת Brichos לשני סוגי הסיבים האלה, הם גילו הבדל בולט. לסיבי Aβ40 של הבקרה היו כ־אתר קשירה אחד של Brichos על כל ~100 מונומרים, שוב מצביע על אתרים נדירים אך חשובים. לעומת זאת, לסיבים שאושרו הייתה רק כאתר אחד על כל ~800 מונומרים — ירידה של כמעט 90% בתדירות האתרים. בניסויים נפרדים שבהם הוסיפו את הסיבים הללו כ"זרעים" לתמיסות Aβ40 טריות, לסיבים שאושרו הייתה היכולת הרבה פחותה לגרום לצבירה חדשה, אפילו כאשר המסה הכוללת שלהם התאמה לזו של סיבי הבקרה. מיצוי קינטי מפורט הראה שירידה בכוח ה"זריעה" הזו לא יכולה להיות מוסברת פשוט על ידי הבדלים באורך הסיבים. במקום זאת, היא התאמה כמותית עם המספר המופחת של אתרי קשירת Brichos, דבר שתומך בעוצמה ברעיון שפגמי גדילה פועלים כמנועים המרכזיים של גרעון משני.
עיקרון כללי עם פוטנציאל טיפולי
על ידי שילוב טיעונים תרמודינמיים, ניתוח מחדש של עבודות קודמות והשוואות בין מספר חלבונים היוצרים אמילואיד, המחברים טוענים שפגמי גדילה נדירים סביר שיהיו מרכזיים לגרעון משני במערכות רבות, ולא רק ב-Aβ הקשורה לאלצהיימר. פגמים אלו חושפים בחלקם את ליבת הסיב הדחוסה מאוד, ומספקים תבנית מוכנה שבה אוליגומרים וסיבים חדשים יכולים להיווצר הרבה יותר בקלות מאשר על פני שטח חלק. ההכרה בפגמים אלה כבעייתיים המרכזיים פותחת נתיבים חדשים לעיצוב תרופות. במקום לנסות לחסום כל אינטראקציה אפשרית על פני סיב, טיפולים יכולים לשאוף להגן או לתקן רק את אתרי הפגם הנדירים הללו, או להקטין את התנאים שגורמים להם להיווצר מלכתחילה. במונחים מעשיים, זה עשוי לכלול הורדת הריכוז היעיל של חלבונים היוצרים אמילואיד במוח או תכנון מולקולות, בהשראת Brichos, שמזהות ומנטרלות מוקדי גרעון מונעי פגם. אם יצליחו, אסטרטגיות כאלה יכולות לחתוך את המקור הראשי של האוליגומרים הרעילים ולהאט את התקדמות המחלות הקשורות לאמילואיד.
ציטוט: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
מילות מפתח: סיבי אמילואיד, מחלת אלצהיימר, גרעון משני, צבר חלבונים, שיירון Brichos