Clear Sky Science · he
תחרויות בין סדרי קשרי מימן מניעות את המתיחות המעצבת של פני המים
למה פני המים מוזרים יותר ממה שנראה
פני המים מאפשרים לחרקים ללכת על שלוליות, מעצבים טיפות גשם ושולטים באופן היווצרותן והתפרקותן של בועות. ועדיין, כשמדענים מודדים עד כמה "הדוקים" אותם פני שטח — כלומר את מתיחות הפנים — הם מגלים שמים מתנהגים בצורה מפתיעה ומוזרה ככל שהם מתקררים, במיוחד כשהם מוקפאים מתחת לנקודת ההקפאה הרגילה. מאמר זה משתמש בסימולציות מחשב מתקדמות כדי לחשוף כיצד הארגון החבוי של מולקולות המים על המשטח מסביר את התעלומה הוותיקה הזו.
שני סוגים חבויים של מים נוזליים
למרות שאנו חווים את המים כנוזל פשוט ואחיד, המולקולות שלהם יכולות לסדר את עצמן מקומית בשתי דרכים מנוגדות. סידור אחד צפוף ומפורר יותר; המחברים קוראים לו מצב ρ. הסידור השני פתוח וסימטרי יותר, כאשר כל מולקולה מוקפת בתבנית טטרהתראלית של כארבע שכנים; זהו מצב S. עבודות קודמות הציעו כי האיזון בין שני התבניות המקומיות האלה מסייע להסביר רבות מתכונות המאסה המוזרות של המים. כאן שואלים המחברים כיצד תמונת שני המצבים הזו מתנהגת בממשק אוויר–מים, שם נולדת מתיחות הפנים.
איך המשטח מושך מולקולות לסדר מסוים
בגבול שבין אוויר למים, המולקולות כבר אינן חשות משיכות שוות בכל הכיוונים. שבר הסימטריה הזה מועדף על מולקולות במצב ρ, שהאטומי המימן והדיפולים המולקולריים שלהן יכולים להיטות בקלות לכיוון מועדף. סימולציות מראות כי בטמפרטורת החדר ובטמפרטורות נמוכות מעט מתחתיה, השכבה העליונה ביותר של המים מתמלאת במולקולות ρ ממוינות אלה, בעוד שמולקולות מצב S נפוצות יותר מעט מתחת לפני המצע ובמאסה. מכיוון שמולקולות מצב ρ מתיישרות בחוזקה, הן יוצרות חוסר איזון בכוחות — אניזוטרופיה של מאמצים — שמניב מתיחות פנים יחסית גדולה בהשוואה לנוזלים רגילים כמו בנזן.
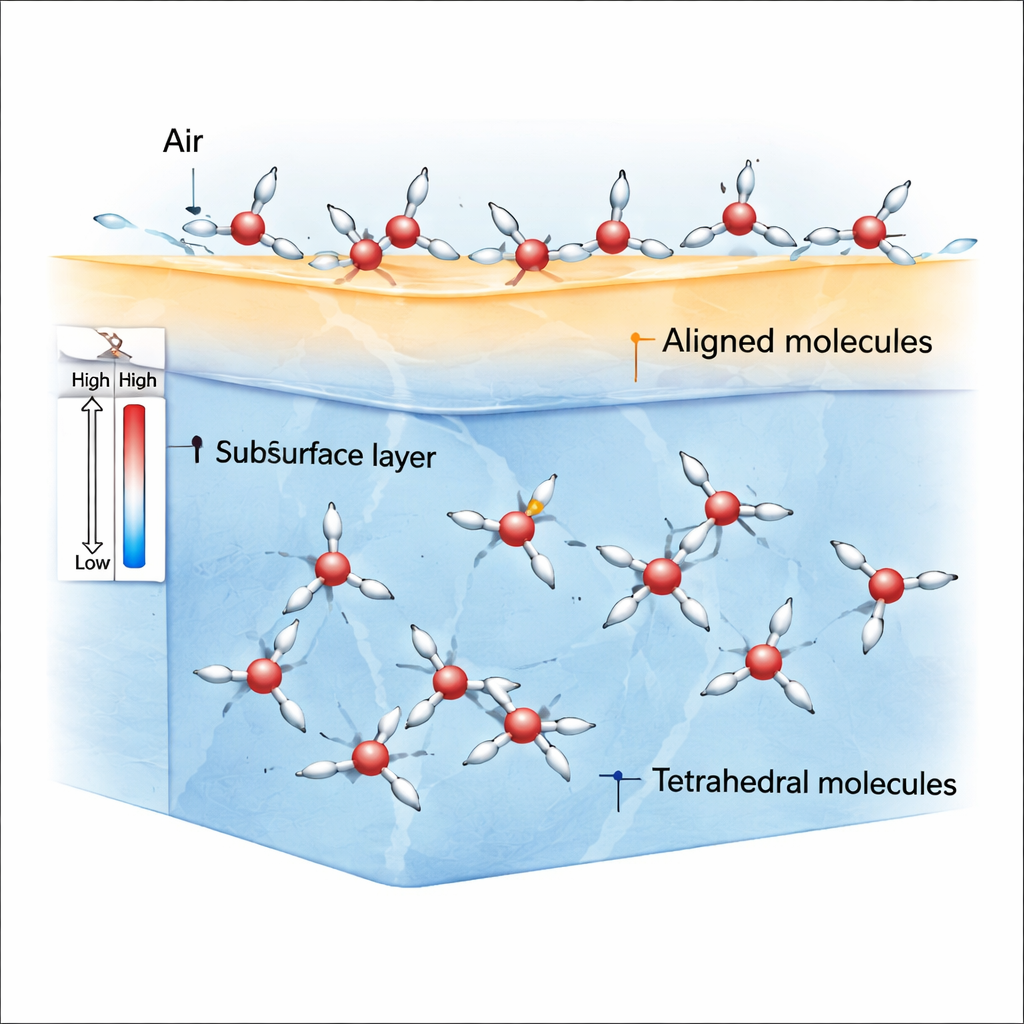
למה הקירור ראשית מאט ולאחר מכן מאיץ את הידוק הפנים
ברוב הנוזלים הפשוטים, הקירור מהדק בהדרגה את המשטח, כך שמתיחות הפנים עולה כמעט בקו ישר. מים עושים זאת רק בטמפרטורות גבוהות יותר. כשהם מתקררים לעבר כ־־0.15– מעלות צלזיוס (275 K), העלייה במתיחות הפנים מתחילה להאט. הסימולציות מראות שהאטה זו מתרחשת כי מולקולות מצב ρ על המשטח כבר הגיעו למידת יישור מקסימלית; קירור נוסף כמעט ואינו משנה את תרומתן. באותו הזמן, מולקולות מצב S שבתת-המשטח נשארות ברובן מכוונות באקראי, ולכן הן עושות מעט כדי להגביר את מאמץ המשטח. התוצאה הכוללת היא סוג של רמה: הטמפרטורה ממשיכה לרדת, אך מתיחות הפנים גדלה באיטיות בלבד.
קירור עמוק מפעיל הידוק שני
כשמיזמים את המים עוד יותר, הרבה מתחת לנקודת ההקפאה הרגילה שלהם לתחום הקפוא-יתר העמוק (בקירוב סביב 250 K ומטה), התנהגותם משתנה שוב. שיעור מבני ה־S הטטרהתראליים עולה בחדות, אפילו בסמוך למשטח. ובעיקר, מולקולות ה־S האלה כבר לא מצביעות בכיוונים אקראיים. הדיפולים שלהן מתחילים להתיישר לאורך הכיוון הניצב למשטח, מונעים על־ידי אינטראקציות בין דיפולים שכנים ועל־ידי אזור של לחץ שלילי ממש מתחת לפני השטח. ברגע שזה קורה, המים במצב S, שהיו מקלים בעבר על מתיחות הפנים, מתחילים כעת לחזק אותה. התרומה הממוינת הנוספת הזו יוצרת עלייה מחודשת ומהירה יותר — העלייה "הנכנסת מחדש" — במתיחות הפנים בטמפרטורות נמוכות.
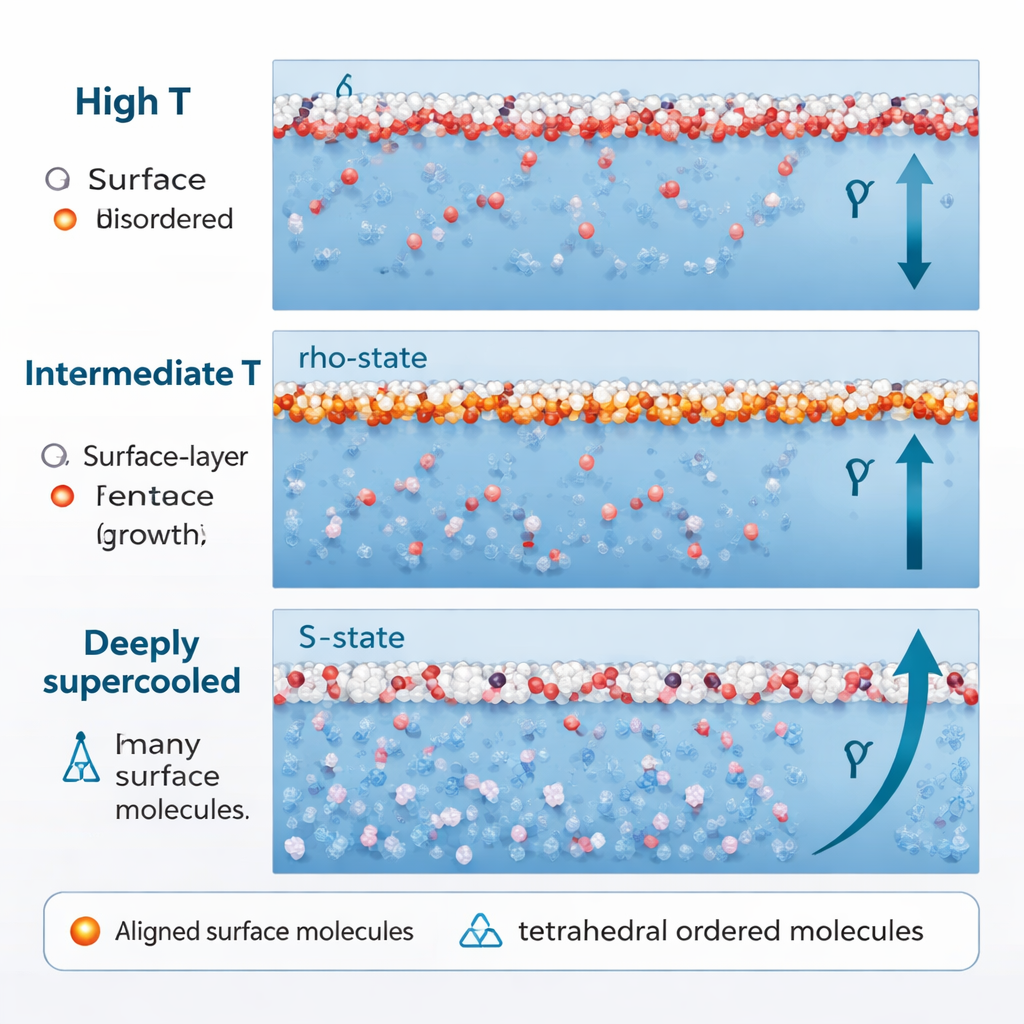
מסתורין פני השטח לקרח ומעבר לכך
אותם אשכולות טטרהתראליים במצב S שמקשיחים את המשטח בטמפרטורות נמוכות גם מזכירים בלוקים ראשוניים של צורות מסוימות של קרח, והסימולציות מגלות שהם מועשרים בסמוך לממשק. משמעות הדבר היא שהגבול אוויר–מים יכול לשמש כעריסת היווצרות הקרח, ועוזר להסביר מדוע ההקפאה מתחילה לעתים קרובות על פני השטח. באופן רחב יותר, העבודה מספקת קישור מוחשי ברמת המולקולה בין האופן שבו מולקולות המים מארגנות ומצינות את עצמן לבין כמה חזק המשטח מושך פנימה. התמונה המבנית־מכניקתית הזו לא רק פותרת את עקומת הטמפרטורה המוזרה של מתיחות פני המים, אלא גם מציעה מפת דרכים להבנה ושליטה בתופעות בין-ממשקיות בנוזלים יוצרי-רשת אחרים, ממים קפואים-יתר בעננים ועד חומרים המשמשים בטכנולוגיה ובביולוגיה.
ציטוט: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
מילות מפתח: מתיחות פני המים, קשרי מימן, מים קפואים-יתר, מבנה נוזלי, התגרענות קרח