Clear Sky Science · he
STING פועל יחד עם TOX בעיכוב ביטוי HO-1 כדי לגרום לפרורפטוזיס בתאי CD8+ החודרים לגידול ולעמידות לחיסון נגד סרטן
מדוע המחקר הזה חשוב לטיפול בסרטן
אימונותרפיות מודרניות נגד סרטן פועלות על ידי שחרור תאי הטוֹסקים (T) של הגוף, אבל גידולים רבים עדיין מצליחים להשבית את התאים האלה. מחקר זה חושף מתג השמדה פנימי נסתר בתוך תאי CD8+ "רצחניים" שבו גידולים מנצלים, ומראה כיצד כיבוי אותו מתג יכול להפוך את האימונותרפיה ליעילה בהרבה.
נתיב מוות נסתר בתוך תאי T שמלחמים בגידול
בתוך הגידול אמורים תאי CD8+ לצוד ולהשמיד תאי סרטן. במקום זאת, הם לעיתים נעשים נדירים, איטיים וקצרים־יומיים. החוקרים התמקדו בשתי מולקולות בתוך תאי T — STING, חיישן של נזקי DNA, ו‑TOX, חלבון המקושר לעייפות תאי T. הם מהנדסים עכברים שבתאי CD8+ שלהם חסרו STING, TOX, או שניהם, ולאחר מכן שתלו מספר סוגי גידולים. באופן מפתיע, בעכברים שתאי ה‑T שלהם חסרו את אחד מהם — STING או TOX — הגידולים נקו הרבה יותר טוב. הגידולים שלהם גדלו לאט יותר, הכילו הרבה יותר תאי CD8+, ותאי ה‑T הללו ייצרו כמויות גדולות יותר של מולקולות שמחסלות סרטן כמו אינטרפרון‑גמא וגרנזים B. ממצאים אלה מצביעים על תוכנית פנימית שמהולה בהידודי תפקוד של תאי ה‑T בתוך הגידול.
כיצד מוות תאיית מונע־ברזל מחליש את החיסון
בבדיקת פעילות גנים בתאי T החודרים לגידול, החוקרים מצאו שתאי T רגילים בתוך הגידול מוכנים לצורת מוות ספציפית הנקראת פרורפטוזיס. שלא כמו אפופטוזיס, פרורפטוזיס מונעת מעודף ברזל והצטברות שומנים פגומים בממברנות התא. בתאי CD8+ חשופים לתאי גידול, גנים המקדמים הצטברות ברזל ונזק לשומנים הופעלו, בעוד גנים מגן כובו. לעומת זאת, בתאי T חסרי STING או TOX נצפה הדגם ההפוך: הם הביעו יותר מהאנזימים המגנים HO-1 ו‑GPX4, היה להם רמות ברזל נמוכות יותר, פחות חמצון שומנים, מיטוכונדריה בריאה יותר, והם התנגדו למוות בפרורפטוזיס. ניסויים במעבדה אישרו שחסימת פרורפטוזיס בכימיה שומרת על תאי T רגילים בחיים, בעוד שהסרת STING או TOX העשירה אותם בהתנגדות טבעית.
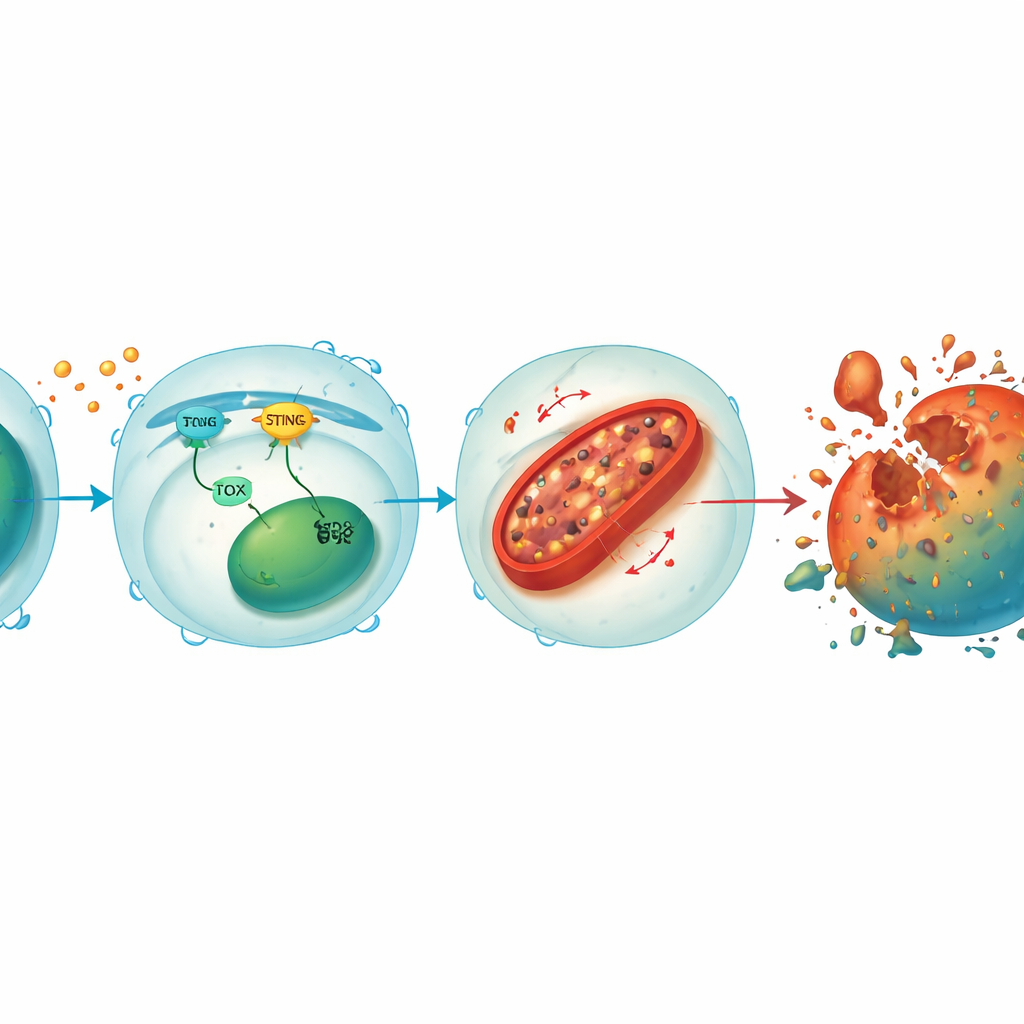
מעגל שמקשר אותות לחץ לנזק מיטוכונדריאלי
בהעמקה נוספת מצאו החוקרים ש‑STING ו‑TOX יוצרים לולאה מחזקת בתוך תאי CD8+. כאשר אותות גידול או וירוס מפעילים את STING, נגרמת הפעלת גורמים שמגבירים את TOX, ו‑TOX בתורו מסייע לשמר את פעילות STING. יחד הם מדכאים את HO-1, אנזים שעוזר בדרך כלל לשלוט על הברזל בתא. כאשר HO-1 מושתקת, הברזל מצטבר במיטוכונדריה — תחנות הכוח של התא — מה שמוביל לרמות גבוהות של מולקולות חמצון וחמצון של שומני ממברנה. נזק מיטוכונדריאלי זה מרוקן את ייצור האנרגיה ולבסוף דוחף את תא ה‑T לפרורפטוזיס. השבתת STING או TOX בתאי knockout החזירה את הצטברות הברזל ומוות התאים, בעוד הורדה נוספת של HO-1 נעשתה אפילו על תאים מוגנים חשופים שוב לפגיעות, מה שמבליט את HO-1 כבלם מרכזי על המסלול ההרסני הזה.
כיצד לחומצת החלב המיוצרת על‑ידי הגידול מפעילה את המתג
המיקרו‑סביבה של הגידול עשירה בחומצת חלב, תוצר לוואי של המטבוליזם המשתנה של הסרטן. המחקר מראה שחומצת החלב הזו אינה פסולת מטבולית בלבד — היא מסייעת באופן פעיל להפעלת מתג הפרורפטוזיס בתאי T. בהשוואה לתאים אחרים, תאי CD8+ רגישים במיוחד לחומצת החלב. כשהחומצה נכנסה לתאים דרך נשאים ייעודיים, היא גרמה להצטברות ברזל, כיווץ מיטוכונדריה, אובדן DNA מיטוכונדריאלי, ועוד נזק חמצוני. במקביל, חומצת החלב הגבירה את פעילות STING ו‑TOX ודיכאה עוד יותר את HO-1. תאי T חסרי STING או TOX היו עמידים הרבה יותר לפגיעה הנגרמת על‑ידי חומצת החלב. חסימת נשא חומצת חלב מרכזי באמצעות תרופה (AZD3965) הגנה על תאי CD8+ מפרורפטוזיס בעכברים, הגדילה את נוכחותם בתוך הגידולים, והאטה את גדילת הגידול — חיקוי של היתרון שהושג בהסרת STING גנטית בתאי T.
הפיכת פגיעות ליתרון טיפולי
תובנות מכאניסטיות אלה נושאות משמעות מעשית. כאשר החוקרים השתמשו בטיפול אימוני תאית מאומצת — הזרקת תאים פעילים ממעבדה לעכברים — הם מצאו שתאי T מהונדסים חסרי STING או TOX שלטו בגידול בעוצמה רבה יותר מתאי T רגילים. יתר על כן, שילוב של תאי ה"עמידים לפרורפטוזיס" האלה עם טיפולים קיימים כגון חוסמי נקודות צ'ק‑פוינט PD‑1 או TIM‑3, כימותרפיית cisplatin, או תרופה המפעילה STING, הניב הצטמצמות גידול משופרת באופן מובהק לעומת כל טיפול בודד. לבסוף, בדגימות גידול של מטופלות עם סרטן צוואר הרחם, רמות גבוהות של TOX ורמות נמוכות של HO-1 בתאי לימפוציטים חודרים לגידול נקשרו להישרדות נמוכה יותר, מה שמרמז שמסלול זה מעצב גם תוצאות קליניות בבני אדם.
מה המשמעות לטיפול בסרטן בעתיד
במילים פשוטות, המחקר מגלה שגידולים יכולים לכפות על תאי ה‑T הטובים ביותר שלנו להחליד מבפנים על‑ידי הובלתם לצורת מוות תאיתי מונעת‑ברזל. מעגל חומצת חלב–STING–TOX מוריד את ההגנה של HO-1, מזיק למיטוכונדריה ומוביל לפרורפטוזיס, מה שמדלל את שורות תאי CD8+ היעילים. פיצוץ הלולאה הזו — על‑ידי הנדסת תאים חסרי STING או TOX, הגברת HO-1, או חסימת כניסת חומצת החלב — שומר על תאי T בחיים, ערניים ומוכנים לתקוף. עבודה זו מצביעה על כיווני אימונותרפיה מדור הבא שמשלבים כוונון מטבולי וגנטי של תאי T עם תרופות קיימות כדי להתגבר על עמידות ולהשיג שליטה בסרטן שהיא יציבה יותר.
ציטוט: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
מילות מפתח: אימונותרפיה של סרטן, תאי CD8, פרורפטוזיס, מיקרו‑סביבה של הגידול, מסלול STING־TOX־HO-1