Clear Sky Science · he
ניתוח הנוף הטרנסקריפטומי והמטבולומי של סרטן הערמונית ממקורות אנטומיים שונים באמצעות snFLARE-seq ו-mxFRIZNGRND
מדוע המחקר הזה חשוב למטופלים ולמשפחות
סרטן הערמונית הוא הסרטן השכיח ביותר בגברים, אך לא כל הגידולים בערמונית מתנהגים באותו אופן. המיקום בו מתחיל הגידול בתוך הערמונית וכיצד הוא מגיב לטיפול הורמונלי יכולים להשפיע במידה רבה על הסיכוי לחזרה או להתמרה לאגרסיבי. במחקר זה נעשה שימוש בשתי טכניקות מעבדה חדשות על רקמות בית חולים המאוחסנות שגרתי, כדי להראות כיצד גידולים מאזורים שונים של הערמונית נבדלים בסוגי התאים שלהם, בסביבת המערכת החיסונית ובמטבוליזם. תובנות אלו עשויות לסייע לרופאים לחזות טוב יותר מי זקוק לטיפול אינטנסיבי ולחשוף דרכים חדשות למנוע מהסרטן להתפתח לצורות שקשה לטפל בהן.
שכונות שונות בתוך אותה בלוטה
לאזורי הערמונית יש אזורים מובחנים, בעיקר איזור היקפי (peripheral zone) והאיזור המעברי (transition zone). כ-70% ממקרי סרטן הערמונית מתפתחים באזור ההיקפי, בעוד שכ־רבע מתחילים באזור המעברי. במעקב אחרי למעלה מ-400 גברים שעברו ניתוח, החוקרים מצאו כי גידולים המוגבלים לאזור המעברי נטו להישנות מאוחרת ופחות תדירה מאלו שבאזור ההיקפי. גידולים שמשתרעים על פני שני האזורים היו המדאיגים ביותר — חזרו במהירות רבה יותר והפגינו עמידות חזקה יותר לטיפולים להורדת הורמונים. דפוסים קליניים אלה, שאושרו גם במטופלים במזרח אסיה, רומזים ש'השכונה' המקורית של הגידול מעצבת את התנהגותו בעתיד.
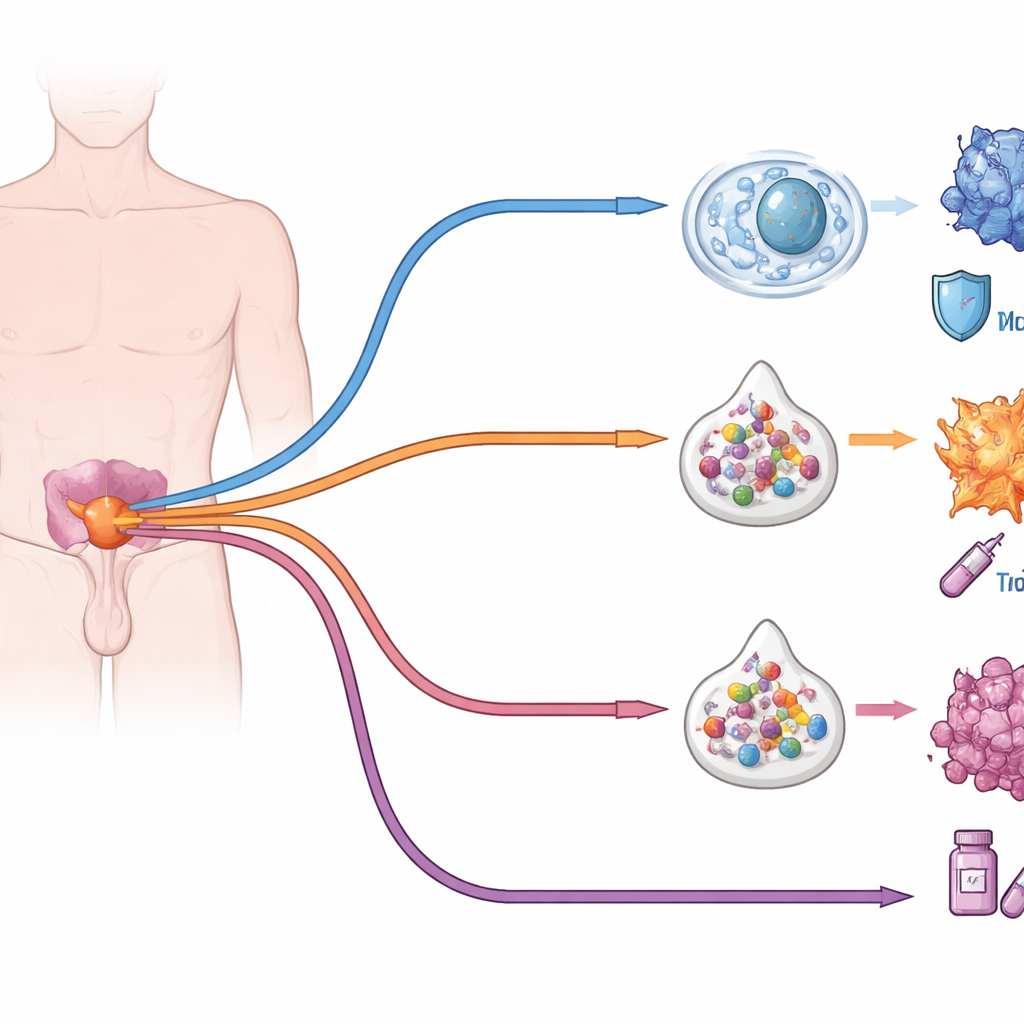
קריאת רקמה פגומה ברזולוציית תא-יחיד
רוב דגימות הפתולוגיה בבתי חולים נשמרות כבלוקים מקובעים בפורמלין ומטופלים בפרפין (FFPE), אשר מצוינים לאחסון ארוך טווח אך קשים לניתוח ברמת המולקולות. הצוות פיתח שתי שיטות משלימות המותאמות לדגימות אלה. הראשונה, שנקראת snFLARE-seq, מחלצת בעדינות גרעינים ותופסת RNA מתאים יחידיים תוך שבירה מבוקרת של קשרים כימיים. גישה זו מאפשרת למדענים למדוד אילו גנים כל תא מבטא, גם שנים לאחר הניתוח. השיטה השנייה, mxFRIZNGRND, משתמשת בהקפאה עמוקה, טחינה וממסים מותאמים כדי לשחזר גם מולקולות מסיסות במים וגם שומנים מבלי להשמיד תרכובות פגיעות. יחדיו, הכלים האלה חושפים גם את ה'הודעות' בתוך התאים וגם את המולקולות הקטנות שמזינות אותם.
כיצד תאי הגידול וסביבתם מתפצלים
ביישום snFLARE-seq על יותר מ-100,000 תאים מתוך גידולי ערמונית ואזורים נורמליים סמוכים, החוקרים מיפו 13 סוגי תאים עיקריים, כולל תאי אפיתל סרטניים, תאי מערכת חיסון ותאי סיב (פיברובלאסטים) תומכים. לגידולים באזור ההיקפי היה שפע של תת-סוגי אפיתל מסוימים שקדמו לקישור למחלות אגרסיביות. תת-סוג אחד הידוע כ'club' הציג הפעלה חזקה של מסלולי דלקת הקשורים ל-IL-17 ורגישות מוגברת להורמונים זכריים, וחתימת הגנים שלו חזה תוצאות גרועות במסדי נתונים ציבוריים גדולים של סרטן. לאחר טיפול הורמונלי, גידולים השולטים על שני האזורים לא התנהגו פשוט כמעין תערובת של גידולי אזור היקפי ומעברי. במקום זאת, התאים האפיתליאליים שלהם הפכו ל'ממוקדים': תת-סוגים אגרסיביים הפכו אפילו לדומיננטיים יותר, בעוד אחרים כמעט נעלמו, מה שמרמז שהטיפול יכול לעצב מחדש את הגידול ולא רק לכווצו.
הגנה חיסונית שהתהפכה
המחקר בחן גם כיצד תאי מערכת החיסון משתנים בין סוגי הגידול. בגידולים שלא טופלו, תאי T זיכרון ותאי T קוטלים היו שכיחים, ונוף המערכת החיסונית הכללי נראה דומה בין האזורים ההיקפי והמעברי. לאחר טיפול הורמונלי בגידולים החוצים אזורים, המאזן הזה השתנה. תאי T מותשים ותאי T רגולטוריים — שניהם ידועים בהחלשת התקפות חיסוניות — הפכו לשולטים, בעוד תאי מבצעים בעלי עוצמה פחתו. גם מקרופאגים ותאי דנדריטית נדחקו לעבר מצבים מדכאים יותר, בדומה ל'מ2' ופגמים בהצגת אנטיגן. שינויים רבים אלה לוּו בפעילות מוגברת של קולטנים לאנדרוגן ושינויים במטבוליזם הכולסטרול, מצב שמצביע על כיבוי חיסוני מונחה הורמונים ומתואם מטבולית שעשוי להגביל את תרומתן של אימונו-תרפיות בהמשך.
החיים הנסתרים של מטבוליזם הגידול
באמצעות mxFRIZNGRND, הצוות פרופיל יותר מאלף סוגי שומנים ומאות מטבוליטים נוספים בפרוסות רקמה תואמות. גידולי אזור ההיקפי הציגו פרופיל שומנים מפתיע ואחיד בדיד פעילות, מה שמרמז על מצב מטבוליטי 'רדום' שעשוי לסייע לתאים לעמוד בפני טיפולים מלחיצים. לעומת זאת, גידולים שחצו את שני האזורים לאחר טיפול הורמונלי הראו מסלולים מואצים שמספקים את אבני הבניין לממברנות תאים, לדנ״א ול-RNA, וכן לאנרגיה. שינויים מרכזיים כללו המרה מהירה של כולין לפוספטידילכולין לממברנות חדשות, הגברה בפירוק סוכרים, ותיתוך מחדש של סרמידים ומולקולות איתות שומניות אחרות. כאשר ממצאים מטבוליים אלה שולבו עם נתוני פעילות גנים ומאגרי נתונים גדולים על סרטן, ארבעה מסלולים מרכזיים — מטבוליזם של כולין ופוספוליפידים, מטבוליזם פחמני מרכזי, סינתזת פירימידין ומטבוליזם סרמידים — בלטו כקשורים בצמוד למחלה אגרסיבית ולתחזית גרועה.
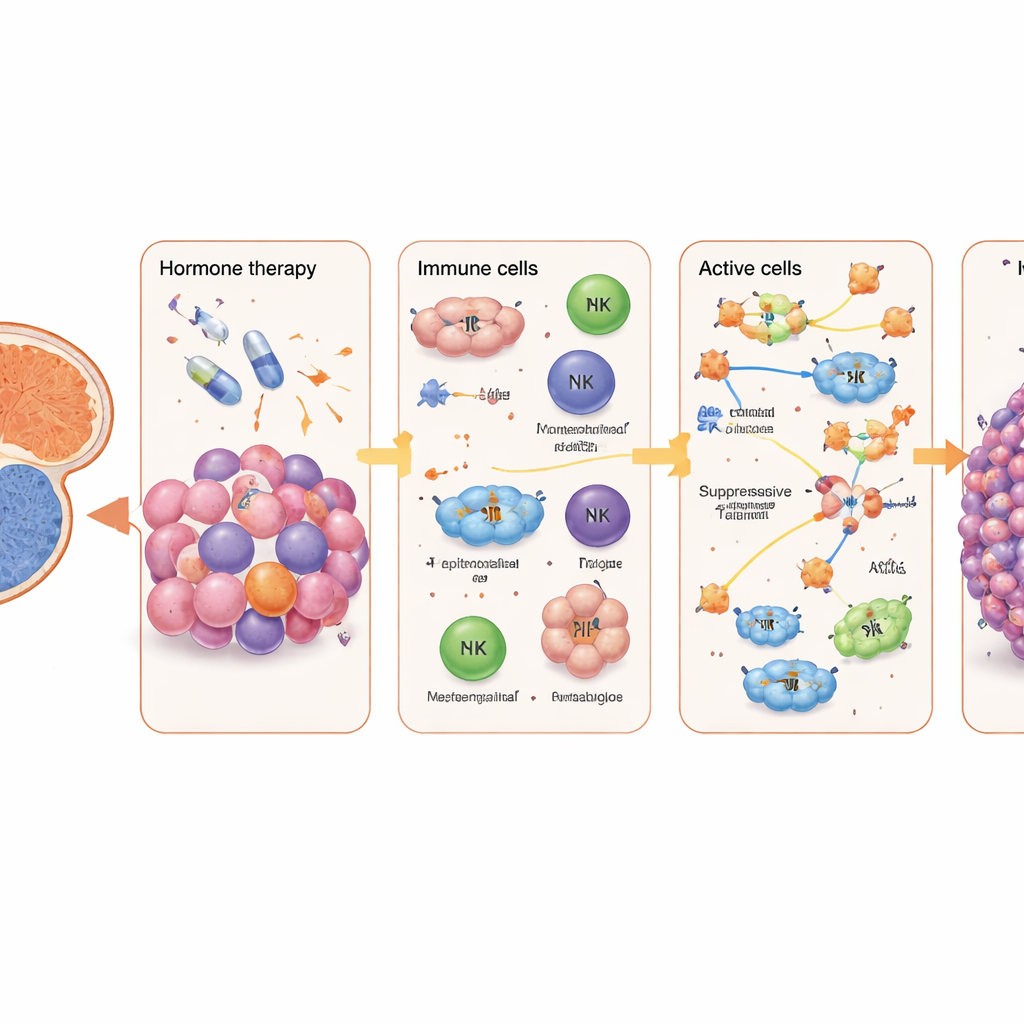
מה משמעות הדבר לטיפול עתידי
ללא רקע מקצועי, המסר העיקרי הוא שסרטן הערמונית אינו מחלה אחת אלא כמה, המעוצבות על־ידי מיקום ההתחלה שלהן ועל־ידי טיפולים שנועדו לשלוט בהן. טיפול הורמונלי עלול לבחור שלא בכוונה בתאים סרטניים עם מעגלי איתות הורמונליים חזקים במיוחד ולהתאים מחדש את תאי המערכת החיסונית והתומכים כך שיקדמו חזרה של המחלה. על ידי כרייה של דגימות FFPE ישנות עם snFLARE-seq ו-mxFRIZNGRND, חוקרים יכולים כעת לעקוב אחר מעברים אלה ברזולוציית תא-יחיד וברמה המטבולית בחולים אמיתיים, ולא רק במודלים מעבדתיים. בטווח הארוך, עבודה זו עשויה להוביל לטיפול מותאם אישית יותר: בחירת תרופות על פי אזור (למשל, כוונת IL-17 בגידולים היקפיים), הוספת חומרים החוסמים מסלולים מטבוליים מרכזיים כמו כולין או איתות PI3K-AKT, ותכנון שילובים חכמים של טיפולים הורמונליים ואימונותרפיות שממנועים היקיצה של תאים סרטניים רדומים תוך שמירה על הגנות הגוף.
ציטוט: He, D., Hu, H., Xiao, K. et al. Analysis of the transcriptomic and metabolomic landscape of prostate cancer with different anatomical origins using snFLARE-seq and mxFRIZNGRND. Nat Commun 17, 2461 (2026). https://doi.org/10.1038/s41467-026-69347-7
מילות מפתח: הטרוגניות של סרטן הערמונית, ריצוף תא-יחיד, מטבוליזם של גידול, התנגדות לטיפול הורמונלי, מיקרו-סביבה של הגידול