Clear Sky Science · he
הכונן הגנטי של אנצפלופתיה נמקית חריפה, RANBP2, מווסת את התגובה הדלקתית לזיהום בנגיף השפעת A
כשהשפעת פוגעת במוח
רוב האנשים תופסים את השפעת כפרק זמן של חום, שיעול ומנוחה במיטה. עם זאת, במקרים נדירים — ובמיוחד אצל ילדים — זיהום שגרתי בשפעת עלול לפתע להתפתח להפרעה מוחית מסכנת חיים הנקראת אנצפלופתיה נמקית חריפה (ANE). משפחות ורופאים חשדו זמן רב שגנים עשויים לקבוע מי יפתח את הסיבוך הקטסטרופלי הזה. מחקר זה חושף כיצד חלבון שער תאי יחיד, RANBP2, בדרך כלל שומר על הנגיף תחת שליטה ומונע מהתגובה הדלקתית של הגוף לברוח משליטה.
סיבוך נדיר אך הרסני של השפעת
ANE מופיעה באופן פתאומי לאחר מחלה עם חום, לעתים קרובות שפעת, ועלולה במהירות לגרום לפרכוסים, תרדמת ונזק עצבי ממושך. בערך מחצית מהמקרים הידועים של ANE בעולם מקושרים לנגיף השפעת A, ובפרט לזן H1N1. ילדים היורשים שינויים מסוימים בגן RANBP2 נמצאים בסיכון גבוה בהרבה, במצב הקרוי ANE1. עד כה, עם זאת, המדענים לא הבינו מה תפקידו המדויק של חלבון זה בזמן זיהום בשפעת, או מדוע שינוי בו גורם לדלקת מוחית כה קשה.
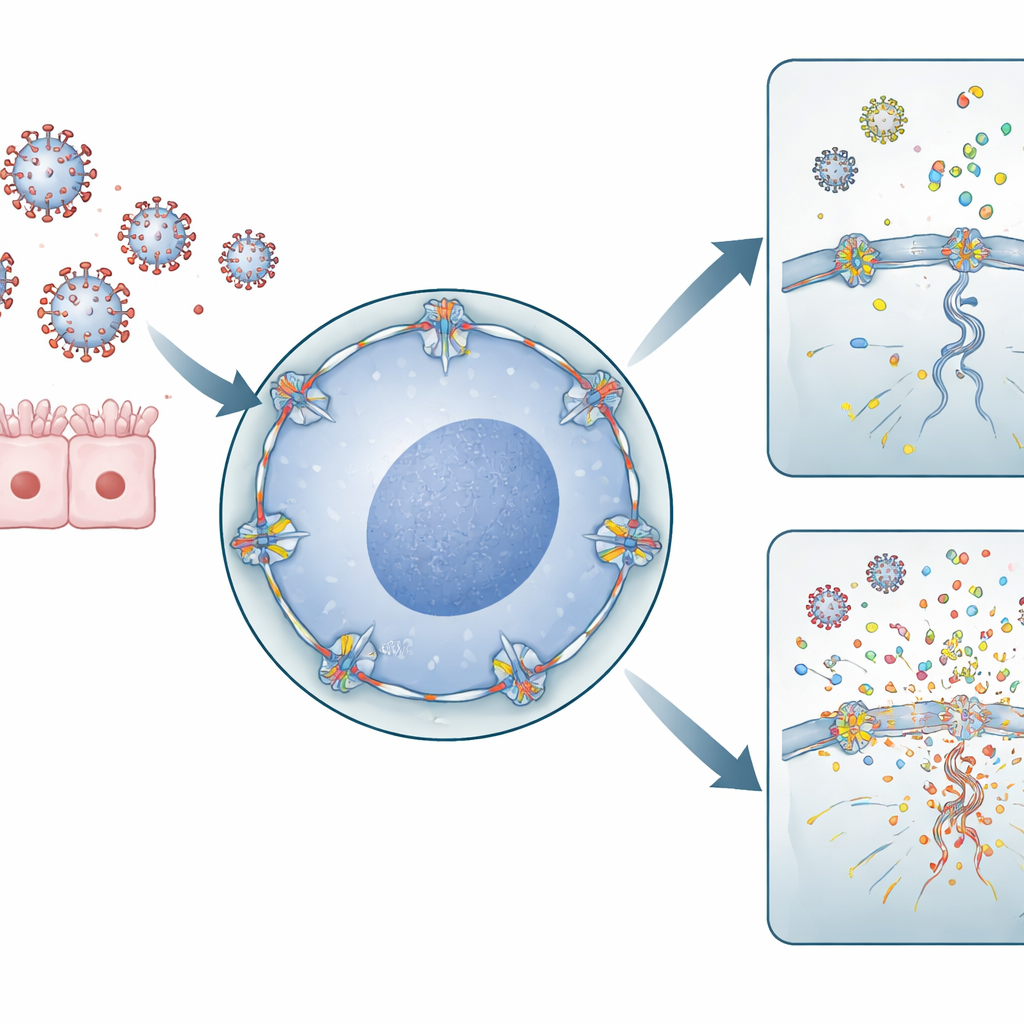
שערים תאיים וגנומי נגיף
לנגיף השפעת A יש אורח חיים יוצא דופן עבור נגיף RNA: הוא חייב להיכנס לגרעין התא כדי להעתיק את החומר הגנטי שלו. לשם כך הוא עובר דרך נקבוביות גרעיניות — שערים גדולים במעטפת הגרעין שמווסתים את התנועה בין הגרעין לציטופלזמה שמסביב. RANBP2 הוא מרכיב מרכזי בצד החיצוני של נקבוביות אלה. החוקרים השתמשו בתאים שמקורם בריאה אנושית ובתאי מערכת החיסון כדי להוריד רמות של RANBP2 או להכניס את המוטציה המקושרת ל‑ANE. הם גילו שכאשר RANBP2 נעדר או מוסט ממקומו, גנומי השפעת הועתקו ביתר בתוך הגרעין, וקטעים גנטיים ויראליים יצאו לציטופלזמה באופן לא מאוזן. באופן מפתיע, שפע זה של RNA ויראלי לא הניב יותר חלקיקים מדבקים של הנגיף, אך שינה את המקומות והאופן שבו החומר הויראלי הצטבר בתוך התא.
כאשר פסולת ויראלית מאכילה את מערכת האזעקה
מערכת החיסון נשענת על חיישנים מולקולריים שמזהים חתיכות RNA ויראלי משוטטות בציטופלזמה כאותות סכנה. הצוות הראה שבתאים שחסרו RANBP2 תקין, הצטברו בציטופלזמה קטעי RNA ויראלי עודפים, ויצרו בדיוק את הדפוסים שהחיישנים האלה מותאמים לזהות. בתאים שמקורם בריאה הדבר עורר רמות גבוהות יותר של מולקולות דלקתיות כגון IL‑6 ו‑IL‑1β. במקרופאגים ראשוניים אנושיים — תאי חיסון קו ראשון מתורמי דם — אובדן RANBP2 הוביל לזינוק בולט בכימוקינים פרו‑דלקתיים, כולל CXCL8, CXCL10, CCL2, CCL3 ו‑CCL4. מולקולות אלה מגייסות ומפעילות תאים חיסוניים נוספים ומעצימות את התגובה הכוללת לזיהום.
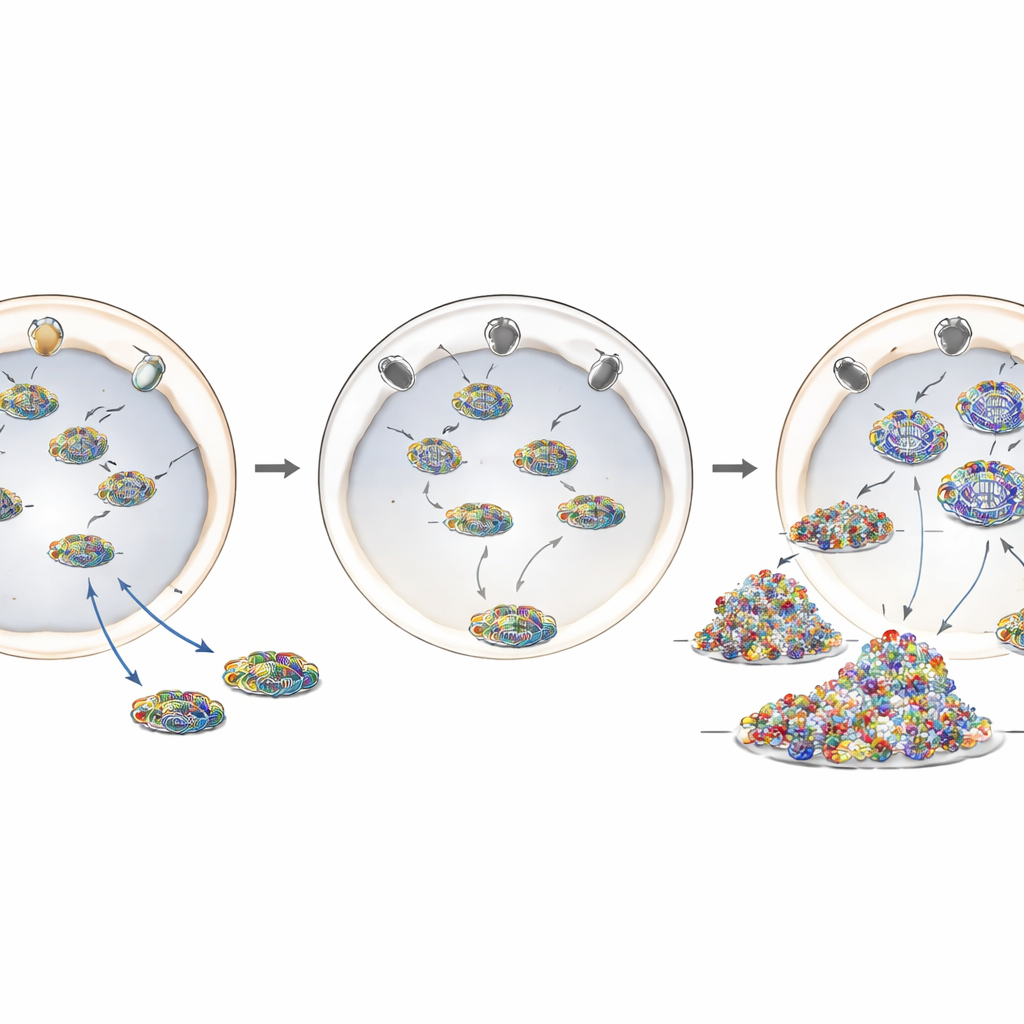
מוטציית מחלה שמסיטה שומרת
כדי לדמות טוב יותר את ANE1, החוקרים השתמשו בעריכת גנום CRISPR‑Cas9 כדי להכניס את השינוי השכיח ביותר הקשור למחלה, T585M, לתוך גן RANBP2 האנושי. בתאים שעברו עריכה זו, רמות חלבון RANBP2 היו ברובן תקינות, אך מיקומו לא היה כך: במקום להבחין בו כטבעת בוהקת סביב מעטפת הגרעין, חלק גדול מהחלבון הוסט לתוך פנים התא. תאים נשאים של מוטציה זו, בין אם בעותק גן אחד או בשני העותקים, התנהגו בדומה לתאים ממותני RANBP2. הם איפשרו שכפול גנומי שפעת מוגבר, הראו יותר חומר ויראלי בציטופלזמה והפעילו תגובה דלקתית חזקה יותר לאחר הזיהום. ממצא זה מרמז שמיקומן הנכון של RANBP2 בנקבוביות הגרעין — ולא כמותו הכוללת — קריטי לתפקידו המגן.
מדוע זה חשוב לילדים בסיכון
במבט כולל, הממצאים מציירים את RANBP2 כשומר תאי שמכוונן באופן עדין כיצד החומר הגנטי של השפעת זז פנימה והחוצה מהגרעין. כאשר RANBP2 נעדר או מוסט ממקומו, RNA ויראלי מועתק ביתר ויוצא בצורה כאוטית, וממלא את הציטופלזמה בפסולת מולקולרית שמעצימה במידה רבה את האותות החיסוניים. ברוב הרקמות המשמעות היא מחלת שפעת קשה יותר אך ניתנת להחלמה. אצל ילדים הפגיעים עם ANE1, עם זאת, דלקת שכזו — ובפרט אם היא מגיעה למוח — עשויה להסביר את הנזק הנוירולוגי החמור והפתאומי שנצפה לאחר זיהומים שבאופן אחר נראים שגרתיים. הבנת מסלול זה עשויה להנחות אסטרטגיות עתידיות לזיהוי מוקדם של מטופלים בסיכון ולהתאמת טיפולים אנטי‑דלקתיים לפני שהתגובה החיסונית תהפוך ממגינה להריסה.
ציטוט: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
מילות מפתח: שפעת, אנצפלופתיה נמקית חריפה, RANBP2, היפר־דלקת, נקבובית גרעינית