Clear Sky Science · he
תפקיד לאינטראקציה בין קונדנסין למדיייטור בארגון כרומוזומי מיטוטי
איך תאים מתחלפים שומרים על הבית הגנטי מסודר
בכל פעם שתא מתחלק, עליו לארוז ולהפריד בקפידה מטרים של DNA כדי שכל תא־בת יקבל סט שלם של כרומוזומים. כשתהליך זה נכשל התוצאה יכולה להיות מוות תאי, הפרעות בהתפתחות או סרטן. המחקר הזה חושף כיצד שני מכונות מולקולריות מרכזיות — אחת ששולטת בפעילות גנים ואחת שמדחסת את ה‑DNA — פועלות יחד לקיפול הכרומוזומים במהלך חלוקת התא, וחושף קשר נסתר בין האיזו גנים נדלקים במיטוזה לבין האם הכרומוזומים מתחלקים נכונה.
שחקנים מרכזיים: המדחס והמנחה
בגרעין פועל קומפלקס חלבוני שנקרא קונדנסין, המתפקד כמדחס מולקולרי — הוא לופק ומדקק את ה‑DNA לכדי הכרומוזומים העבים המאפיינים מיטוזה. קומפלקס גדול נוסף, מדיייטור, מסייע בוויסות אלו גנים מופעלים או מושתקים על‑ידי עבודה משותפת עם RNA פולימראז, האנזים שמעתיק DNA ל‑RNA. החוקרים בחנו קומפלקסים אלה בשמרת שחלה (fission yeast), אורגניזם מודל מבוסס שהביולוגיה הכרומוזומלית שלו דומה מאוד לזו של תאים אנושיים. הם גילו כי תת‑יחידה של הקונדנסין, Cnd1, נקשרת פיזית לתת‑יחידה של המדיייטור שנקראת Pmc4. אינטראקציה זו מתרחשת בגנים בעלי פעילות גבוהה ובקבוצת גנים מיוחדת שמופעלת רק במיטוזה. גנים אלה, "גני מיטוזה", יושבים בקצות שכונות כרומוזומליות גדולות — דומיינים — ונראים כאילו הם משמשים כסימני גבול.
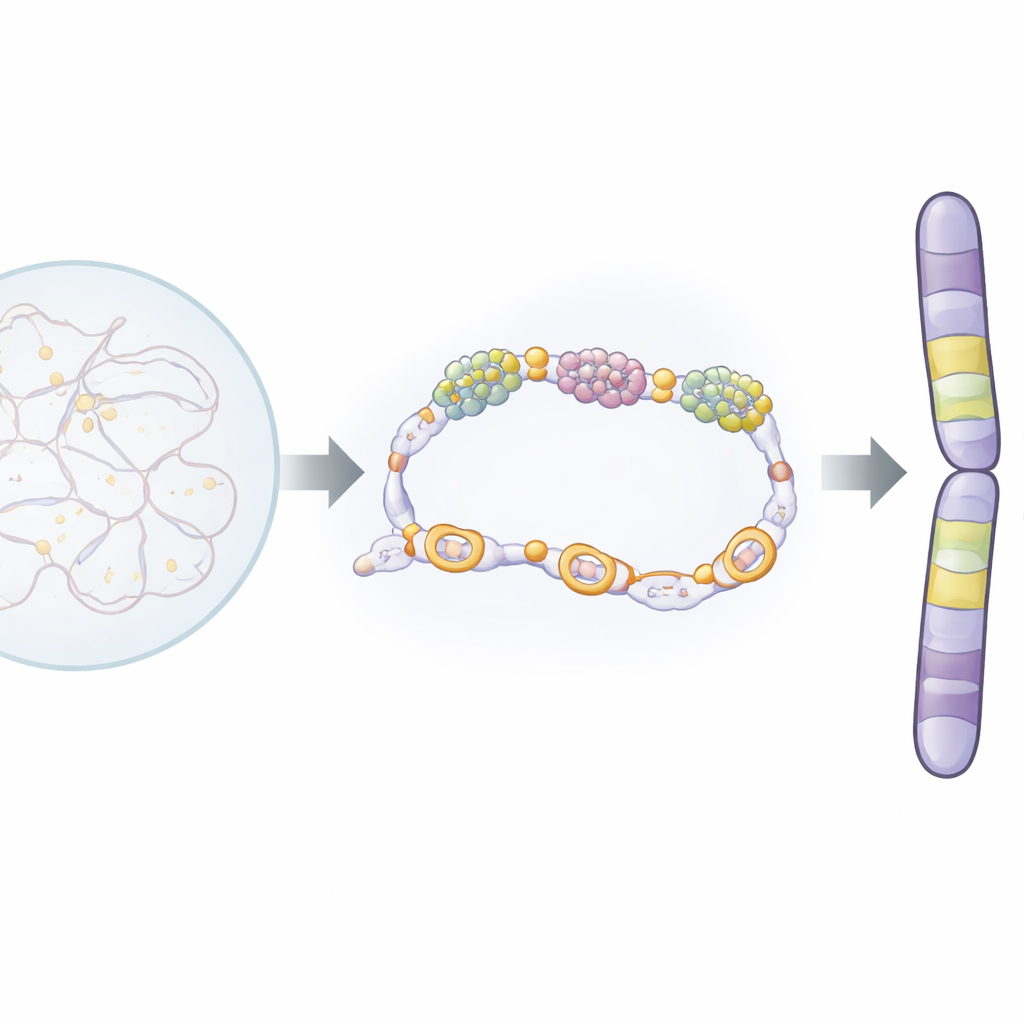
לחיצת יד מולקולרית אחת עם השלכות גדולות
כדי לבדוק עד כמה לחיצה זו חשובה, החוקרים מהנדסים מוטציה מדויקת ב‑Cnd1, ששינתה חומצה אמינית אחת בלבד (K658E), כך ש‑Cnd1 כבר לא יכולה לקשור את Pmc4 ועדיין יכולה להרכיב קומפלקס קונדנסין נורמלי. תאי שמרים הנשאים מוטציה זו היו חיים, אך הכרומוזומים שלהם נפרדו בשגיאות בתדירות גבוהה יותר, והשארו מקטעי DNA מאחרים במהלך מיטוזה. באמצעות מיפוי גנום תלת־ממדי (Hi‑C) והדידות מרחבית מיקרוסקופית בין נקודות DNA נבחרות, הראו החוקרים שהתאים המוטנטיים הפגינו קשרים מוחלשים הנוצרים על‑ידי קונדנסין ודומיינים כרומוזומליים פחות דחוסים. במילים אחרות, בלי אינטראקציית Cnd1–Pmc4 תקינה, קונדנסין לא הצליח לקפל את הכרומוזומים ביעילות למבנים מארגנים וחזקים המבוססים על דומיינים במהלך חלוקת התא.
פעילות גנים כבונה גבולות
המחקר בדק אחר כך כיצד מדיייטור תורם לקיפול זה. כאשר מורידו את Pmc4, קשירת הקונדנסין בהרבה גנים ירדה ועוצמת הדומיינים שנוצרו על‑ידי קונדנסין פחתה. באופן בולט, הגבולות בין דומיינים שכנים נעשו מטושטשים, ואינטראקציות DNA החלו לזרום מעבר למה שהיו גבולות חדים בעבר. מדידות RNA מפורטות חשפו שהיעלמות Pmc4 הורידה בעוצמה את הביטוי של תת‑קבוצה של גנים שמופעלים במיטוזה ונתונים לוויסות על‑ידי פקטור השעתוק Ace2. גנים גבוליים אלה בדרך כלל מציגים תפוסה גבוהה מאוד של מדיייטור, קונדנסין ופקטור שעתוק בסיסי הנקרא TBP. הנתונים תומכים במודל שבו מדיייטור ו‑TBP מגייסים תחילה את הקונדנסין לפרומוטרים של גנים בעלי פעילות גבוהה ושל גני מיטוזה; עם ההתקדמות של השעתוק הקונדנסין נדחף לאורך גופי הגנים ועוזר לארוג DNA סמוך ללולאות, כאשר גני יעד של Ace2 קובעים את קצוות כל דומיין מדוחס.
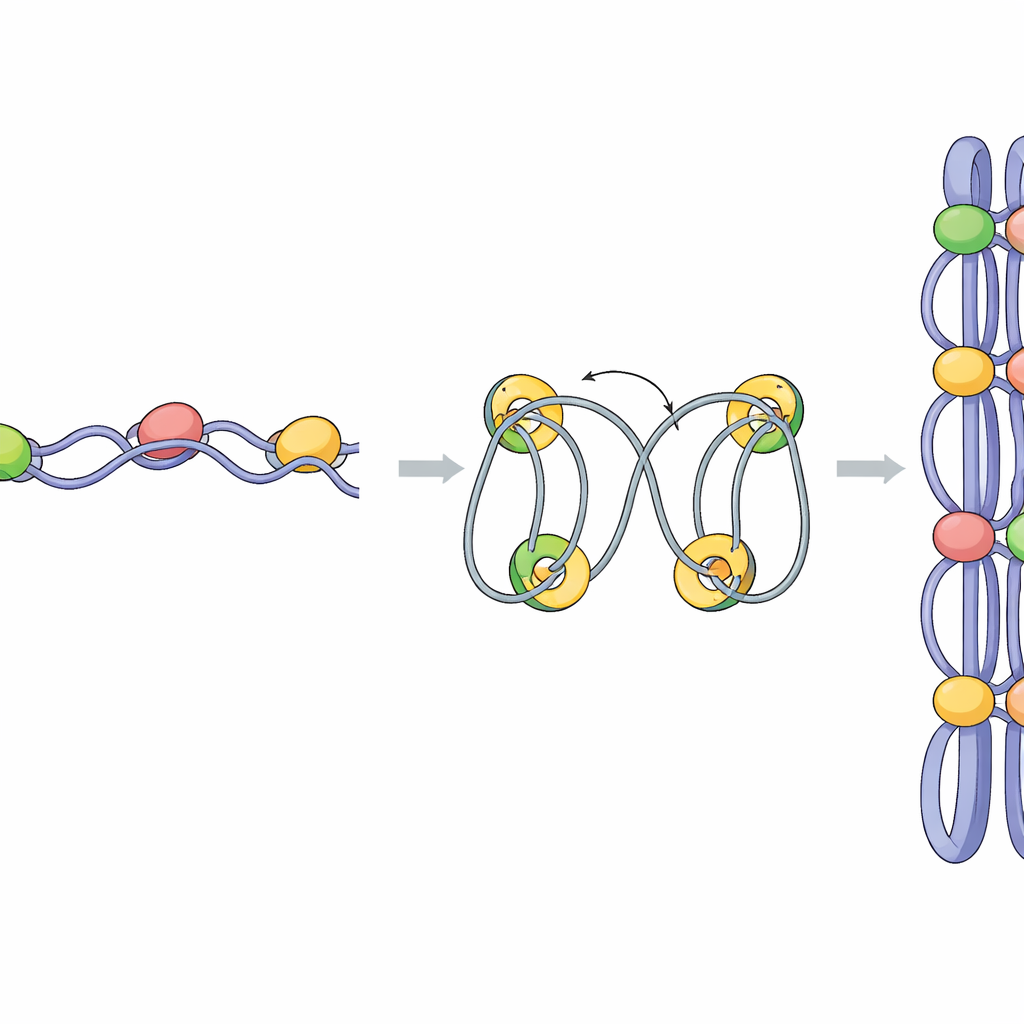
תפקיד אפשרי לטיפות בעלות אופי נוזל‑כמו
ידוע שמדיייטור בתאים אנושיים יוצר טיפות בעלות אופי נוזל‑כמו בתהליך שנקרא הפרדה פאזה, שיכול לרכז מכונת שעתוק במרכזים גרעיניים קטנים. החוקרים מצאו שמדיייטור של שמר השחלה מתנהג באופן דומה: תת‑היחידה Pmc4 יכולה ליצור טיפות במבחנה, וטיפול תאים ב‑1,6‑הקסנדיול, כימיקל המפרק קונדנסטים כאלה, פזר במהירות מוקדי מדיייטור בגרעין. טיפול קל בהקסנדיול החליש את קשירת המדיייטור והקונדנסין בגנים מרכזיים וטישטש ספציפית את הגבולות בין דומיינים כרומוזומליים, אף על פי שהדחיסה הכללית של הכרומוזומים נמשכה. ממצא זה מציע שטיפות עשירות במדיייטור בגני גבול מיטוטיים עשויות לסייע לעצב היכן דומיינים מתחילים ומסתיימים על‑ידי ריכוז פעולת השעתוק והטענת הקונדנסין באתרים אלה.
מלמידת שמרים לבריאות האדם
לבסוף בדקו החוקרים האם שותפות דומה קיימת בתאים אנושיים. באמצעות מבחן אינטראקציה מצאו שהםד4 (MED4), המקבילה האנושית של Pmc4, נקשרת באופן ספציפי ל‑CAP‑D3, תת‑יחידה של קונדנסין II הדומה ל‑Cnd1 בשמר. מוטציה אנושית ב‑CAP‑D3 המקבילה לשינוי K658E בשמר פגעה באינטראקציה זו וגרמה לשגיאות מיטוטיות, כגון כרומוזומים מסודרים בצורה שגויה ויצירת מיקרו‑גרעינים. ירידה ב‑MED4 גם היא יצרה פגמים בסגרגציה. מקבילות אלה מצביעות על כך שהקישור בין מדיייטור לקונדנסין הוא אסטרטגיה שמורה האבולוציונית שבאמצעותה תאים מתאמים בין פעילות הגנים לקיפול הכרומוזומים, ומבטיחים שה‑DNA נארז ונחולק באופן שווה במהלך חלוקת התא.
מדוע זה חשוב להבנת מחלות
עבודה זו מראה שדרך קיפול הכרומוזומים במיטוזה אינה רק עניין של דחיסה גסה. במקום זאת, היא תלויה במיקום ובזמן בהם גנים מסוימים נדלקים, כאשר שעתוק מונע‑מדיייטור בגני גבול מגייס קונדנסין כדי לעצב דומיינים בקנה‑מידה גדול. בכך שהיא מדגימה כיצד אינטראקציה אחת בין שני קומפלקסים יכולה להשפיע על ארכיטקטורת כרומוזום שלמה ועל נאמנות ההפרדה, המחקר מציע מסגרת חשיבתית המסבירה כיצד שינויים עדינים במכונות ויסות הגנים או בפונקציית הקונדנסין עשויים להוביל לאי־יציבות כרומוזומלית — סמן של סרטן ומחלות גנטיות רבות.
ציטוט: Iwasaki, O., Tashiro, S., Chung, C.YL. et al. A role for condensin-mediator interaction in mitotic chromosome organization. Nat Commun 17, 2509 (2026). https://doi.org/10.1038/s41467-026-69270-x
מילות מפתח: ארכיטקטורת כרומוזום, קונדנסין, קומפלקס מדיייטור, מיטוזה, ארגון גנום תלת־ממדי