Clear Sky Science · he
מפורקים של חלבון הקפסיד של וירוס הדנגי מציגים פרמקולוגיה מובחנת בהשוואה למעכבי הקפסיד
להפנות את מעטפת הוירוס נגדו
קדחת הדנגי מדביקה מאות מיליוני אנשים מדי שנה, ועדיין לרופאים חסרות תרופות אנטי‑ויראליות אמינות לטיפול בה. המחקר בוחן גישה חדשה לנטרול וירוס הדנגי באמצעות השמדה של אחד מרכיביו החשובים בתוך תאים נגועים, במקום לנסות רק לחסום את פעילותו. העבודה מראה שמולקולות מעוצבות בקפידה יכולות לתייג חלבון וירלי מרכזי להשמדה במערכת ניהול הפסולת של התא, להפחית את ייצור הוירוס ולהחליש את יכולתו להסתיר עצמו מפני ההגנה החיסונית שלנו.
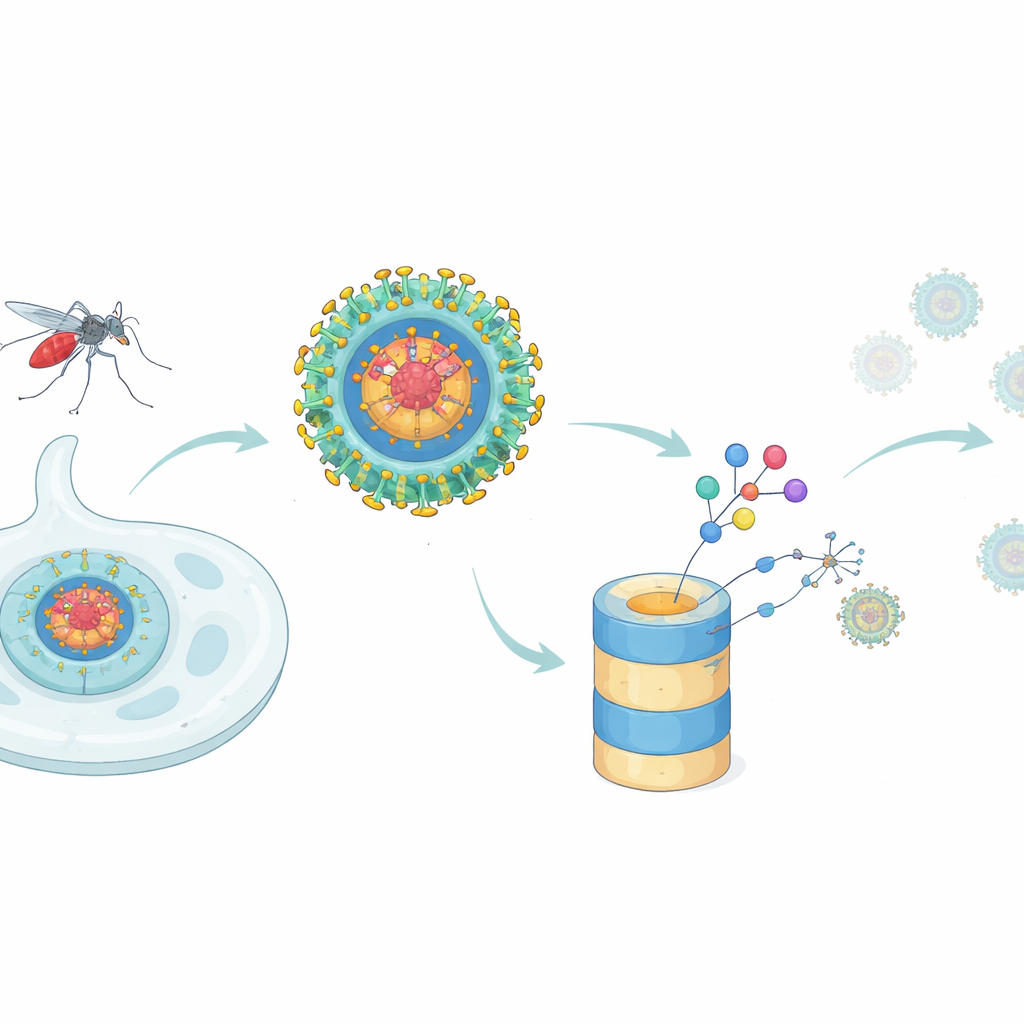
טקטיקה חדשה לעצירת הדנגי
רוב התרופות האנטי‑ויראליות פועלות כמו פקקים במכונה: הן מתיישבות על אתר תפקודי אחד של חלבון וירלי ומנסות לחסום אותו. גישה זו מתקשה כשחלבון וירלי מבצע משימות רבות, או כשמוטציות קטנות מחלישות את אחיזת התרופה. חלבון הקפסיד של הדנגי הוא דוגמה מרכזית לכך. הוא יוצר את מעטפת הליבה שמארזת את החומר הגנטי של הוירוס בחלקיקים חדשים, אך גם מתערב בתפקודי התא המאכסן על‑ידי אינטראקציה עם חלבונים אנושיים רבים ובהשתקת תגובת האינטרפרון של הגוף, אזעקה אנטי‑ויראלית בקו החזית. החוקרים שאלו האם קונספט תרופתי חדש — הידרדרות ממוקדת של חלבונים — יכול להתעלות על מעכבים קלאסיים על‑ידי הסרה ממשית של חלבון הקפסיד מתוך תאים נגועים.
עיצוב "צייד פרסים" מולקולרי
כדי לבנות כזה מפורק, החוקרים התחילו מ‑ST148, מולקולה קטנה ידועה שנקשרת לקפסיד של הדנגי ומפריעה להרכבת חלקיקים ויראליים חדשים. הם קישרו כימית את ST148 למודול שני המגייס קומפלקס אינזימטי אנושי האחראי לתיוג חלבונים להרס. המולקולות הכימריות הנוצרות, הנקראות PROTACs, מעוצבות לתפוס את הקפסיד בקצה אחד ואת קומפלקס ליגאז E3 בקצה השני, לקרב ביניהם כך שהקפסיד יסומן בתגי יוביקוויטין וידגם לפרוטאוזום של התא — המכתש הראשי של החלבונים. באמצעות בדיקות של אורכי קישורונים וקבוצות מגייסות ליגאז שונות, זיהו compound בולט אחד, שכונה RPG‑01‑132, שהפחית באופן מהימן את רמות הקפסיד בתאים נגועים באופן התלוי בצורת ה‑CRBN של הליגאז ובתפקוד תקין של הפרוטאוזום.
כיבוי ייצור הוירוס והתחמקות מהחיסון
לאחר שהיה להם מפורק עובד, הצוות בדק מה הוא עושה למעשה לזיהום הדנגי. בתאים שמקורם בכבד הנגועים בוירוס הדנגי, RPG‑01‑132 גרם לירידה חזקה במספר הוירוסים המדבקים שמשתחררים, בריכוזים שבהם הוא הוריד רק באופן חלקי את רמות הקפסיד הכוללות. חשוב מכך, חלבונים ויראליים אחרים ורנ״א ויראלי נותרו ללא שינוי, מה שמעיד שהתרכובת לא רעלת פשוט את השכפול הכולל אלא פעלה באופן ספציפי דרך איבוד הקפסיד. מיקרוסקופ אלקטרונים סיפק קריאה ויזואלית: תאים שטופלו במעכב המקורי ST148 צברו ערימות של חלקיקים ויראליים חלקית מורכבים ברשת האנדופלזמטית, בהתאמה לחסימה בהרכבה, בעוד תאים שטופלו במפורק הראו כמעט אין חלקיקים נראים כלל. המפורק גם הפחית את יכולת הקפסיד להשתיק איתות אינטרפרון‑β במערכת דיווח, דבר שמרמז שתפקידו הלא‑מבני של הקפסיד בדיכוי המערכת החיסונית המולדת יכול להתהפך על‑ידי פירוקו.
להתגבר על גיוון ויראלי והתנגדות לתרופות
וירוס הדנגי קיים בארבעה סרוטיפים עיקריים השונים בתגובתם למעכבי מטרה המבוססים על הקפסיד, ועמידות יכולה להופיע כתוצאה ממוטציות בודדות. המחברים השוו את המפורק ל‑ST148 על פני זני ייצוג מכל ארבעת הסרוטיפים ונגד וירוס הנושא מוטציה (S34L בקפסיד) שהוכחה בעבר כגורמת ל‑ST148 לא להיות יעיל. כפי שציפו, ST148 עבד הכי טוב על סרוטיפ אחד ואיבד פעילות נגד המוטנט העמיד. RPG‑01‑132, בניגוד לכך, הראה עוצמה אנטי‑ויראלית דומה על פני כל הסרוטיפים ושמר פעילות נגד מוטציית S34L, ועדיין פעל דרך אותו מסלול פירוק התלוי ב‑CRBN. זה ממחיש יתרון מרכזי של פרמקולוגיה "מונעת־אירועים": המפורק לא צריך להיצמד בחוזקה לכל מולקולת קפסיד בכל העת, כל עוד הוא מסוגל להצית מספיק אירועי פירוק כדי להטות את המאזן.
מה משמעות הדבר לטיפולים עתידיים בדנגי
מחקר זה מראה שניתן לתקוף את חלבון הקפסיד של הדנגי לא רק כמרכיב מבני של הוירוס אלא כצומת ניתנת להסרה שתומכת בצעדים רבים של זיהום והתחמקות חיסונית. על‑ידי המרת מעכב מסורתי למפורק, יצרו החוקרים תרכובת החוסמת ייצור ויראלי, מסירה חלק מהדיכוי של המערכת החיסונית המולדת על‑ידי הוירוס, ונשארת יעילה מול זני וירוס מגוונים ומוטציית עמידות ידועה. RPG‑01‑132 עצמה תצטרך אופטימיזציה — כניסה טובה יותר לתא, פעילות חזקה יותר במודלים של בעלי חיים ובדיקות בטיחות קפדניות — אך היא מספקת הוכחה משכנעת לקונספט. באופן רחב יותר, העבודה מציעה כי חטיפת מנגנון ההשמה של התא יכולה לפתוח דרכים חדשות לתרופות אנטי‑ויראליות שקשה יותר לווירוסים להתחמק מהן ושהן יכולות לנטרל חלבונים בעלי תפקידים מרובים בתוך תאים נגועים.
ציטוט: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
מילות מפתח: וירוס הדנגי, חלבון הקפסיד, הידרדרות ממוקדת של חלבונים, עיצוב תרופות אנטי‑ויראליות, PROTACs