Clear Sky Science · he
מיקוד בתיקון NHEJ מפעיל איתות STING דרך פירוק MYC כדי להגביר את החיסון נגד גידולים ב-SCLC
מדוע המחקר הזה חשוב
סרטן הריאה מסוג תאים קטנים הוא אחד הסרטנים הקטלניים ביותר, כאשר רוב החולים חיים פחות משנה אחרי האבחנה. באופן מפתיע, לגידולים אלה יש רבות ממוטציות ה-DNA שצריכות להפוך אותם למטרות קלות למערכת החיסון, אך בפועל הם מגיבים בצורה לקויה לתרופות אימונותרפיה מודרניות. מחקר זה חושף מעצור מולקולרי נסתר שמונע מהמ��כת החיסון לזהות את הגידולים ומדגים כיצד כיבוי חלבון מפתח בתיקון DNA יכול להפוך את הגידולים האלה מ"קרים" ל"חמים", ולאפשר לטיפולים קיימים לפעול בצורה טובה בהרבה.
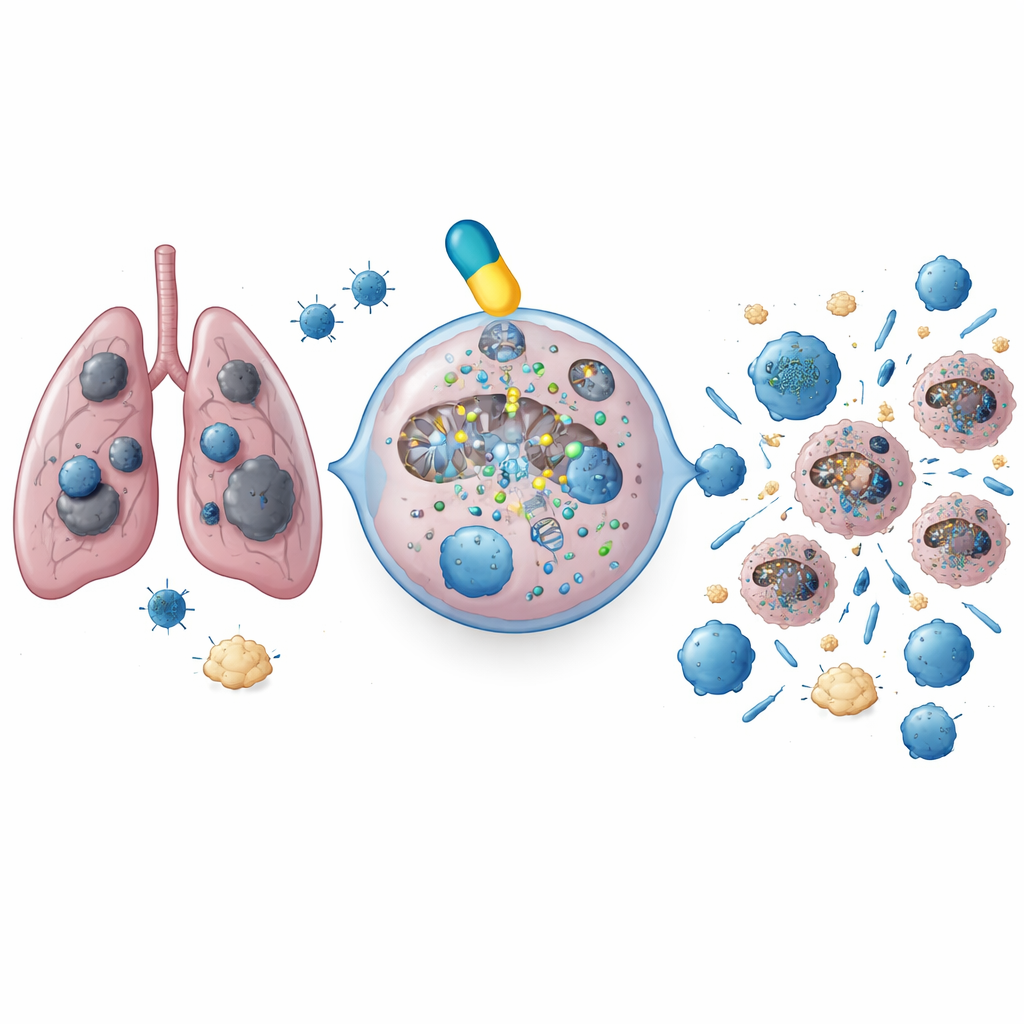
מתג תיקון נסתר בגידולי ריאה
החוקרים התחילו בסינון נתונים גנטיים מיותר מ-179,000 גידולים אנושיים ב-24 סוגי סרטן. הם התמקדו במסלול תיקון DNA שנקרא nonhomologous end joining, שמתקן שבירות מסוכנות בגדילי ה-DNA. בקרה מרכזית של מסלול זה, חלבון בשם DNAPKcs (מורכב על ידי הגן PRKDC), התגלה ברמות גבוהות מהרגיל בסרטן הריאה מסוג תאים קטנים. מתוך אלפי דגימות של גידולי ריאה, המקרים של תאים קטנים הראו את הפעילות החזקה ביותר של מתג התיקון הזה. חולים שלגידוליהם היו רמות PRKDC הגבוהות ביותר חיו פחות זמן והיו פחות סבירים להפיק תועלת מכימותרפיה ותרופות מעכבות צ'קפוינט סטנדרטיות, מה שאומר ש-DNAPKcs מסייע לגידולים לשרוד גם נזק ל-DNA וגם מתקפת מערכת החיסון.
מנזק DNA לאזעקה פנימית
כדי לראות מה קורה כאשר משנה התיקון הזה מוסתר, הקבוצה השתמשה הן בתרופות והן בכלי השתקה גנטית לחסימת DNAPKcs בלוחות תאים של סרטן הריאה מסוג תאים קטנים ובמודלים חייתיים של גידולים. ברבים מהדגמים האלה, במיוחד באלה המזכירים תת-סוגים אנושיים עם פעילות אונקוגנית גבוהה של MYC, מעכבי DNAPKcs הפחיתו באופן חזק את גדילת תאי הגידול ואף הקטינו גידולים שמקורם בחולים בעכברים. ברמה התאית, חסימת DNAPKcs הובילה להצטברות של DNA שבור, הנראה כנקודות של סימן נזק בתוך הגרעין וכגופים קטנטנים מלאי DNA הנקראים מיקרו-גרעינים. שברי DNA אלה דלפו לציטופלסמה של התא, שם הם יכולים להיתפס כאותות סכנה.
הפעלת מערכת האזעקה ה"ויראלית" של התא
DNA חופשי במקום הלא נכון הוא בדרך כלל סימן לזיהום ויראלי. תאים מזהים זאת בעזרת גלאי בשם cGAS, שמפעיל נתיב אזעקה יורד בשם STING. המחברים הראו שאחרי חסימת DNAPKcs, cGAS התקבץ על המיקרו-גרעינים, STING הופעל, ומסלול של מולקולות המעוררות חיסון הופעל. התאים ייצרו יותר אינטרפרונים מסוג I ו-II וכימוקינים המגייסים תאים חיסוניים. גם התצוגה המשטחית של חלבוני "דגל" מרכזיים (מולקולות MHC מחלקה I), המסייעים לתאים החיסוניים לזהות אנטיגנים של הגידול, עלתה. כאשר נתיב ה-STING נחסם כימי או הושתק גנטית, שינויים אלה נעלמו ברובם, וההשפעות האנטי‑גידוליות של עיכוב DNAPKcs היו חלשות הרבה יותר, מה שמדגיש שמערכת אזעקה פנימית זו חיונית לתגובה.
חיסול MYC כדי לגלות את הגידול
המחקר מקשר נוסף בין DNAPKcs ל-MYC החזק, מנהיג גדילה שנחשב זמן רב כ"לא ניתן לתרופה". בגידולים עם פעילות MYC גבוהה, עיכוב DNAPKcs הקטין איתות AKT הפעיל ושחרר מעצור מולקולרי על אנזים אחר, GSK3β. לאחר שהופעל, GSK3β תייג את MYC להרס, וכתוצאה מכך רמות החלבון MYC ירדו. הורדה ישירה של MYC בעזרת כלים גנטיים חיקתה רבות מהשפעות ההפעלה החיסונית של חסימת DNAPKcs: איתות STING עלה, גני אינטרפרון הופעלו, ורמת MHC מחלקה I עלתה. להיפך, אילוץ תאים לייצר עודף MYC למחצה ביטל במידה רבה את ההשפעה המגבירה חיסון של מעכב DNAPKcs. ממצאים אלה מצביעים על כך ש-DNAPKcs בדרך כלל מסייע לייצוב MYC, ושדחיפת MYC לעבר פירוק היא שלב מרכזי בהפעלת מנגנון החיסון נגד הגידול.
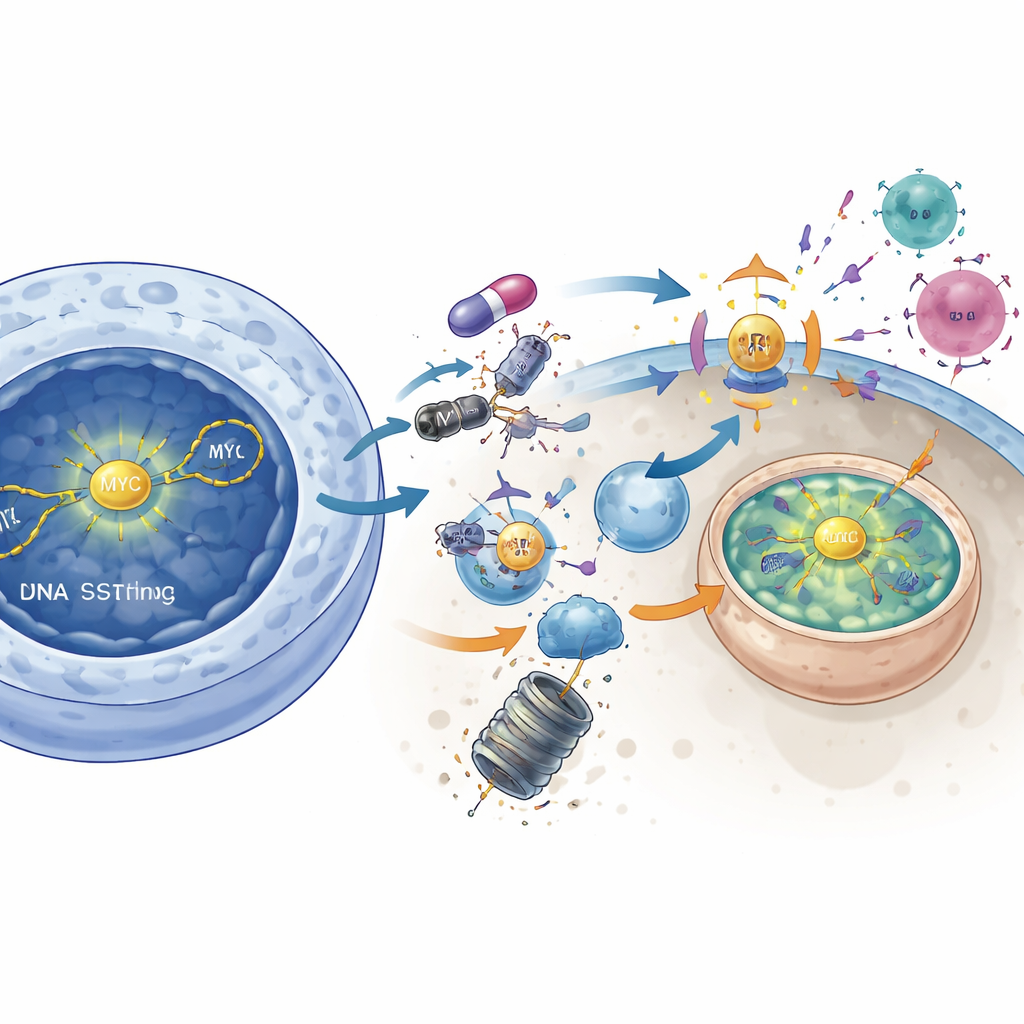
מגידולים "קרים" ל"חמים" במודלים חיים
במודלים עכבריים עם מערכת חיסון תקינה המדמים במדויק את סרטן הריאה מסוג תאים קטנים אנושי, טיפול במעכב DNAPKcs בלבד האט או הקטין משמעותית את הגידולים. חשוב לציין כי שילוב המעכב עם תרופת צ'קפוינט נגד PD-L1 קיימת הפך גידולים שהיו עמידים בעבר, והוביל לסלקציה דרמטית של הגידול ולעיתים להיעלמות מוחלטת. פרופיל חיסוני מפורט הראה שחסימת DNAPKcs הגדילה את תאי ה-CD8 ההורגים סרטן, חיזקה מאקרופאגים דלקתיים מסוג M1, הפחיתה תאים מדכאים והגבירה את רמות MHC מחלקה I בגידולים. הסרת תאי CD8 או השתקת STING בטל את היתרונות הללו, ואיששה שהטיפול פועל על ידי הפיכת הגידול לאות למשיכת התקפת מערכת החיסון ולא רק על ידי הרג ישיר של תאי הסרטן.
מה זה אומר עבור החולים
ביחד, התוצאות הללו חושפות את DNAPKcs כמנהל מרכזי הן של תיקון DNA והן של התחמקות מחיסון בסרטן הריאה מסוג תאים קטנים. על ידי חסימת DNAPKcs, הגידולים צוברים נזק ל-DNA, MYC מתייצב פחות, אזעקת cGAS–STING מופעלת, ונתיבי אינטרפרון והצגת אנטיגן נדלקים. רצף אירועים זה ממיר גידולים אילמים חיסונית לאלה שמגיבות בחוזקה לחסימת צ'קפוינט ולכימותרפיה במודלים פרה‑קליניים. למרות שעדיין דרושים ניסויים קליניים, העבודה מרמזת שמעכבי DNAPKcs הקיימים יכולים להיות משולבים עם אימונותרפיה כדי לתת לחולים עם סרטן אגרסיבי זה סיכוי טוב יותר לשליטה ממושכת.
ציטוט: Chakraborty, S., Elliott, A., Sen, U. et al. Targeting NHEJ activates STING signaling through MYC degradation to boost antitumor immunity in SCLC. Nat Commun 17, 2597 (2026). https://doi.org/10.1038/s41467-026-69262-x
מילות מפתח: סרטן הריאה מסוג תאים קטנים, עיכוב תיקון DNA, נתיב STING, פירוק MYC, אימונותרפיה נגד גידולים