Clear Sky Science · he
הפטוציטים מתוכנתים תפקודית על ידי תאי סרטן קולורקטלי עם ביטוי גבוה של KIAA1199 ומקדמים הצטברות של נויטרופילים פרו‑מטסטטיים Egr1+
כאשר סרטן המעי התפתח לכיוון הכבד
רוב האנשים מדמיינים הפצה של סרטן כיציאה של תאים מרדנים שמתנתקים ופשוט נסחפים לאיברים חדשים. המחקר הזה מצייר סיפור מטריד יותר: גידולים קולורקטליים יכולים באופן שקט לשנות את הכבד הרבה לפני שהתווספו אליו תאי סרטן, ולבנות "אדמה" מסבירת פנים שבה גידולים עתידיים שורשים בקלות רבה יותר. הבנת שלב ההכנה הסמוי הזה עשויה לפתוח פתח לטיפולים שעוצרים גרורות כבד — הסיבה העיקרית לתמותה בסרטן קולורקטלי — עוד לפני שהן מתחילות.
היערכות חשאית לפני הגעת הגידולים
סרטן קולורקטלי מדבק לעתים קרובות לכבד, אך רק חלק מהגידולים מפיצים עצמם באופן אגרסיבי. המחברים התרכזו במולקולה בשם KIAA1199, השכיחה בגידולים בסיכון גבוה. במודלים של עכברים ובמדגמי חולים נמצא כי גידולים עם ביטוי גבוה של KIAA1199 לא רק גדלו מהר יותר; הם גם הכינו את הכבד להיות "נישה קדם‑מטסטטית" — מיקרו‑סביבה שנוחה באופן יוצא דופן לתאי סרטן נכנסים. גם כשהזריעו גרורות לכבד ממקור נפרד בניסויים, בעכברים שנשאו גידולי מעי עם KIAA1199‑גבוה התפתחו הרבה יותר גרורות בכבד והם נפטרו מוקדם יותר. ממצאים אלה הראו כי אותות מהגידול הראשוני, ולא רק תאים נודדים, משנים את הכבד מראש.
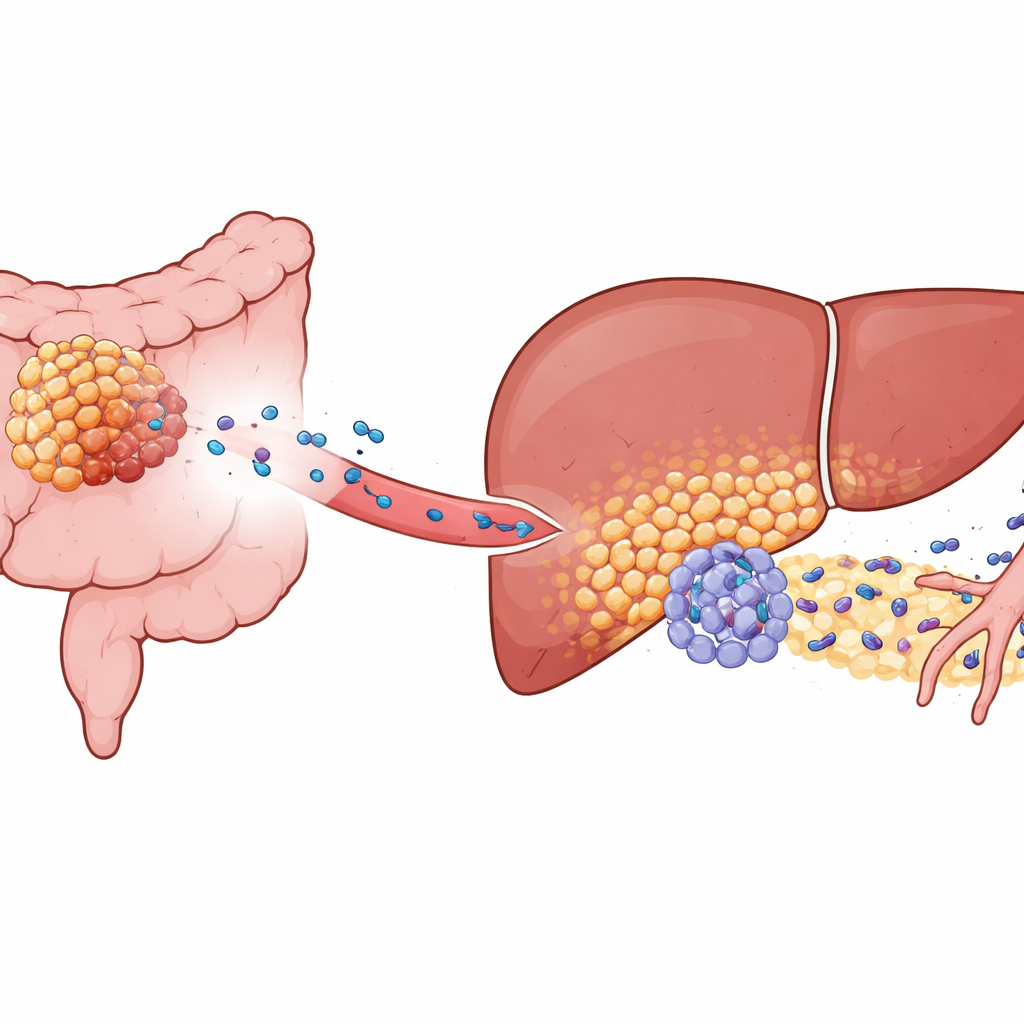
תאי כבד מתכנתים מחדש להופעה כעוזרים לגידול
בהעמקה נוספת השתמשו החוקרים ברצף חד‑תאי ומיפוי מרחבי כדי לבחון רקמת כבד ברזולוציה גבוהה. הם גילו תת‑אוכלוסייה מובחנת של הפטוציטים — תאי העבודה הרגילים של הכבד — שעברו "תכנות פונקציונלי מחדש". תאים אלה הופיעו רק בנוכחות גידולים עם ביטוי גבוה של KIAA1199. במקום לנהל שקט את המטבוליזם, ההפטוציטים המותאמים עברו לאופן מטבולי דמוי‑ממאירות והורידו את הפעילות של רגולטור מגן בשם PPARγ, שלרוב עוזר לשלוט בדלקת ובתגובות מול מתח. עם דיכוי PPARγ, הפטוציטים החלו לייצר רמות גבוהות של חלבון בשם SAA2, ששחררו לסביבה, במיוחד בגבול שבו רקמת הכבד פוגשת תאים גידוליים פולשים.
הפיכת מגנים רגילים לנויטרופילים פרו‑מטסטטיים
נויטרופילים — תאי דם לבנים הידועים בלחימתם בזיהומים — התנהגו גם הם בצורה חריגה בכבד המוכונן. המחברים זיהו תת‑אוכלוסייה מיוחדת שנושאת חתימת "Egr1+", על שם גורם שעתוק שמשנה את תפקוד התאים הללו. במקום להגיע מהשיליה כבר במצב מושתל, נראה שנויטרופילים עוברים חינוך מחדש מקומי על ידי ההפטוציטים המתוכנתים. SAA2 ששוחרר מהפטוציטים נקשר לקולטן בשם FPR2 על נויטרופילים סמוכים, והפעיל מסלול איתות פנימי PI3K‑AKT שייצב את פעילות Egr1. התוצאה היתה נויטרופיל בעל אורך חיים מוגבר ופעילות גבוהה, שהפריש כמויות גדולות של VEGFA, מניע חזק של יצירת כלי דם חדשים. נויטרופילים אלה Egr1+ התקבצו בממשק בין הגידול והכבד, בדיוק במקום שבו כלי דם חדשים ורגישים נבטו.
בניית כלי דם שמקבלים את פני תאי הגידול
המחקר מראה כי נויטרופילים משוכנעים אלה אינם רק עברים שוליים — הם משנים באופן פעיל את מבנה כלי הדם בכבד. בתרבית תאים, גורמים ששוחררו על ידי נויטרופילים Egr1+ עוררו תאי אנדותל לגדול, לנוע ולהיווצר למבנים בצורת צינור שמזכירים כלי דם חדשים. בעכברים, הוספת נויטרופילים Egr1+ הגברה את הגרורות בכבד והאיצה את המוות. חסימת שלבים מרכזיים בשרשרת — או את אות SAA2–FPR2 לנויטרופילים או את מסלול ה‑PI3K‑AKT ההמשך — קטעה את השרידות של הנויטרופילים ואת יצור ה‑VEGFA, צמצמה את צמיחת כלי הדם ואת התפשטות המטסטזות. באופן דומה, השבתת פעילות PPARγ בהפטוציטים בעזרת התרופה ל‑סוכרת רוזיגליטזון הורידה את רמות ה‑SAA2, צמצמה את הופעת נויטרופילים Egr1+ והורידה באופן חד את גרורת הכבד במודלים פריקליניים.
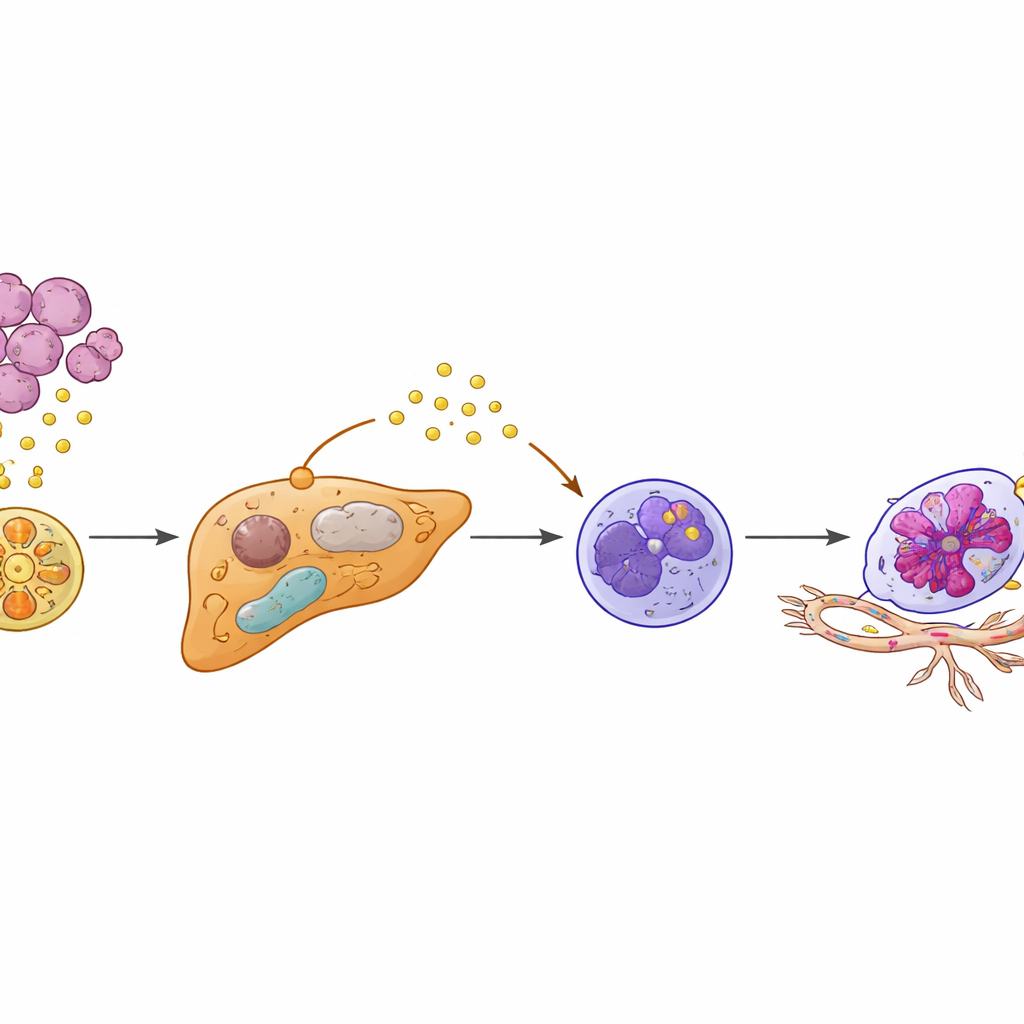
ממנגנון לחיזוי ומניעה
מכיוון ש‑KIAA1199 בגידולים ו‑SAA2 בכבד עומדים קרוב לראש של הקסקדה הזו, המחברים בחנו האם חלבונים אלה עשויים לסייע לזהות מטופלים בסיכון גבוה לגרורות כבד. במספר קבוצות חולים, אנשים עם רמות דם גבוהות של שני הסמנים היו בעלי סבירות גבוהה יותר לפתח גרורות בכבד ולעשות זאת מוקדם יותר. ציון משולב פשוט של KIAA1199–SAA2 עלה על כל אחד מהסמנים בנפרד בניבוי הסיכון והוכלל לנומוגרמה קלינית שמעריכה את הסבירות האינדיבידואלית להפצת הכבד בשנים הבאות. יחד, הממצאים מציירים תמונה ברורה: גידולי מעי עם ביטוי גבוה של KIAA1199 משדרים אותות נשאים‑וזיקולות שמטמעות מחדש את ההפטוציטים, שממנפים בתורם נויטרופילים סמוכים לנוטרופילים ארוכי‑חיים ובוני‑כלי דם. באמצעות ייעוד ציר KIAA1199–PPARγ/SAA2–Egr1 — דרך תרופות מטבוליות, סוכנים שמשנים את המערכת החיסונית, או שניהם — יתכן שאפשר לא רק לטפל בגרורות כבד קיימות, אלא גם למנוע את התקנתן מלכתחילה.
ציטוט: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
מילות מפתח: גרורת כבד מסרטן קולורקטלי, נישה קדם‑מטסטטית, נויטרופילים, תכנות מחדש של הפטוציטים, מיקרו‑סביבה גידולית