Clear Sky Science · he
הפחתת מתילציה של היסטון 3.3 באתר ליזין 4 במרכז הגנגליוני המדיאלי וההיפותלמוס משחזרת פנוטיפים של הפרעות בהתפתחות העצבית
איך תגים כימיים זעירים מעצבים מוח וגוף
מדוע שינויים גנטיים מסוימים גורמים גם לקשיי למידה וגם לצמיחה בלתי שגרתית, למשל להיות קטנים מאוד בילדות אך שמנים בבגרות? המחקר בוחן תגים כימיים זעירים על חלבוני עיטוף ה-DNA במוח ומראה כיצד הפרעה בהם בשתי אזורים מרכזיים בלבד יכולה להתפשט ולהביא להתקפים, להתנהגויות הדומות לחרדה, לבעיות בזיכרון ושינויים דרמטיים בגודל הגוף בעכברים.
מתגים על כפתורי הדימר של הגנום
בתוך כל תא מוח ה-DNA כורכר סביב חלבונים דמויי גליל שנקראים היסטונים. סימנים כימיים המונחים על היסטונים אלה פועלים כמו כפתורי דימר, שמגבירים או מדכאים קבוצות של גנים. סימן אחד כזה, המתווסף למיקום שנקרא H3K4, קשור בחוזקה להפעלת גנים. מחקרים גנטיים בבני אדם הראו שאנשים שנולדו עם תקלות באנזימים שמוסיפים או מסירים סימן זה לעתים קרובות סובלים מהפרעות נוירו־התפתחותיות המשולבות בפיגור שכלי, אפילפסיה וצמיחה בלתי תקינה של הגוף. עם זאת, לא היה ברור אילו תאי מוח רגישים ביותר להפרעה זו וכיצד התקלקלותם יכולה לקשר בין עירוריות מוחית לתפקוד המטבולי של הגוף כולו.
מיקוד לשני מרכזי מוח קריטיים
החוקרים מהנדסים עכברים שבהם גרסה מוטנטית של חלבון היסטון (H3.3K4M) הופעלה רק בתאים שמקורם בשתי אזורי מוח עובריים: המרכז הגנגליוני המדיאלי, שמייצר רבים מתאי הבלימה האפקטיביים של המוח, וההיפותלמוס המתפתח, שמווסת תיאבון, הורמונים ואיזון אנרגיה. מוטציה זו חוסמת ספציפית את מתילציית H3K4 מבלי להשמיד את ההיסטונים עצמם. בדיקות אישרו שהחלבון המוטנטי נוכח ברבים מהאזורים הממוקדים ושסימני H3K4 התקינים פחתו שם באופן משמעותי בעוד שרמות ההיסטונים הכוללות נשארו יציבות. עיצוב זה מחקה מצבים אנושיים רבים שבהם רק עותק אחד של גן הקשור ל-H3K4 פגום, ולא חסרון מוחלט.
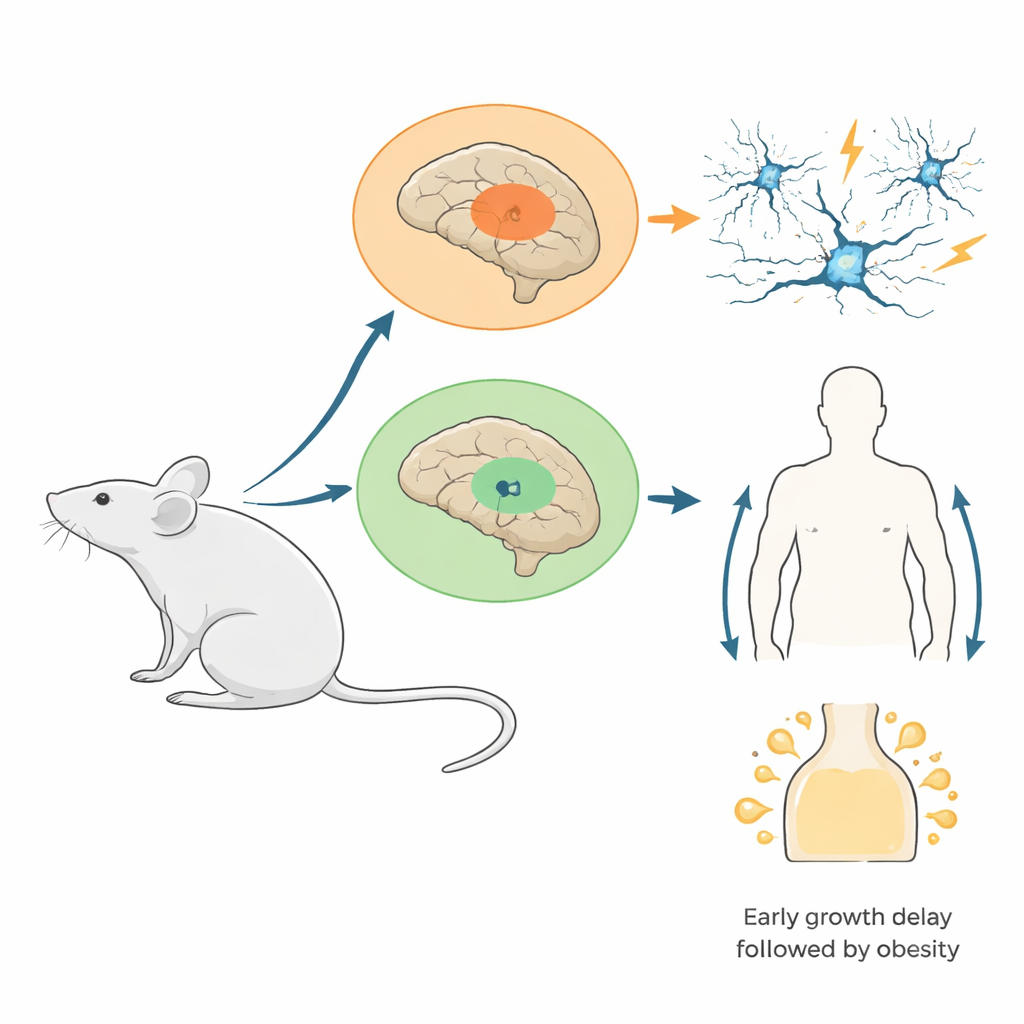
מתאי בלימה חסרים למעגלים רגישים להתקפים
בגדילתם של העכברים נחשפו ההשלכות על מעגלי המוח. במוטנטים הצעירים נרשמה ירידה במספר האינטרנוירונים המעכבים בקורטקס ובהיפוקמפוס, במיוחד בסוג מהיר־ירי שבדרך כלל שומר על תזמון קפדני של קצבי עצב. הקלטות מפורטות הראו שהאינטרנוירונים שנותרו היו נוכחים אך מציגים שונות גדולה יותר בתכונות החשמליות שלהם, מה שמרמז על בגרות מופרעת. כאשר הגירוי להיפוקמפוס בוצע בפרוסות מוח, תנודות תדירות־גבוהה ("גמא")—קצבים חשמליים הקשורים בעיבוד מידע—היו חלשות ואטיות יותר, והופיעו אירועי התפרצויות בלתי תקינות. בחיות חיות, רבים מהמוטנטים, ובפרט נקבות, פיתחו התקפים ספונטניים והיו רגישים בהרבה להתקפים מונעים־תרופתית. בשלב מוקדם של ההתפתחות עקבו החוקרים אחרי אובדן התאים וגילו שהוא נובע בעיקר מהגירה לקויה של אינטרנוירונים אל הקורטקס, ולא ממוות תאי מוגבר או חלוקה תאית מופחתת.
חיווט מחדש של פעילות גנים בתאים מקושרי־התקפים
כדי לקשר את השינויים הפיזיים לשליטה על גנים, הצוות השתמש בריצוף גרעיני־יחיד שקורא הן פעילות גנטית והן נגישות DNA בתאים יחידים. במרכז הגנגליוני המדיאלי העוברי, רוב הגנים שהשתנו במוטנטים היו מושתקים, כולל רגולטורים מפתח שמנווטים תאים לגורל מעכב ספציפי. באינטרנוירונים בוגרים, היחס בין תת־הסוגים השתנה וקבוצות גנים שמעורבות ביצירת קשרים ושליטה בזרמי אשלגן—הזרמים שעוזרים לקבוע מהירות ירי—היו ממווסתות באופן שגוי. ניתוח רשת חשף הפרעה מתואמת בגני תעלות האשלגן שידועים כבר שמשפיעים על אפילפסיה וקצבי מוח, ובכך סיפק קישור מולקולרי ישיר בין אובדן סימן היסטון, שינוי זהות האינטרנוירון ורגישות להתקפים.
חוסר איזון היפותלמי ועקומת גדילה דו־שלבית
ההיפותלמוס סיפר סיפור משלמים שעסק בצמיחת הגוף. כגורי עכברים, המוטנטים היו קטנים וחלק ניכר מהם מת מוקדם. אלה שהישרדו, לעומת זאת, אכלו יותר מאוחר, צברו שומן ופיתחו רמות גבוהות של ההורמון לפטין, מה שמצביע על השמנה ועל חסינות לפרטין. ניתוח תאי־יחיד של ההיפותלמוס העוברי חשף יותר תאים פוריים מתחלקים אך פחות תאים שנועדו לגרעינים מרכזיים הקשורים לאכילה, במיוחד באזורים שמרגישים מצב תזונתי ומווסתים הורמוני גדילה. בהיפותלמוס הבוגר, תמהיל התאים השתנה: האסטרוציטים עלו באופן חד, האוליגודנדרוציטים פחתו, ותאים מיוחדים של מחסום שנקראים טניציטים וגליה שכנה איבדו את הסידור הסדרתי שלהם בממשק שבין המוח להורמונים ולחומרי הזנה בסירקולציה. שינויים מבניים וביטויי גנים אלה סביר שמעוותים כיצד המוח חשה מאגרי אנרגיה ושולטת בתיאבון.
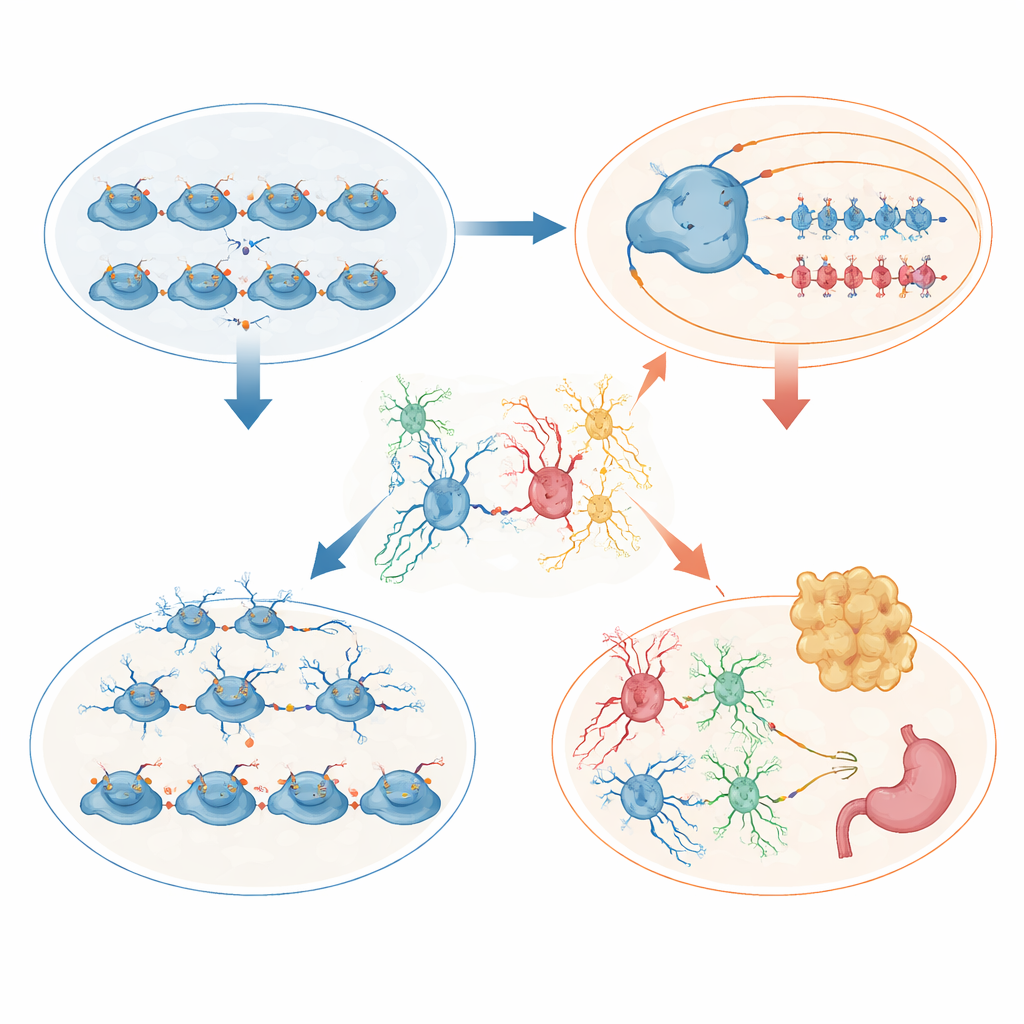
הד יצבי של הפרעות נוירו־התפתחותיות אנושיות
ההתנהגות של העכברים הדהדה תסמינים הנראים בהרבה מצבי נוירו־התפתחות. הם הציגו התנהגויות הדומות לחרדה חזקות יותר, הליכה משונה, ירידה בתנועה הספונטנית בבית וביצועים לקויים במשימות שמבחנות זיכרון, זיהוי חפצים וסינון קולות מפתיעים. במבחנים מסוימים נצפו גם מעשים אימפולסיביים מוגברים. במדידות שונות, נקבות נטו להיות מושפעות קשות יותר מאשר זכרים, מה שמרמז שמערכות הורמונליות ותהליכי ויסות גנים המבדילות לפי מין עשויות באינטראקציה עם סימני היסטון לקבוע פגיעות.
מה משמעות הדבר לבריאות האדם
ביחד הממצאים מראים שהחלשת קבוצה אחת של סימני היסטון בשתי נקודות־מפתח עובריות מספיקה לשחזר קונסטלציה רחבה של בעיות: פחות "בלמים" מעכבים, רשתות מוחיות בלתי יציבות, התקפים, מעגלי אכילה מופרעים וצמיחה גופנית בלתי תקינה. למי שאינו מומחה, המסר המרכזי הוא שסימנים אפיגנטיים כגון מתילציית H3K4 אינם תוספות עמומות אלא דיילים מדויקים שעוזרים לתאי מוח מתפתחים להפוך לסוג הנכון, במקום הנכון, בזמן הנכון. כשהדיילים האלה מכוונים לא נכון, כפי שקורה בהרבה תסמינים גנטיים נדירים, התוצאה יכולה להיות שילוב צמוד של תסמינים קוגניטיביים, התנהגותיים ומטבוליים. הבנת שורשים משותפים אלה עשויה בסופו של דבר לכוון טיפולים שתתקנו לא רק תסמין בודד, כמו התקפים או השמנה, אלא את המערכת המשולבת שמביאה אותם לידי ביטוי.
ציטוט: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
מילות מפתח: אפיגנטיקה, אינטרנוירונים, היפותלמוס, התקפים, השמנת יתר