Clear Sky Science · he
הפרדה בין פאזת ההפרדה לפיבריליזציה שומרת על פעילותם של עיבושים ביומולקולריים
מדוע זה חשוב לבריאות המוח
מחלות מוח רבות, כולל אלצהיימר, מערבות חלבונים שמתקלסים עם הזמן לצברים קשים וסיביים. אותן חלבונים יכולים גם להיווצר למבנים רכים יותר בדמות טיפות בתוך התאים שעוזרות לארגן תגובות כימיות, קצת כמו תחנות עבודה נוזליות זעירות. המחקר שואל שאלה מרכזית: האם ניתן לעצור את ההתקשות המזיקה של טיפות אלו לסיבים מבלי לפגוע בתפקידן היומיומי השימושי? החוקרים מראים שמטבוליט תאי שכיח, חומצת אמינו אל-ארגינין, יכול לעשות בדיוק זאת עבור חלבון מפתח הקשור לאלצהיימר שנקרא טאו.
מחלבון צף לטיפות זעירות
בתוך תאים, חלבונים מסוימים לא תמיד נשארים מפוזרים באופן אחיד בנוזל הפנימי. במקום זאת הם יכולים להתגודד לטיפות, שנקראות עיבושים ביומולקולריים, שמתנהגות כמו ג׳לים רכים מאוד או נוזלים צמיגים. הצוות התרכז בטאו, חלבון שבדרך כלל מסייע בבנייה וייצוב של מיקרוטובולים—סיבים חלולים הפועלים ככבישים בתוך תאי עצב. טאו מזוהה גם ביצירת סיבי עמילואיד קשיחים, הסיבים הנמצאים בצברים שמאפיינים מחלות ניורודגנרטיביות רבות. כדי לחקור כיצד טיפות טאו מתפתחות עם הזמן, החוקרים הנדסו גרסה של החלבון, שכינו אותה SynTag-Tau, שיוצרת עיבושים פעילים שמזדקנים להפיכת עמילואיד בזמן מתאים לניסויים, ללא תוספים קשים.
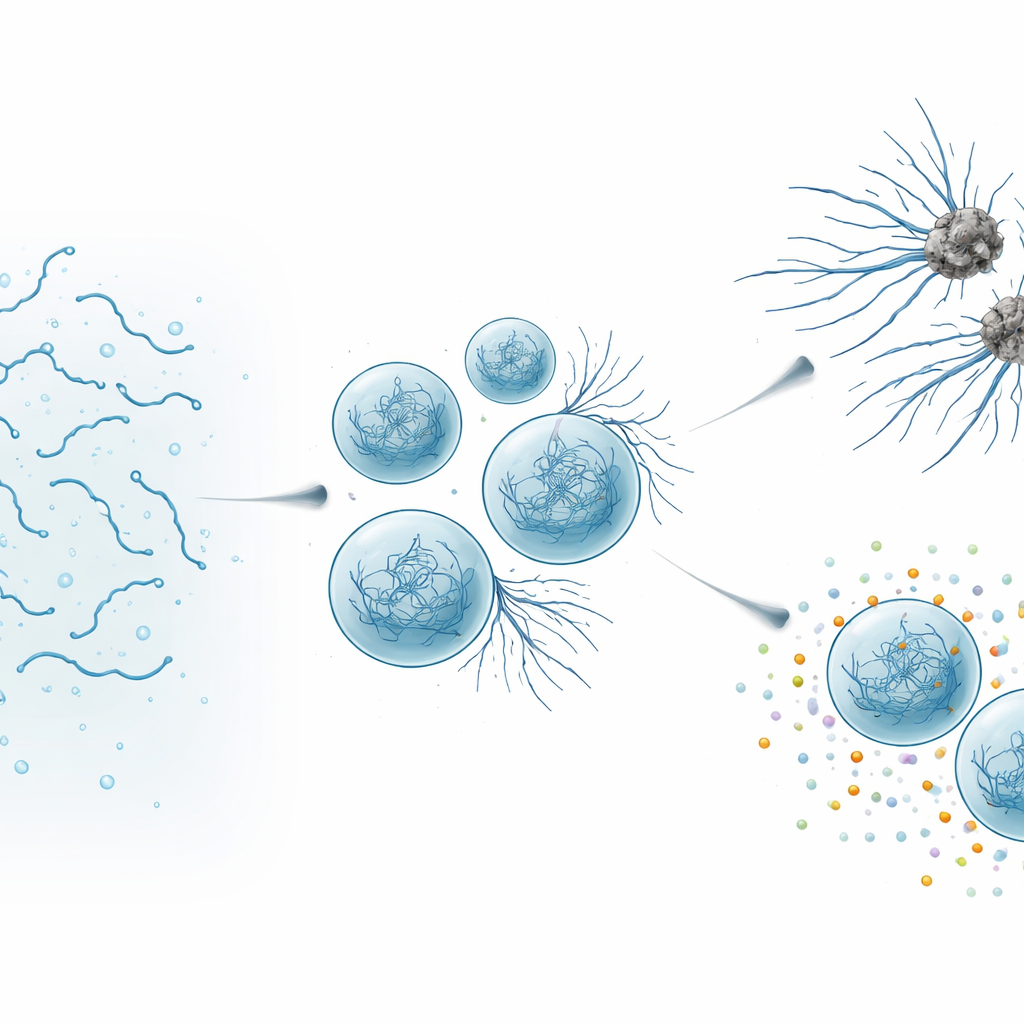
מתי טיפות מועילות הופכות למזיקות
באמצעות מיקרוסקופיה ברזולוציה גבוהה ומדידות ביופיזיקליות, החוקרים צפו בשינוי טיפות SynTag-Tau במהלך שעות. טיפות טריות התנהגו כנוזלים: התאחדו בקלות, מולקולותיהן זזו במהירות ולא היה סימן למבנה מסודר. עם הזמן הטיפות האטו והתקשחו, וסיבים דקים החלו להוציא ניצנים ממשטחיהן אל התמיסה שסביבן. שיטות אופטיות רגישות הראו שסיבים אלה הכילו את ארכיטקטורת "קרוס–בטא" הדחוסה הטיפוסית לעמילואיד. באופן חשוב, הממשק—הגבול בין הטיפה הצפופה לנוזל שמסביב—שימש כתוספת חמה בה הופיעו הסיבים ראשונים. ככל שהטיפות הזדקנו ופרחו סיבים נוספים, תפקודו הרגיל של טאו נפגע: העיבושים הפכו פחות טובים בספיגת טובולין, יחידת הבנייה של מיקרוטובולים, ובסופו של דבר איבדו את יכולתם לתמוך בהרכבת מיקרוטובולים לחלוטין.
מולקולות קטנות שמטות את המאזן
החוקרים שאלו האם מטבוליטים פשוטים יכולים להאט או למנוע את המעבר מנוזל לסיב תוך שמירה על הטיפות עצמן שלמות. בסריקה של כמה מולקולות קטנות שמתרחשות באופן טבעי הם מצאו שחומצות האמינו בעלות המטען החיובי אל-ארגינין ואל-ליזין מעכבות בעוצמה או חוסמות את יצירת סיבי העמילואיד מתוך טיפות SynTag-Tau, ורק אינם מבטלים את היווצרות הטיפות בריכוזים מציאותיים בטווח מילימולרי נמוך. לעומת זאת, חומצות אמינו בעלות מטען שלילי כמו גלוטמט ואספרטט האיצו את יצירת הסיבים, וכימיקלים כלליים שמפריעים לחלבונים או נכשלו בעזרה או שהפריעו אף הם לטיפות. אנלוג פלואורסצנטי של אל-ארגינין הראה שמולקולה זו מעדיפה לשהות בתוך עיבושי טאו ולא מחוצה להם, מה שמרמז שהיא פועלת במקום שבו זקוקים לה ביותר.
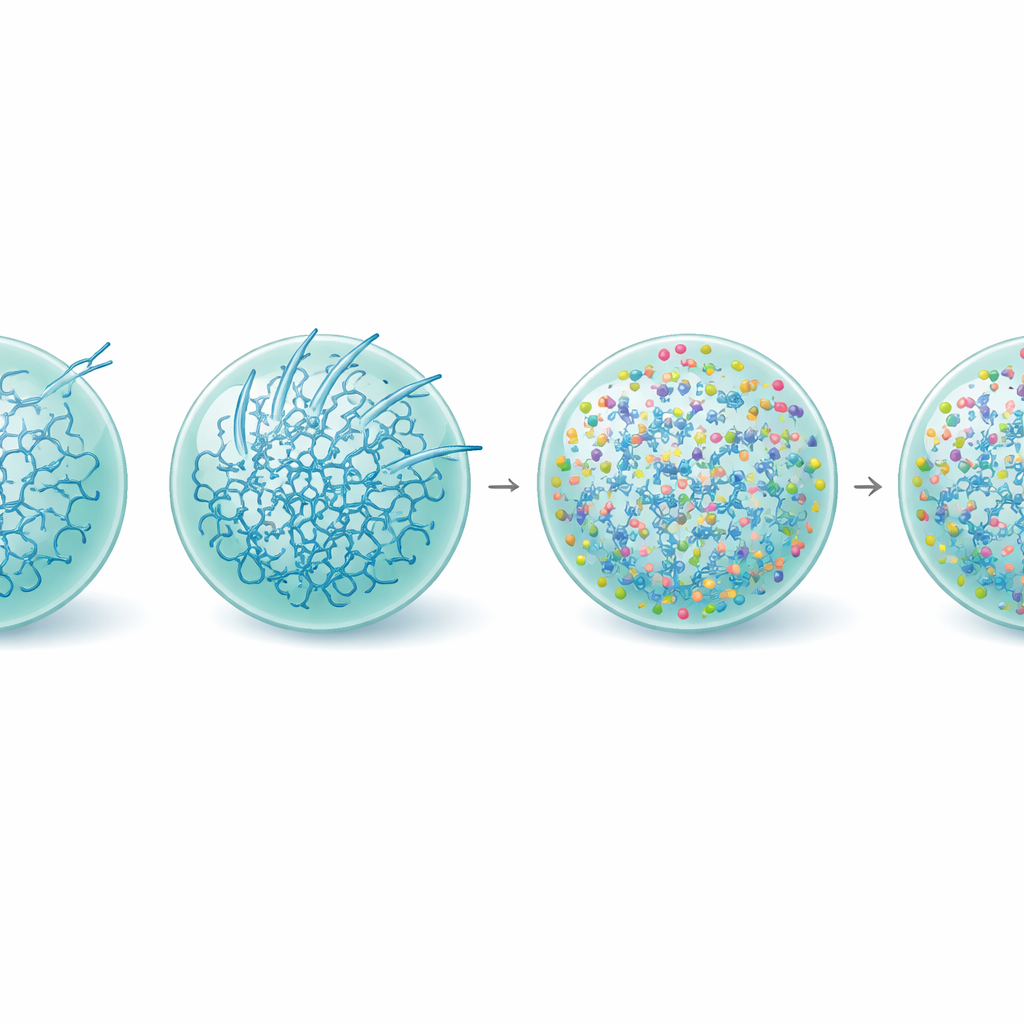
הקשחת הטיפה, הצלת התפקוד
בהעמקה, הצוות בדק כיצד אל-ארגינין מעצב מחדש את חיי הפנים של טיפות טאו. מדידות של מבנה החלבון הראו שבנוכחות אל-ארגינין, החלק של מולקולות טאו שמאמצות צורות בטא עשירות וקשות הקשורות לעמילואיד ירד, אפילו בטיפות ישנות. ננו-ריאולוגיה מבוססת וידאו—מעקב אחרי תנועת חרוזים זעירים בתוך העיבושים—חשפה שאל-ארגינין למעשה עושה את טיפות טאו לוויסקואלסטיות יותר, כלומר הרשת הפנימית שלהן מתחזקה והופכת מקושרת יותר תוך שמירה על אופיין הנוזלי. חיזוק זה נראה כשומר המערכת במצב מטסטבילי ותפקודי, ומעלה את מחסום האנרגיה הנדרש ליצירת סיבים, במיוחד במשטח הטיפה. בהתאם לכך, עיבושים שטופלו באל-ארגינין המשיכו לגייס טובולין באופן אחיד ותמכו בצמיחת מיקרוטובולים הרבה אחרי שטיפות בלתי מטופלות הפכו לא פעילות.
מה משמעות הדבר עבור טיפולים עתידיים
העבודה ממחישה שכוחות שמניעים יצירת טיפות חלבון וכוחות שמניעים יצירת סיבים מזיקים קשורים אך ניתנים להפרדה. באמצעות כיוונון הכימיה בתוך העיבושים בעזרת מטבוליט כמו אל-ארגינין, ניתן לשמר את המצב המועיל הדמוי-נוזל תוך עיכוב או מניעת המעבר לסיבי עמילואיד הקשורים למחלה. למרות שהמחקר משתמש במערכת טאו מהונדסת במיוחד במבחנה, הוא מציע הוכחה עקרונית: מולקולות קטנות שמחזקות בררנית את יציבות העיבושים עשויות יום אחד לעזור להגן על תאים מהצטברות הדרגתית של אגירות חלבון רעילות מבלי לחסום את התפקידים הסדירים והמסדרת של עיבושים ביומולקולריים.
ציטוט: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
מילות מפתח: חלבון טאו, עיבושים ביומולקולריים, סיבי עמילואיד, אל-ארגינין, ניורודגנרציה