Clear Sky Science · he
הבסיס המולקולרי של גלקטוזילציה של קולגן על ידי GLT25D1
איך תגיות סוכר זעירות מסייעות בבניית רקמות חזקות
קולגן הוא החלבון הנפוץ ביותר בגוף, ומהווה את השלד התומך של העור, העצמות, כלי הדם ורקמות רבות אחרות. אבל קולגן לא עובד לבד: יש לקשטו במולקולות סוכר קטנות בנקודות מדויקות כדי להשיג את החוזק והגמישות הנכונים. המחקר הזה חושף, בפרטי אטומים, כיצד אנזים מרכזי אחד, GLT25D1, מצמיד סוכר מסוים לקולגן וכיצד ליקויים בתהליך זה עלולים להוביל לכלי דם שבריריים, בעיות שריר ואולי אפילו לסרטן.
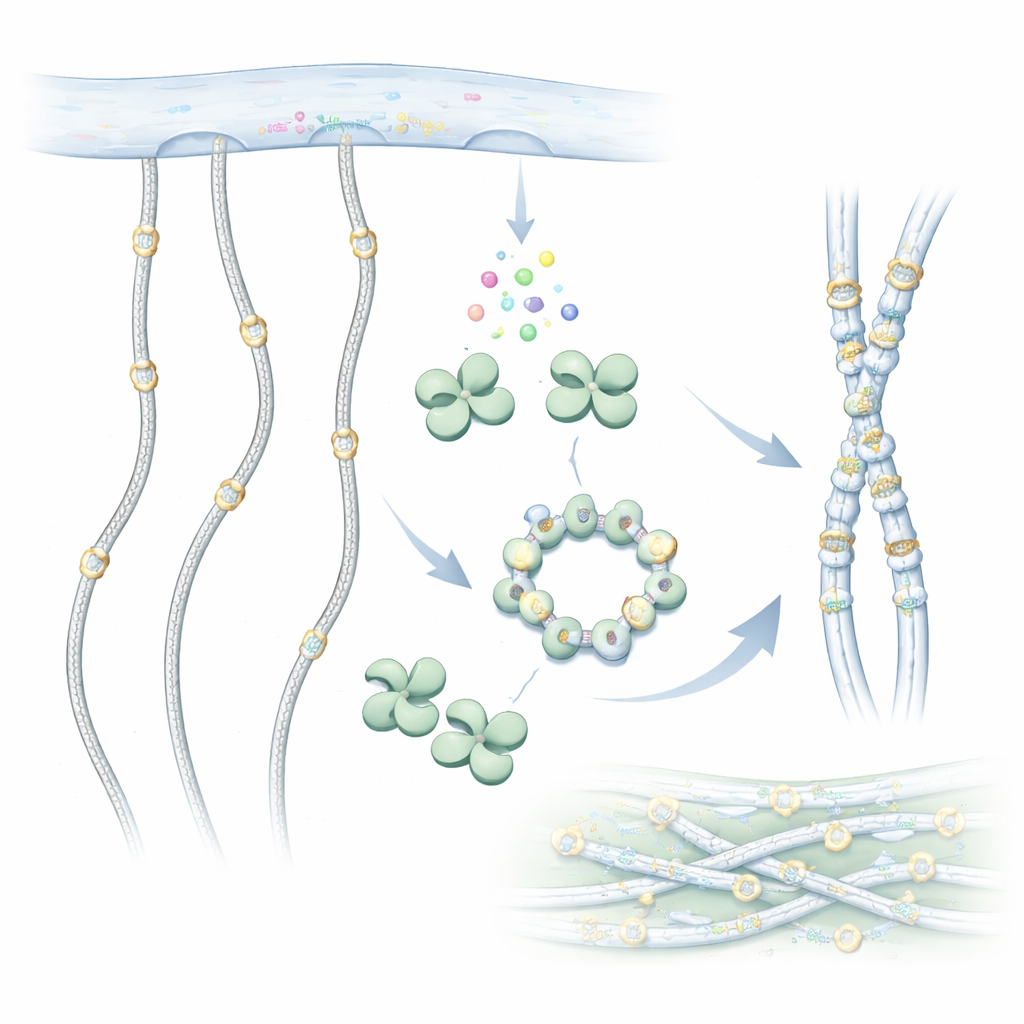
מבט מקרוב על השינוי החבוי של הקולגן
מולקולות קולגן הן שרשראות ארוכות בדמות חבל שמתקבצות לסיבים חזקים מחוץ לתאים. לפני שהן עוזבות את התאים, הן עוברות עריכה כימית. אחת העריכות החשובות היא הוספת קבוצות סוכר לחומרי־הבסיס המיוחדים שנקראים הידרוקסיליזינים לאורך השרשרת. GLT25D1 מבצע את הצעד הראשון בסימון הסוכרים הזה, מעביר סוכר גלקטוז ממולקולת תורם להידרוקסיליזין. קישוט הסוכר הזה שמור מבעלי חיים פשוטים ועד בני אדם ועוזר לקולגן להתקפל נכון, לתקשר עם תאים ולהתנגד לשחיקה.
גילוי צורתו של "המעצב" של הקולגן
כדי להבין איך GLT25D1 פועל, החוקרים השתמשו במיקרוסקופיה אלקטרונית קפואת (cryo‑EM) כדי לדמות את האנזים האנושי ברזולוציה כמעט אטומית. הם גילו שלכל מולקולת GLT25D1 יש שתי אונות דומות, שתיהן שייכות לקיפול אנזים המוכר בחלבוני העברת סוכרים. אונות אלה יוצרים זוגות היוצרים דימרים מוארכים, ושלושה דימרים יכולים להתאסף יחד להקסמר בצורת טבעת. בהרכבים אלה, מרכזי הפעולה — האתרים הקטליטיים — ממוקמים מרחוק זה מזה, פריסה שעשויה לאפשר מספר אתרי הוספת סוכר לפעול לאורך שרשרת קולגן מתוחה בו–זמנית.
החלקים הפועלים: איפה מתרחשת העברת הסוכר באמת
הצוות פתר מבנים של GLT25D1 קשור הן למולקולת התורם הסוכרית והן לפפטיד קצר דמוי קולגן שעובר הידרוקסיליזין. קומפלקס תלת‑גופי זה הראה שרק האונה השנייה, שנקראת תחום C‑קונסטרלי (C‑terminal domain), מבצעת בפועל את הכימיה. שם, מולקולת התורם מתמקמת בכיס שמייצב אותו יון מתכתי, בעוד שהפפטיד שוכב בחריץ צר שמכתיב דפוס מקומי ספציפי: הידרוקסיליזין שאחריו מיד גליצין קטן. שאר אחד מסוג אספרטט פועל כבסיס כימי, מגרה את קבוצת ההידרוקסיל של ההידרוקסיליזין כדי שתוכל לתקוף את הסוכר ולהשלים את ההעברה. שינויים בכל אחד מחומצות האמינו המרכזיות האלה מפחיתים או משביתים לחלוטין את הפעילות, מה שמאשר את תפקידן החיוני.
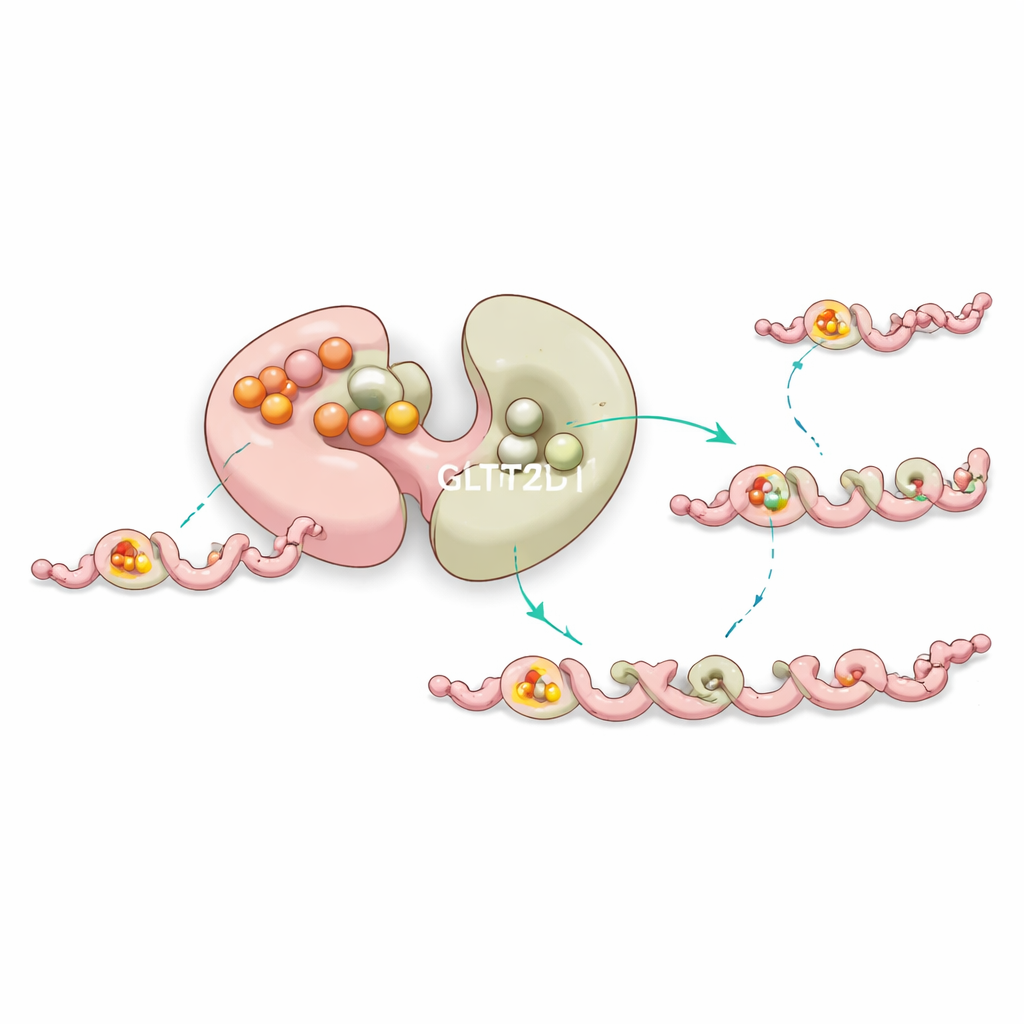
מייצב מובנה ושליטה לטווחים ארוכים
באופן מעניין, האונה הראשונה של GLT25D1 קושרת את מולקולת התורם בצורה הדוקה אך אינה מבצעת את ההעברה. במקום זאת, ניסויים וסימולציות ממוחשבות מצביעים על כך שאתר ה"דומם" הזה מסייע לייצב את האנזים ומכוון בעדינות את התנהגות האונה הפעילה באמצעות תקשורת לטווח ארוך בתוך החלבון. מוטציות בקרבת כיס לא‑קטליטי זה לעתים קרובות מייצבות פחות את החלבון או משנות את היעילות שלו, מה שמרמז שברירה טבעית משתמשת באתר קשירה נוסף זה כסוג של בקרת איכות פנימית כדי לשמור על תיקון הקולגן בצורה חלקה.
כש"המעצב" נכשל: קישורים למחלות
על ידי מיפוי מוטציות שמקורן בחולים על דגם המבנה שלהם, החוקרים יכלו להסביר כיצד שגיאות ב‑GLT25D1 מובילות למחלות אנושיות. כמה מוטציות חותכות את האונה הקטליטית לחלוטין, אחרות מייצבות את הליבה של החלבון בצורה לקויה, ועוד מוטציות פוגעות ישירות באתרים לקשירת הסוכר או לקשירת הקולגן. ליקויים אלה מפחיתים או מבטלים את הוספת הסוכר לקולגן ותקועו בקישור למחלות כלי דם קטנים במוח, לבעיות קוגניטיביות ולפגמים בשריר ובעצמות. מוטציות המקושרות לסרטן גם מרוכזות באזורים קריטיים, מה שמרמז כי קישוט קולגן שונה עשוי להשפיע על גדילה והתפשטות גידולים.
מדוע זה חשוב לבריאות ולטיפולים עתידיים
על‑ידי הצגת תיאור תלת‑ממדי מפורט של GLT25D1 בפעולה, עבודה זו מסבירה כיצד תגיות סוכר מדויקות נוספות לקולגן ולמה שלב זה כה חשוב לשמירת שלמות הרקמות. לקהל רחב, המסר המרכזי הוא ששינויים כימיים זעירים על הקולגן יכולים להיות בעלי השפעות גדולות על כלי דם, עצמות ואפילו על סיכון לסרטן. המפה המבנית של GLT25D1 מציעה כעת מדריך לאבחון וריאנטים מזיקים ולתכנון טיפולים — בין אם מולקולות קטנות שייצבו אנזימים פגומים או אסטרטגיות גנטיות — שעשויים יום אחד לתקן ליקויים בסימון הסוכר של הקולגן במקורם.
ציטוט: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
מילות מפתח: גליקוזילציה של קולגן, GLT25D1, מטה־תאי חוץ־תאי, מחלות כלי דם, מבנה קריו‑EM