Clear Sky Science · he
חוסר סקלווסטין מרגיש תאי שומן לבנים לאותות תרמוגניים שמניעים הופעת שומן בז' (beiging) בעכברים
מדוע חימום השומן עשוי לקרר מחלות
רובנו חושבים על עצם ושומן בגוף כעל שני עולמות נפרדים: האחת מספקת לנו מבנה, והשנייה מאחסנת אנרגיה. המחקר הזה בעכברים מראה שעצם ושומן נמצאים בדיאלוג כימי מתמיד, ושחלבון שמיוצר על ידי תאי עצם יכול להכריע האם השומן ה"לבן" שלנו יישאר באחסון קלוריות או יהפוך לשומן בז' פעיל יותר, המבזבז קלוריות. הבנת הדיאלוג הנסתר הזה עשויה לפתוח דרכים חדשות לטיפול בהשמנה, סוכרת ואובדן עצם בו־זמנית.
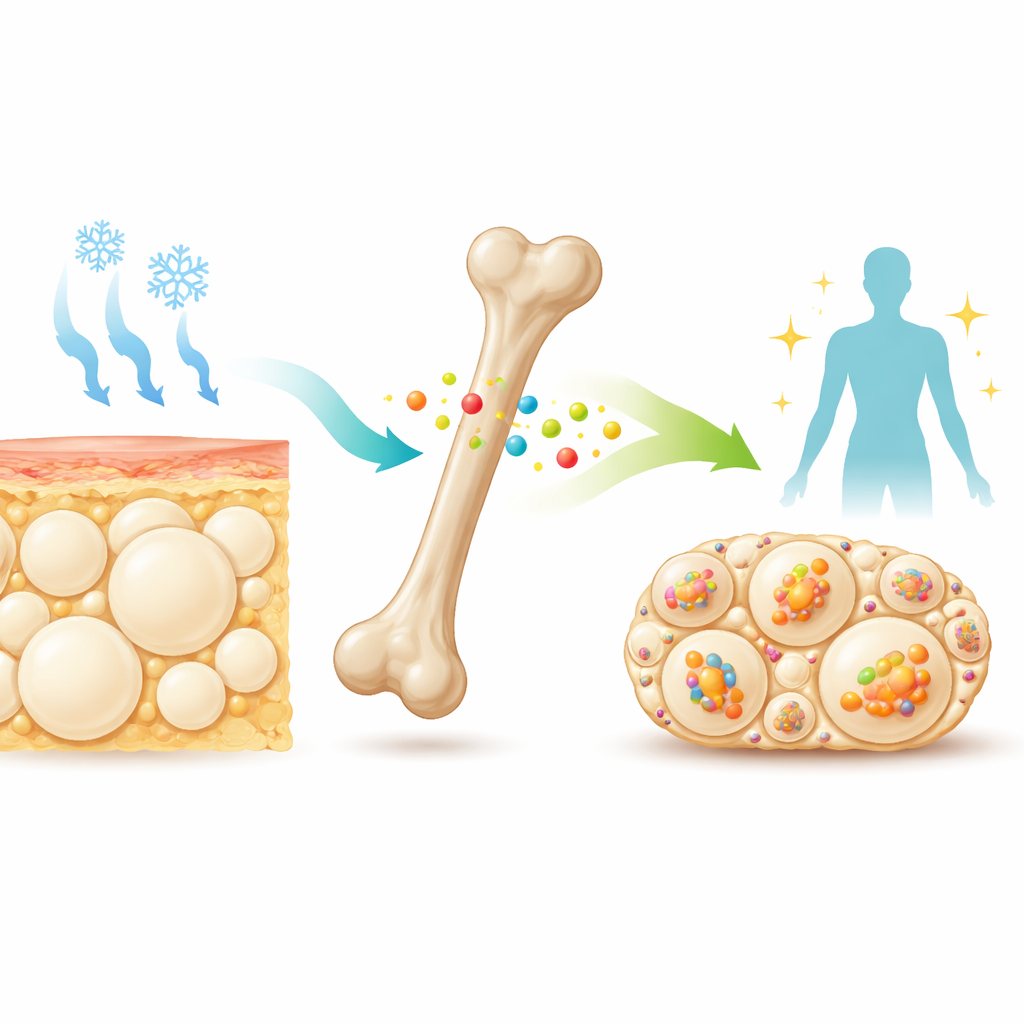
שליח שקט מהעצם
עמוק בתוך העצמות, תאים מיוחדים משחררים לחלבון קטן בשם סקלווסטין לזרם הדם. רופאים כבר מכוונים לסקלווסטין באמצעות תרופות כדי לחזק עצם אצל מטופלים בסיכון לשברים. עבודות קודמות הראו שעכברים חסרי סקלווסטין אינם רק בעלי עצמות חזקות יותר, אלא גם רזים יותר בעלי רגישות טובה יותר לאינסולין. השומן התת‑עורי שלהם, במיוחד סביב הירכיים (שומן לבן אינגווינלי), מכיל תאים זעירים רב‑מחיצתיים המזכירים שומן בז', היכולים לשרוף דלק ליצירת חום. הרמזים האלה הובילו את החוקרים לשאול האם סקלווסטין בדרך כלל פועל כמעצור על יכולת הגוף להמיר שומן לבן לשומן בז' כאשר הוא נחשף לקור או לתרופות המדמות אותות עצביים לשומן.
אותות קור, אותות עצם והצתת השומן
הקבוצה חשפה עכברים מבחינה נורמלית ולעכברים חסרי גן הסקלווסטין (Sost-/-) לתרופה שמפעילה קולטני שומן ספציפיים (קולטן β3‑אדרנרגי), או לקור מתון. בבעלי חיים רגילים, אותות תרמוגניים אלה הגבירו את ייצור הסקלווסטין בעצם והעלו את רמתו בדם. עלייה זו נשענה לאובדן בעצם הספוגי אך רק לשינויים ממוצעים בשומן התת‑עורי. לעומת זאת, בעכברים חסרי סקלווסטין נצפתה תגובה חזקה הרבה יותר: שומן אינגווינלי לקח יותר גלוקוז, שחרר יותר חומצות שומן, צומק בגודל ומלא בתאים דמויי בז' עם מיטוכונדריה רבתית. גנים מפתח לתרמוגנזה הודלקו ביתר עוצמה בעכברים אלה, במיוחד בשומן התת‑עורי, בעוד ששומן חום קלאסי נותר ברובו ללא שינוי.
דיוק שריפת השומן באמצעות מתג משותף
כדי להבין איך סקלווסטין מיישם שליטה זו, החוקרים התרכזו ב‑β‑קטנין, חלבון המעורב במסלול איתות Wnt שאותו סקלווסטין מדכא בדרך כלל בעצם. ברקמת שומן, הפעלת β‑קטנין לאחר הלידה דחפה תאים לבנים לעבר מצב דמוי בז' והגבירה את תגובתם לאותות β3‑אדרנרגיים, אך אפקט זה נעלם כאשר העכברים הוחזקו בטמפרטורת נוחות תרמית חמה שבה הגוף כבר לא זקוק לחום נוסף. באופן הפוך, השמטת β‑קטנין באופן ספציפי בתאי שומן של עכברים חסרי סקלווסטין מחקה את השומן הבז', השיבה תאי שומן לבנים גדולים יותר והפכה שיפורים ברמות אינסולין וחומצות שומן. ניסויים אלה מרמזים שכאשר סקלווסטין נמוך, β‑קטנין בתאי השומן הופך למנוף פנימי חשוב שהופך את השומן הלבן לרגיש יותר לאותות תרמוגניים.
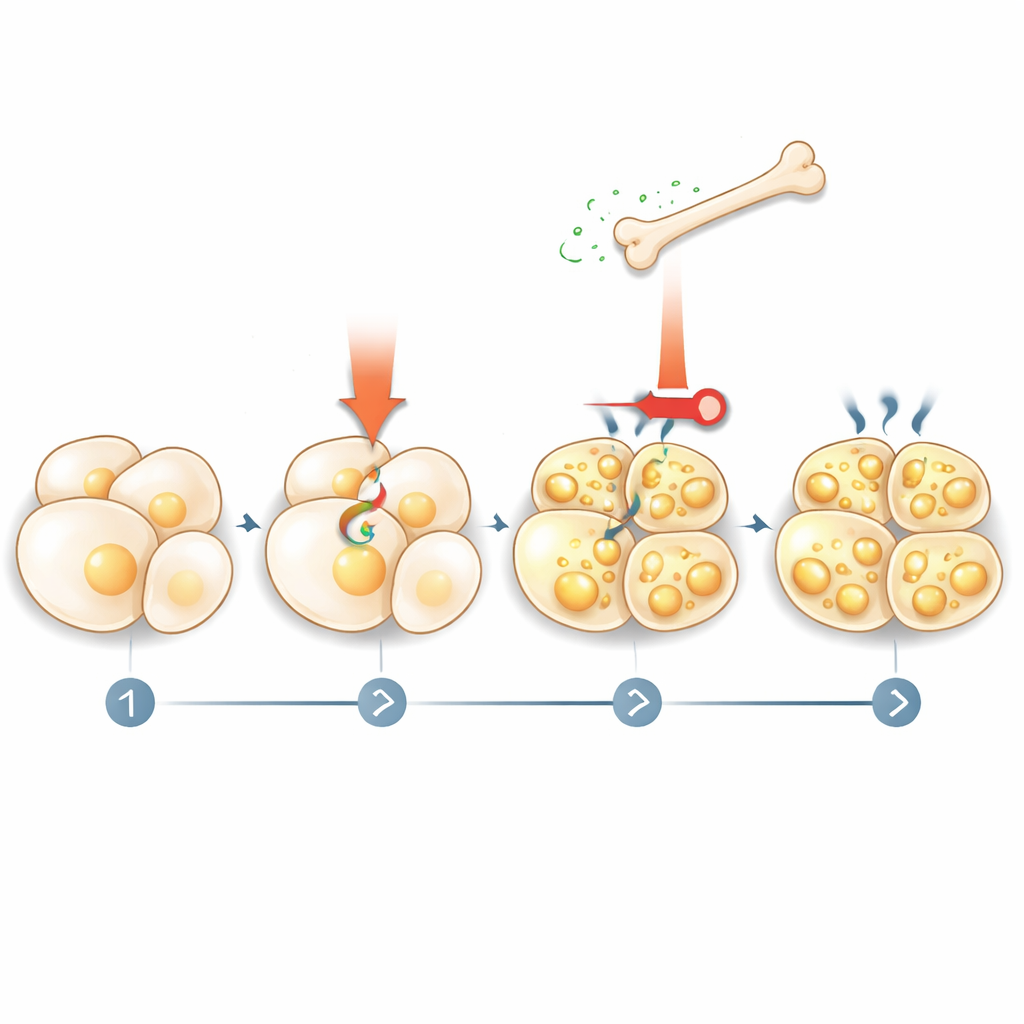
איך השומן משיב לעצם
הסיפור לא הסתיים בכך שהעצם אומרת לשומן מה לעשות. הקבוצה מצאה כי גירוי תרמוגני מפעיל פירוק שומן (ליפוליזה), המשחרר חומצות שומן לדם. חומצות שומן אלה, בתורן, פועלות על תאי עצם דרך קולט גרעיני בשם PPARγ, ומגבירות את ייצור הסקלווסטין. כאשר החוקרים חסמו את הליפוליזה בתאי שומן או הסירו את PPARγ מתאי עצם, תרופות המדמות קור כבר לא יכלו להעלות את רמות הסקלווסטין. הדבר חושף לולאת משוב: אותות תרמוגניים גורמים לשומן לשחרר דלק, הדלק הזה מורה לעצם להפריש יותר סקלווסטין, וסקלווסטין אז חוזר וממעיט את המשך הפעלת השומן וההופעה לבז'.
שילוב תרופות לעצם ולשומן לטובת בריאות מטבולית
לבסוף, החוקרים בדקו האם חריגה בלולאה זו יכולה להועיל בהקשר דמוי מחלה. עכברים שמנים על תזונה עתירת שומן קיבלו מינון נמוך של מיראברגון (תרופה β3‑אדרנרגית הנמצאת כבר בשימוש לבעיות של שלפוחית), נוגדן שנטרל את הסקלווסטין (רומוסוזומאב, מאושר לאוסטיאופורוזיס), או את שניהם. בעוד שכל תרופה לחוד ייצרה אפקטים מתונים, השילוב הקטין את מסת השומן במאגרים מרכזיים, הזיז את השומן לעבר תאים קטנים ופעילים יותר, הוריד אינסולין, טריגליצרידים וכולסטרול, ושמר על חוזק העצם. מחיה בחום, שמפחיתה את הצורך של הגוף בחום, כמעט ומחקה את היתרונות המטבוליים של חוסר סקלווסטין, מה שמדגיש שדרך זו חשובה בעיקר כאשר אותות תרמוגניים נוכחים.
מה המשמעות לטיפולים עתידיים
במילים פשוטות, עבודה זו מראה שעצם אינה רק שלד פסיבי אלא רגולטור פעיל של כמה אנרגיה תאי השומן ישרפו. סקלווסטין מתפקד ככונן עוצמה ששומר על פעילות השומן התרמוגני, ובכך על צריכת הדלק, תחת שליטה. כיבוי הכונן הזה — באמצעות גנטיקה או תרופות — עושה שמאגרים לבנים מסוימים יהיו מוכנים יותר לעבור למצב ייצור חום כאשר הגוף נדחף על ידי קור או תרופות ספציפיות. מאחר שהתערבות דומה יכולה לחזק עצם ולשפר בריאות מטבולית בעכברים, שילובים מתוכננים בקפידה של טיפולים המכוונים לעצם ולשומן עשויים בעתיד לסייע בטיפול בהשמנה, סוכרת ואוסטאופורוזיס יחד, ולא במחלה אחת בכל פעם.
ציטוט: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
מילות מפתח: סקלווסטין, שומן בז' (beige), תקשורת עצם‑שומן, תרמוגנזה, מחלה מטבולית