Clear Sky Science · he
סינתזה מקומית של PI(4,5)P2 על ידי איזופורמים של PIPKIγ המקושרים לספטינים שולטת בקישוריות של centralspindlin אל ה-midbody במהלך הציטוקינזה
איך תאים משלימים את ההיצרפות לשניים
ציטוקינזה — ההצעיקה הסופית שמפצלת תא אחד לשניים — קל לקחת כמובן מאליו, אבל כשהיא מתקלקלת היא עשויה לתרום להתפתחות סרטן ומחלות אחרות. המחקר הזה חושף כיצד קבוצת מולקולות מסוימת מתנהגת כמנהלי בנייה בגשר הצר שמחבר שתי תאים חדשים, ומוודאת שההפרדה תושלם בצורה נקייה במקום שתחזור לאחור או תקפא.
הגשר הסופי בין התאים הבת
לאחר שהתווסף החומר התורשתי והכרומוזומים הופרדו, התא חייב להיפצל פיזית. טבעת כיווצית של סיבים חלבוניים מתכווצת סביב מרכז התא ויוצרת חריץ עמוק הנקרא חריץ הה cleavage. כשהחריץ נמשך פנימה, שני התאים הבת נשארים מקושרים באמצעות גשר בין-תאי דק שמכיל ליבה צפופה, ה-midbody. ה-midbody הוא מבנה זעיר אך מורכב המורכב מצברי מיקרוטובולים, חלבוני תשתית וליפידים מסמנים, והוא פועל גם כעוגן וגם כמרכז בקרה שתואם את הצעדים האחרונים של החלוקה והחיתוך הסופי בין התאים. 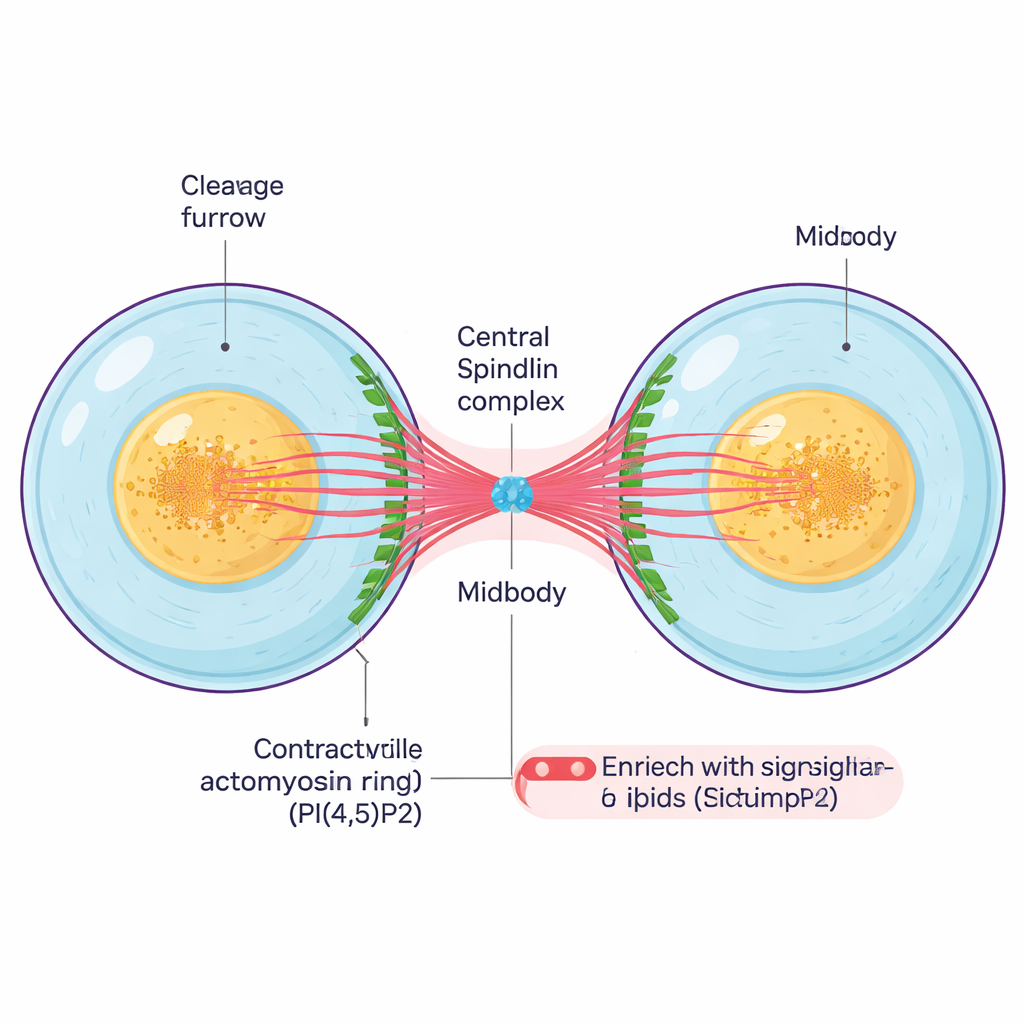
אות ליפידי שצריך להיות במקום הנכון
שחקן מרכזי בתהליך זה הוא מולקולת שומן מסמנת בממברנת התא הנקראת PI(4,5)P2. ליפיד זה מסייע לעגן חלבונים רבים שבונים וכיווצי את הטבעת הכיווצית ומייצבים את הגשר. החידה הייתה כיצד התאים שומרים על המיקום והזמן של הופעת PI(4,5)P2, מכיוון שהיא עלולה להתפזר בממברנה. המחברים התמקדו באנזימים הנקראים קינזות מסוג I PIP, שמייצרות PI(4,5)P2, ובמיוחד בגֵן אחד, PIPKIγ, הקיים בכמה צורות חיתוך־יחסי (splice) עדינות. על ידי הפחתה סלקטיבית של כל קינאז בתאים אנושיים ותצפית בתוצאות באמצעות מיקרוסקופיה מתקדמת, הם מצאו של־PIPKIγ תפקיד מיוחד בשלב המאוחר של הציטוקינזה, כשהגשר וה-midbody נוצרים, אף על פי שהוא אינו משנה משמעותית את רמות ה־PI(4,5)P2 הכוללות על פני הממברנה.
תשתיות ספטין מגייסות אנזים מיוחד
הקבוצה גילתה ששתי גרסאות חיתוך של PIPKIγ, הנקראות i3 ו‑i5, פועלות ככלים מדויקים שמועברים למיקום המתאים על ידי חלבוני מבנה הידועים כספטינים. ספטינים יוצרים סיבים וטבעות שעוזרים לעצב את הגשר ולארגן מרכיבים אחרים. משיכות ביוכמיות ותצפיות תאיות הראו ש‑PIPKIγ‑i3 ו‑PIPKIγ‑i5 נקשרים פיזית לקומפלקסים של ספטינים ומקשטים את סיבי הספטין, בעוד שגרסאות אחרות של PIPKIγ אינן עושות זאת. כשמדענים שינו שני חומצות אמינו ספציפיות בהכנסות החיתוך הללו, האנזימים לא יכלו עוד להיקשר לספטינים. בתאים מתחלקים, PIPKIγ‑i3/i5 תקינים נעים מתבנית ממברנלית מפוזרת לריכוז בחריץ הה cleavage ואז מסמנים את הגשר הבין‑תאי וה‑midbody בקורלציה עם הספטינים וחלבון מבנה נוסף, אנילין. הסרת גרסאות i3 ו‑i5 בלבד הפיצה את אנילין ואת הספטינים הרחק מה‑midbody לאורך הגשר, ורבים מהתאים נכשלו בציטוקינזה, וסיימו עם מספר גרעינים.
ייצור ליפידים מקומי נעוץ במכונת החלוקה
כדי לבדוק האם השפעות אלה תלויות בייצור מקומי של PI(4,5)P2, החוקרים מדדו את ה‑PI(4,5)P2 סביב ה‑midbody ומנעו או הגבירו אנזימים שמוסיפים או מסירים ליפיד זה. דילול של PIPKIγ‑i3/i5 הפחית את ה‑PI(4,5)P2 ב‑midbody, בעוד שחסימת אנזים מפרק PI(4,5)P2 הביאה להשפעה הפוכה. חשוב: השבתת שחזור של איזופורם PIPKIγ חיתוכי פעיל שמקשר לספטין הצילה את הצפיפות הנכונה של אנילין וספטינים על הגשר, בעוד שמוטנטים חסרי קינאז או חסרי קשירת ספטין לא הצילו. בעזרת דימות חיות וטכניקה של מיקרוסקופיית התרחבות שמנפחת פיזית את הדגימה כדי לחשוף פרטים עדינים, הראו שאין‑בו PIPKIγ‑i3/i5, הספטינים מפסיקים לנוע על מיקרוטובולי הגשר, הגשר מתקצר ופחות מקובץ, וקומפלקס קריטי שנקרא centralspindlin נכשל להישאר קשור בחוזקה ל‑midbody. 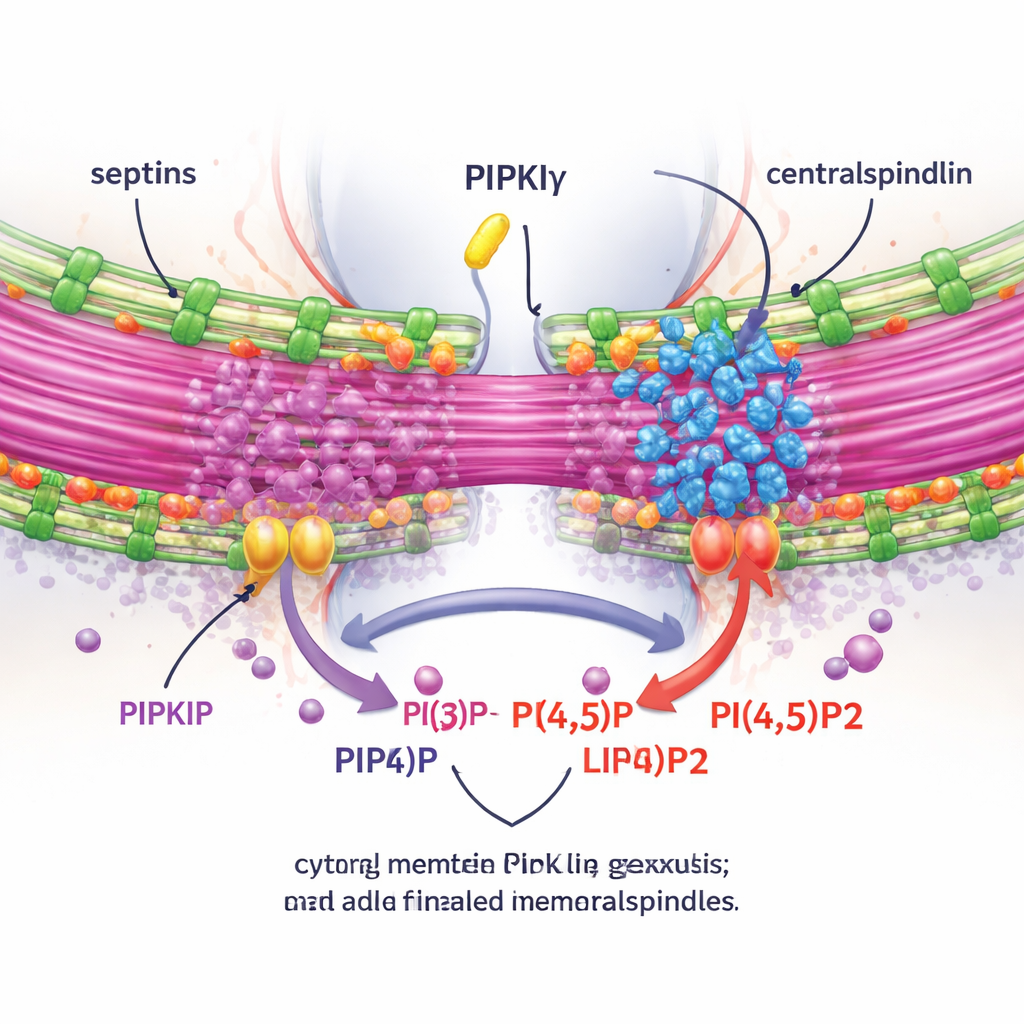
בניית נקודת בקרה לחיתוך נקי
centralspindlin מסייע לקשר בין מיקרוטובולי ה‑midbody לממברנה הסובבת ומווסת מתגי מולקולות קטנים ששולטים בצורת התא. המחקר מראה ש‑centralspindlin קשור הן לספטינים והן ל‑PIPKIγ, ושאיבוד כל אחד מהשותפים מחליש באופן דומה את נוכחותו ב‑midbody. המחברים מציעים שספטינים מגייסים את PIPKIγ‑i3/i5 לחריץ שנכנס פנימה, שם אנזימים אלה יוצרים כתם מרוכז של PI(4,5)P2. מאגר ליפידי מקומי זה, בתורו, מייצב את אנילין, את centralspindlin ואת הספטינים בסמוך ל‑midbody, מקדם את קיבוץ וייצוב מיקרוטובולי הגשר, ומאפשר לגשר הבין‑תאי להבשיל עד שמתבצע החיתוך הסופי של האברציה. כאשר מערכת זו מופרעת, PI(4,5)P2 מופיע במקום הלא נכון, חלבוני התשתית מתפזרים, המיקרוטובולים אינם מקובצים כראוי, וציטוקינזה לעתים קרובות נכשלת.
מדוע זה חשוב מעבר לביולוגיה תאית בסיסית
על‑ידי זיהוי כיצד איזופורמים חיתוכיים ספציפיים של PIPKIγ וספטינים משתפים פעולה כדי לייצר אות ליפידי מקומי ב‑midbody, עבודה זו מסבירה כיצד תאים מעניקים דיוק מרחבי למולקולה מסמנת בעלת תנועה גבוהה. דיוק זה קריטי להשלמת חלוקת התא בבטחה, ועוזר למנוע חלוקה לקויה של כרומוזומים ומספרי תאים חריגים שעשויים לקדם התפתחות גידולים. מבני ה‑midbody עצמם משפיעים גם על גורל התאים ועל הפרוליפרציה לאחר החלוקה, ולכן הבנת האופן שבו הם מורכבים פותחת דרכים חדשות לחקור כיצד שגיאות בתשתיות הננומטריות הללו עשויות לתרום לסרטן ואפשרות של מניפולציה של תאים גזעיים.
ציטוט: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
מילות מפתח: חלוקת תא, ציטוקינזה, ליפידים מסמנים, ספטינים, ביולוגיה של סרטן