Clear Sky Science · he
מעכב פנ-RAF אקזאראפניב מכוון לסרטן ריאה מסוג BRAF כיתות II/III וחושף עמידות ARAF-KSR1 ואסטרטגיות שילוב
מדוע המחקר הזה חשוב לחולי סרטן ריאה
רוב האנשים שמעו על תרופות ממוקדות שמטפלות בשינויים גנטיים ספציפיים. אך עבור מטופלים רבים עם סרטן ריאה, ובפרט אלה שלגידולים שלהם יש מוטציות פחות נפוצות בגן בשם BRAF, התרופות הממוקדות הקיימות כיום פשוט לא עושות את העבודה. מחקר זה מציג תרופה ניסיונית חדשה, אקזאראפניב, שנועדה לפגוע בטווח רחב יותר של גידולי BRAF ומסביר כיצד תאי הסרטן מנסים להימלט ממנה — ובכך חושף טיפולים משולבים שעשויים לשמור על שליטה בגידולים אלה למשך זמן ארוך יותר.
רוב מוסתר של מוטציות מוזנחות
החוקרים התחילו בשאלה בסיסית: כמה נפוצות סוגי המוטציות השונות ב‑BRAF בסרטן מתקדם, ובמיוחד בסרטן ריאה שאינו קטן תאים (NSCLC)? באמצעות מאגר גדול של בדיקות ביופסיית נוזל (liquid biopsy) שכלל מעל 160,000 מטופלים, הם ניתחו רסיסי DNA של הגידול הנמצאים במחזור הדם. הם מצאו שבסרטן ריאה מוטציות ב‑BRAF מופיעות בכ‑4–5% מהמטופלים, מספר שמתרגם לאלפי אנשים ברחבי העולם. באופן מהותי, כ‑שני שלישים מהגידולים הריאתיים הללו נשאו את מה שמכונה מוטציות BRAF כיתה II וכיתה III — סוגים שתרופות BRAF מאושרות כיום אינן מכוונות אליהם ביעילות. מטופלים עם אחת מהכיתות האלה, ובפרט כיתה II, נטו לשרוד זמן קצר יותר מאשר אלה עם המוטציה המוכרת ככיתה I, ככל הנראה מפני שמטופלי כיתה I נהנים מגישות טיפול ממוקדות מבוססות בעוד שמטופלי כיתה II/III מקבלים בדרך כלל כימותרפיה סטנדרטית או אימונותרפיה.
תרופה דור‑הבא שמכוונת את כל המסלול
BRAF הוא חלק מרצף חלבונים (נתיב MAPK) שמעביר אותות גדילה מממברנת התא אל הגרעין. תרופות BRAF רבות שפיתחו עד כה עוצבו לחסום רק צורה מוטנטית אחת ולעתים אף עלולות לגרום להמרצה של חלבונים קשורים בתאים תקינים. אקזאראפניב עוצב אחרת: הוא מעכב "פנ‑RAF" שנועד לכבות כמה מחברי משפחת RAF (ARAF, BRAF ו‑CRAF) בצורות יחיד וזוגיות, תוך שמירה על מרבית האנזימים התאית האחרים. בבדיקות ביוכימיות שנערכו מול מאות קינאזות אנושיות, אקזאראפניב חסם בעוצמה את שלושת חלבוני ה‑RAF אך גרם למעט השפעות מחוץ‑מטרה, מה שמרמז על פרופיל בטיחות נקי יותר ביחס לתרכובות פנ‑RAF מוקדמות.
השפעות עוצמתיות במודלים של גידולים קשים לטיפול
הצוות בחן את אקזאראפניב בסדרה של שורות תאים ובמודלים עכבריים שנושאים מוטציות שונות ב‑BRAF וב‑RAS, כולל גידולים שמקורם בחולים. בתרביות התאים, אקזאראפניב האט גדילה וכיבה את איתותי MAPK לא רק בתאים עם BRAF V600E הקלאסי אלא גם באלה עם מוטציות כיתה II וכיתה III וברבים מהתאים המוטנטיים ב‑RAS שלרוב חסרות אפשרויות ממוקדות טובות. בעכברים שנושאו גידולי ריאה עם השינויים הללו, אקזאראפניב הקטין או האט את הגידולים במידה תלויה מינון והדגים קשרים ברורים בין רמות התרופה, דיכוי הנתיב ותשובת הגידול. נתונים קליניים מוקדמים משני חולים עם סרטן ריאה מתקדם מוטנטי BRAF — אחד עם פיוז'ן נדיר של BRAF ואחר עם מוטציית נקודה כיתה II — הראו תגובות חלקיות והקלה משמעותית בסימפטומים, ותמכו ברלבנטיות של העבודה הפרה‑קלינית.
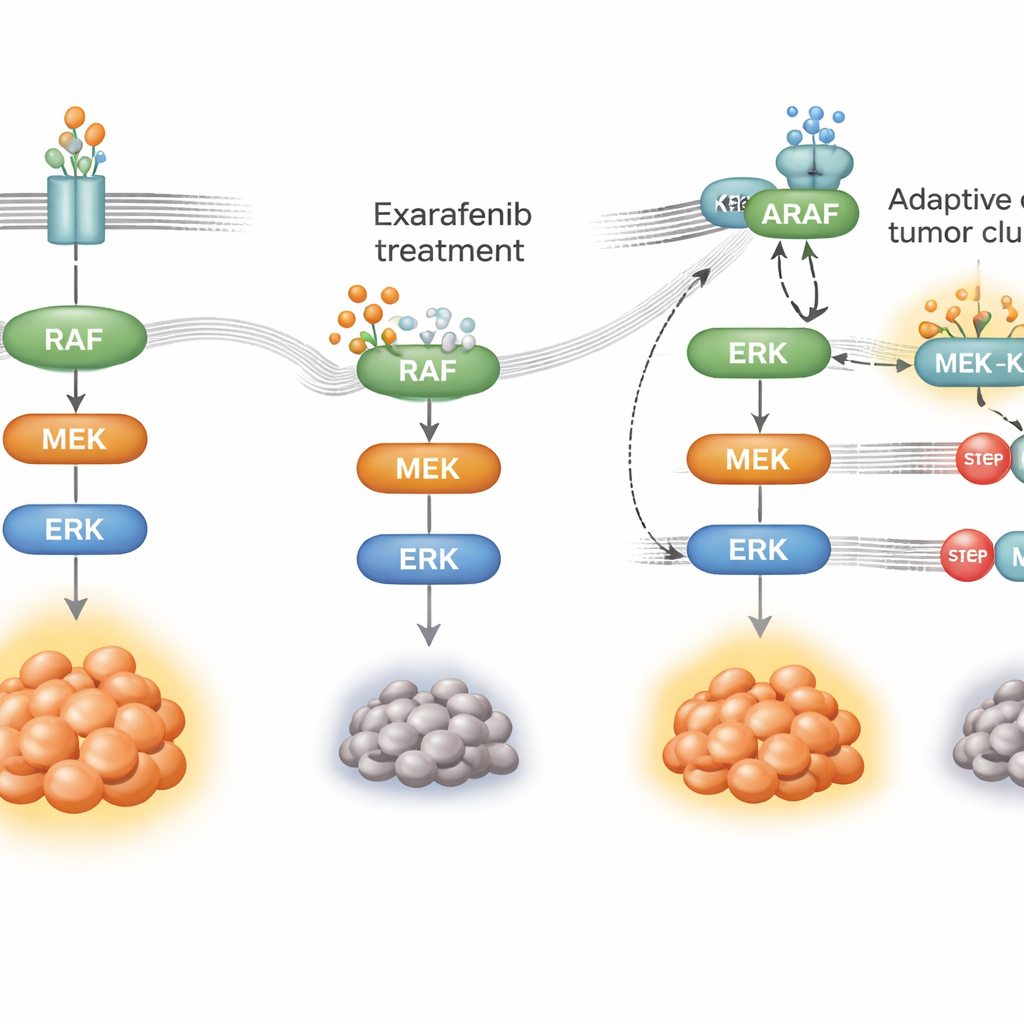
כיצד הסרטן לומד לעקוף את התרופה
אין טיפול ממוקד שפועל לנצח; תאי הסרטן מתאימים עצמם. כדי לבדוק כיצד גידולים עלולים לפתח עמידות לאקזאראפניב, החשיפו החוקרים תאים של סרטן ריאה מוטנטי BRAF לתרופה למשך חודשים עד שצמחו אוכלוסיות עמידות. תאים אלה עדיין היו תלויים באותו מסלול גדילה אך חיברו אותו מחדש. במקום להסתמך בעיקר על BRAF המוטנטי, הם הגדילו את פעילות מתג על־זרם בשם RAS ומנעו לשימוש בחבר משפחה אחר, ARAF, יחד עם חלבון מעגן בשם KSR1. תחת לחץ התרופתי, ARAF ו‑KSR1 יצרו קומפלקסים הדוקים שעזרו לשמור על המשדר MAPK פועל גם כאשר אקזאראפניב היה קשור. כאשר המדענים השתקו באופן סלקטיבי את ARAF או את KSR1, או הפחיתו את פעילות RAS, התאים העמידים חזרו להיות רגישים לאקזאראפניב והאותות התומכים בהישרדות התמוטטו.
אסטרטגיות שילוב כדי להקדים את העמידות
מצוידים במפה מנגנונית זו, החיפוש אחר תרופות שותפות שנתקעות בצווארי בקבוק משותפים לנתיב המקורי ולאפשרות העקיפה הוליד תוצאות מבטיחות. נמצא ששילוב אקזאראפניב עם מעכבי MEK או ERK — שלבים מרכזיים מטה בנתיב MAPK — הניב סינרגיה חזקה במגוון דגמי תאים ועכבר, כולל גידולים שהיו פחות רגישים מלכתחילה או שפיתחו עמידות. שילובים אלה שמרו על הנתיב כבוי למשך זמן רב יותר, עוררו יותר מוות תאי ובחיות לעתים עבדו כיעילים או יעילים יותר ממינונים גבוהים של אקזאראפניב לבדו, ללא רעילות נראית נוספת. גם סוכנים המכוונים ישירות ל‑RAS שיפרו את השפעת אקזאראפניב במודלים שבהם RAS הנהיגה בבירור את העמידות, מה שמציע טקטיקה קלינית נוספת בעלת פוטנציאל.
מה המשמעות עבור המטופלים
לאנשים עם NSCLC שנושאים מוטציות BRAF כיתה II או כיתה III — או פיוז'נים מורכבים של BRAF ומוטציות משולבות ב‑RAS — אין כיום טיפולים ממוקדים מאושרים, ותוצאותיהם חלשות יחסית לעומת מטופלים עם שינויים שכיחים יותר. המחקר נותן טיעון מדעי חזק שאקזאראפניב עשוי למלא פער זה על‑ידי כיבוי רחב של איתותים מונעי RAF. הוא גם מסביר כיצד גידולים עלולים להסתגל באמצעות מעקף ARAF‑KSR1 ומראה כי תקיפת הנתיב במספר רמות, ובפרט באמצעות שילוב מעכבי RAF ו‑MEK או הוספת מעכבי RAS, עשויה להעניק שליטה עמוקה וברת‑קיימא יותר על הגידול. יחד, התובנות האלה מציירות דרך לניסויים קליניים שמטרתם להביא טיפולים ממוקדים משולבים, מותאמים לקבוצה גדולה וקודם לכן מוזנחת של חולי סרטן ריאה.
ציטוט: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
מילות מפתח: סרטן ריאה מוטant BRAF, מעכב פנ‑RAF, אותות MAPK, עמידות לתרופות, שילובי טיפולים ממוקדים