Clear Sky Science · he
הנדסה מטבולית של ביוסינתזת דוקסורובצין דרך אופטימיזציה של שותפי רדוקס P450 וניתוח מבני של DoxA
מדוע סיפור המקור של תרופת־סרטן חשוב
דוקסורובצין הוא אחד מהתרופות המרכזיות בכימותרפיה המודרנית, המשמש לטיפול בסרטן מדלקתיות עד גידולי שד. למרות שימוש במשך עשורים, הדרך שבה אנו מייצרים את התרופה מפתיעה בנסיוביותה: תעשייה בדרך כלל בונה אותה מתוך תרכובת קרובה במקום לאפשר למיקרוב הטבעי להשלים את התהליך. המחקר הזה חושף מדוע החיידק המייצר מתקשה להשלים את הצעדים הכימיים האחרונים ומראה כיצד הנדסה מחודשת של המכאניזם הפנימי שלו יכולה להגביר באופן חדה את הייצור של דוקסורובצין בשלמותו, מה שפותח את הדלת לאספקה אמינה וזולה יותר פוטנציאלית.
מחיידקי אדמה לתרופה שמצילה חיים
דוקסורובצין שייך למשפחת האנטראשיקלינים, קבוצת מולקולות טבעיות הנבנות על ידי חיידקי אדמה מהסוג Streptomyces. תרכובות אלה חולקות שלד פחמני קשיח ושטוח שנכנס בין בסיסי ה‑DNA, ובנוסף יחידת סוכר שמתחבאת בתוך החריצים של ה‑DNA. יחד, התכונות האלה חוסמות את המכאניזם המטפל ב‑DNA בתא ומובילות בסופו של דבר למוות תאי — דבר שימושי נגד תאים סרטניים המתרבים במהירות. המייצר הקלאסי, Streptomyces peucetius, מייצר באופן טבעי בעיקר פרהקורסור בשם דאונורובצין, ורק כמות צנועה של הדוקסורובצין היעיל יותר, ששונה רק בקבוצת חמצן נוספת אחת. שינוי מבני זעיר זה משפר באופן דרמטי את הפעילות אך מתגלה כקשה במיוחד להשגה ביעילות על ידי המיקרוב.
למצוא את החיווט החשמלי הנכון בתוך התא
האנזים הקריטי המבצע את שלושת צעדיו האחרונים של החמצון על שלד התרופה נקרא DoxA, חבר במשפחת ציטוכרום P450. כמו מפעל כימי זעיר, DoxA זקוק לזרם יציב של אלקטרונים על מנת להפעיל חמצן ולהתקין אטומי חמצן חדשים על מולקולת התרופה. בתוך החיידק, האלקטרונים מסופקים דרך רצף חלבונים מסייעים הידועים כשותפי רדוקס. הגנום של S. peucetius מכיל מספר מועמדים, מה שהופך את זה ללא ברור אילו מהם באמת משתפים פעולה עם DoxA. על‑ידי השוואת פעילות גנים ומטבוליזם בזן רגיל, מוטנט העשיר בדאונורובצין ומוטנט העשיר בדוקסורובצין, החוקרים זיהו פרדוקסין אחד (Fdx4) ופרדוקסין רדוקטאז אחד (FdR3) כשותפים הטבעיים. בנייה מחדש של השלישייה הזו בתגובות בניסויי מעבדה אישרה כי DoxA פועל בצורה מיטבית כאשר הוא מחובר לשרשרת העברת האלקטרונים הספציפית הזו, בדומה להתאמת מתאם כוח נכון למכשיר.
שחרור האטת העצמית של האנזים
אפילו עם החיווט החשמלי הנכון, DoxA נוטה להיתקע בשלב האחרון שממיר דאונורובצין לדוקסורובצין. עבודות קודמות רמזו כי המוצר עצמו עלול לסתום את האנזים. הצוות פנה לגֵן שכונבי קרוב, dnrV, שתפקידו היה חידתי. בדיקות ביוכימיות הראו כי חלבון DnrV נקשר בחוזקה למגוון מולקולות אנטראשיקלין, כולל דוקסורובצין, מבלי לשנותן כימית. הוספת DnrV לתגובות DoxA שיפרה מאוד את זרימת התגובות הכימיות, ואיפשרה המרה מלאה של הפרה‑קורסורים לתרופה הסופית תוך הימנעות מתגובות צד הרסניות. במונחים מעשיים, DnrV פועל כמו ספוג פנימי הסופג דוקסורובצין שזה עתה נוצר, ומונע ממנו לסתום את האנזים או לפגוע ב‑DNA בתוך התא המייצר.
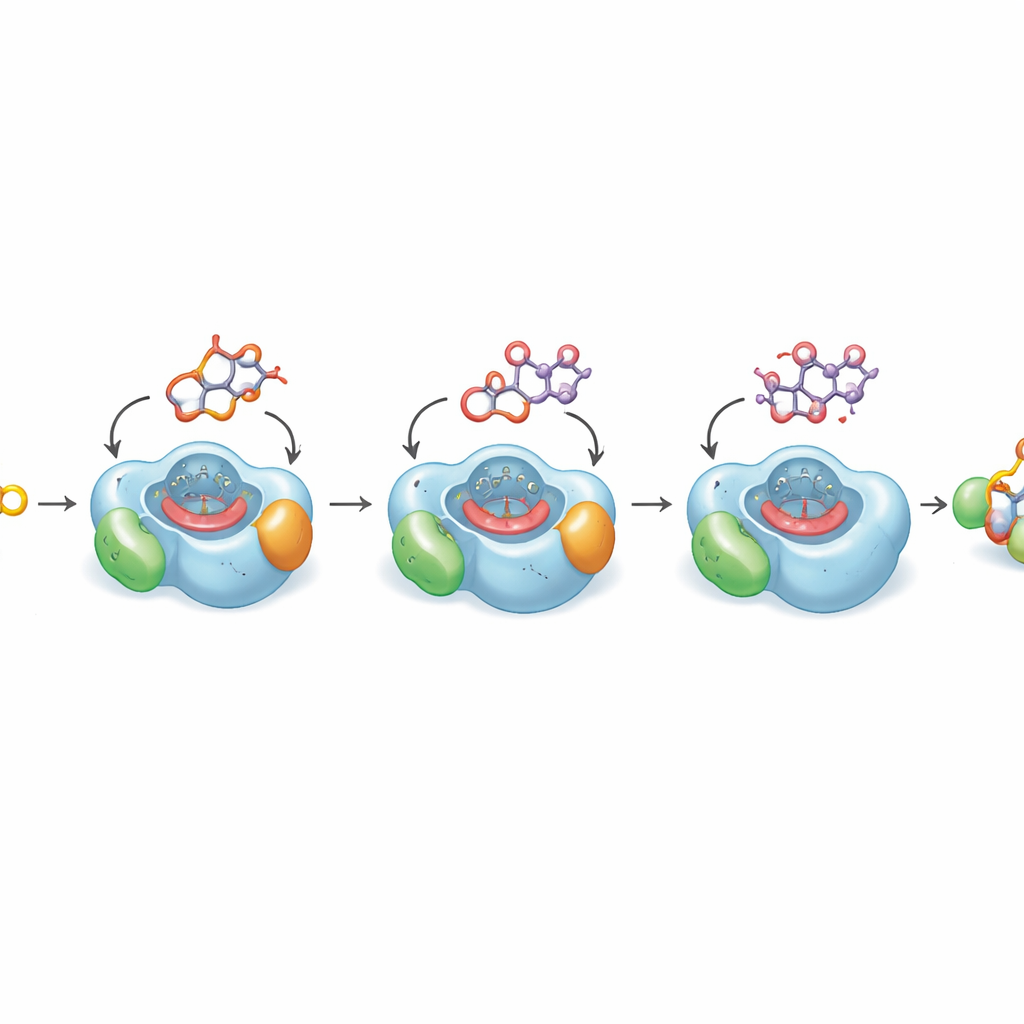
לראות מדוע השלב האחרון כה איטי
כדי להבין מדוע חמצון המפתח האחרון הוא איטי מטבעו, המחברים פיענחו מבני גביש ברזולוציה גבוהה של DoxA קשור לשלושה אינטרמדיייטים עוקבים. מבנים אלה חושפים כיצד הליבת התרופה השטוחה והסוכר המוצמד משתבצים בתוך כיס הדוק מעל קבוצת ההים של האנזים, מרכז המתכת הריאקטיבי המבצע את החמצון. בשלבים המוקדמים, האטום בפחמן שיש לשנות נמצא קרוב להים במיקום אידיאלי לתגובה. אך בתת‑המסובב האחרון, דאונורובצין, החלק במולקולה שיש להידרוקסיל נטה הרחק מההים לתוך חלל קטן ושמנוני, סידור שלפי חישובי קוונטים מועדף אנרגטית. סימולציות מחשב על קנה‑מידת זמן מיקרו‑שניות מאשרות כי המולקולה רק מזדקנת מדי פעם לפוזה פרודוקטיבית עבור הכנסת החמצן האחרונה. הטיה מבנית זו מסבירה מדוע ההמרה לדוקסורובצין אינה יעילה מטבעה.
בניית זן משופר לייצור דוקסורובצין
מצוידים בתובנות אלה, החוקרים עיצבו מחדש את החיידק באופן רציונלי במקום להסתמך על מוטגנזה אקראית. הם הכניסו גן לתיקון DNA לייצוב הייצור, ואז התקינו עותקים נוספים של doxA, שותפי הרדוקס האופטימליים fdx4 ו‑fdr3, וחלבון הקשירה המסייע dnrV תחת מובילים שנבחרו בקפידה כדי לאזן את רמותיהם. הם גם כווננו את תנאי הגידול והשתמשו ברזינים מיוחדים לספיחת אינטרמדיייטים רעילים ודביקים. בבקבוקיות מעבדה ובביו‑רטור בנפח 20 ליטר, הזן המהונדס הטוב ביותר ייצר 336 מיליליטוגרם דוקסורובצין לליטר תרבית עם יחס של 81:19 של דוקסורובצין לדאונורובצין — עלייה של כ‑180% בהשוואה לזן ההתחלתי ותערובת מוצר נקייה בהרבה.
מה משמעות הדבר לאספקת תרופות סרטן בעתיד
על‑ידי פירוק הן של מערכת התמיכה החשמלית והן של המבנה התלת‑ממדי של אנזים מרכזי, עבודה זו מסבירה מדוע מיקרוב רפואי חשוב מגלה ביצועים חלשים בייצור האנטראשיקלין הנחשק ביותר שלנו. התאמת DoxA לשותפי הרדוקס הטבעיים שלו, הוספת חלבון מסייע קושר תרופה, ואיזון מחדש של ביטוי הגנים הפכו מייצר מרוכז למייצר חזק. בעוד שכוונון נוסף של האנזים עשוי להאיץ עוד יותר את השלב הכימי האחרון, המחקר כבר מקרב את הייצור הביולוגי המלא של דוקסורובצין למציאות תעשייתית. עבור מטופלים ומערכות בריאות, התקדמות כזו עשויה להתבטא בגישה בטוחה יותר, מדרגית וחסכונית יותר לתרופה בסיסית בכימותרפיה.
ציטוט: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
מילות מפתח: ייצור דוקסורובצין, ביוסינתזה של אנטראשיקלינים, הנדסת אנזימים, ייצור תרופות חיידקי, ציטוכרום P450