Clear Sky Science · he
מנגנון משאבת Na+ המונעת על‑ידי רדוקציה ב‑NADH‑קוינון אוקסידורדוקטאז של Vibrio cholerae נשען על שינויים קונפורמציוניים דינמיים
איך תחנת הכוח של הכולרה הפכה למטרה לתרופות
החיידק שגורם הכולרה, Vibrio cholerae, שורד ומתרבה על‑ידי הפעלת תחנת כוח מולקולרית זעירה בממברנת התא שלו. המחקר הזה חושף, בפרטים חסרי תקדים, כיצד אחד המנועים המרכזיים שלו — אנזים בשם Na⁺‑NQR — משנה את צורתו בזמן שהוא משאבת כיפות נתרן מחוץ לתא. הבנת המנגנון המולקולרי אינה מספקת רק סקרנות בסיסית לגבי האופן שבו החיים ממירים מזון לאנרגיה זמינה, אלא גם מצביעה על דרכים חדשות לעצב אנטיביוטיקה שמפסיקה חיידקים מזיקים מבלי לפגוע בתאים האנושיים.
מנוע מונע בנתרן בחיידקים
חיידקים ימיים ורבים מהחיידקים הפתוגניים תלויים ב‑Na⁺‑NQR כצעד הראשון בשרשרת הנשימה שלהם — סדרת התגובות המוציא אנרגיה מהמזון. Na⁺‑NQR יושב בממברנה הפנימית ולקוח אלקטרונים ממולקולת דלק הנקראת NADH, ומעביר אותם לאורך שרשרת של מולקולות סייע (קופקטורים) צבועות אל הקוינון, מולקולה קטנה נוספת המוטמעת בממברנה. כשזרימת האלקטרונים מתרחשת, האנזים משתמש באנרגיה זו כדי לדחוף יוני נתרן (Na⁺) מהצד הפנימי של התא לחוץ, וליצור מפל נתרן. מפל זה דומה לסוללה טעונה: הוא מספק כוח למנוע השוט החיידקי לשחייה, מסייע בייצור ATP (מטבע האנרגיה של התא), ומניע קליטת מזון ויציאת תרופות. מאחר ש‑Na⁺‑NQR קיים רק בחיידקים ושונה מאוד מהאנזים המקביל במיטוכונדריה שלנו, הוא מהווה מטרה אטרקטיבית לאנטיביוטיקה סלקטיבית מאוד.
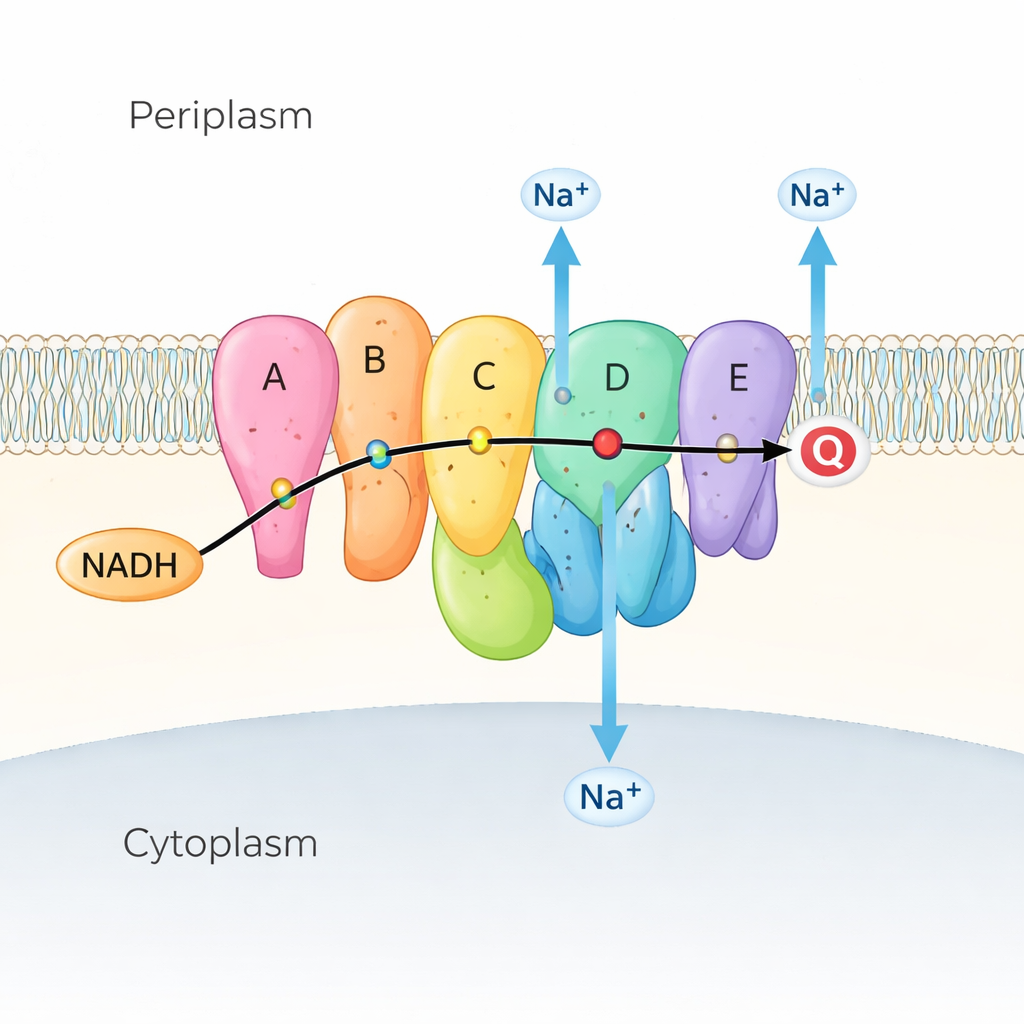
צופים במכונה בתנועה
תצלומי רנטגן וקריו‑אלקטרונים קודמים הראו היכן נמצאים תת‑יחידות וקופקטורים של Na⁺‑NQR, אך גם חשפו חידה: קפיצות אלקטרונים קריטיות היו מרוחקות מדי כדי שהאלקטרונים יעברו ביעילות אלא אם החלבון משנה את צורתו. המחברים פתרו זאת על‑ידי לכידת Na⁺‑NQR במצבים מעט שונים. הם השתמשו במוטנטים שמסירים קופקטורים מסוימים, בתרופות שעוצרות את התגובה בשלבים מוגדרים, ובתמיסות עם ואחרי הסרת נתרן. בעזרת קריו‑EM ברזולוציה גבוהה וניתוח תמונה מתקדם הם יכלו להפריד ולבנות מחדש קונפורמציות מרובות של אותו אנזים, ובאופן יעיל להפוך תמונות סטטיות לסרט של מחזור הפעולה שלו.
זרוע גמישה ומצמיד משוטט
ממצא מרכזי אחד כולל תת‑יחידה ציטופלסמית גמישה, NqrF, שמחזיקה שני קופקטורים נשאי אלקטרון. הצוות זיהה שלוש עמדות לדומייתה ה"כמו פרדוקסין" — שנקראו "מעלה", "אמצע" ו"מטה". במצב ה"מטה" הנדיר אך קריטי, דומיית זו מתנדנדת לכיס שנוצר על‑ידי שתי תת‑יחידות ממברנליות, NqrD ו‑NqrE, ומביאה את אשכול הברזל‑גפרית שלה קרוב מספיק להעברת אלקטרון הלאה. במקביל, תת‑יחידה פריפלסמית (חיצונית) הנקראת NqrC מתנהגת כמו צבת נעה. בקונפורמציה אחת ("יציבה") היא נצמדת כנגד תת‑יחידה ממברנלית אחרת, NqrB, וממוקמת להעביר אלקטרונים לכיוון מקבל הקוינון הסופי. בקונפורמציה שנייה ("מוסטת"), NqrC זזה לעבר NqrD/E, ומקרבת את הקופקטור הפלביני שלה כדי לקבל אלקטרון מאשכול הברזל‑גפרית שלהם. תנועות אלה מראות כי NqrF ו‑NqrC פועלים כשליחים דינמיים, שמגשרים על פערים גדולים בשרשרת הקופקטורים.
כיצד שינויים בצורה משאבים נתרן
לב המשאבה נמצא בזוגת תת‑היחידות NqrD ו‑NqrE, היוצרות חבילה מרכזית של הליקסים חוצים‑ממברנה. באמצעות מבנים וסימולציות דינמיקה מולקולרית ברמת אטום, המחברים מראים שכאשר אשכול הברזל‑גפרית ב‑NqrD/E מתחמצן פחות (צובר אלקטרון), הוא יוצר אתר בעל מטען שלילי שמושך יון Na⁺ וכמה מולקולות מים מצדו הציטופלסמתי, ויוצר כיס קשירה חולף. חומצות אמינו הידרופוביות מעל ומתחת לכיס זה מתנהגות כשערים פנימי וחיצוני, השולטים בגישה ליון. כאשר NqrD/E עוברים ממצב "פתוח פנימה" למצב "פתוח החוצה", ה‑Na⁺ נע לכיוון הצד הפריפלסמי ומשתחרר לבסוף בזמן שאשכול הברזל‑גפרית מחוזר מחדש. הסימולציות מראות שה‑Na⁺ נשאר חלקית מיובש אך לעולם לא נתקל במנהרה רציפה מלאה מים, מה שמרמז שהאנזים אטום היטב לדליפות פרוטונים בלתי רצויות.
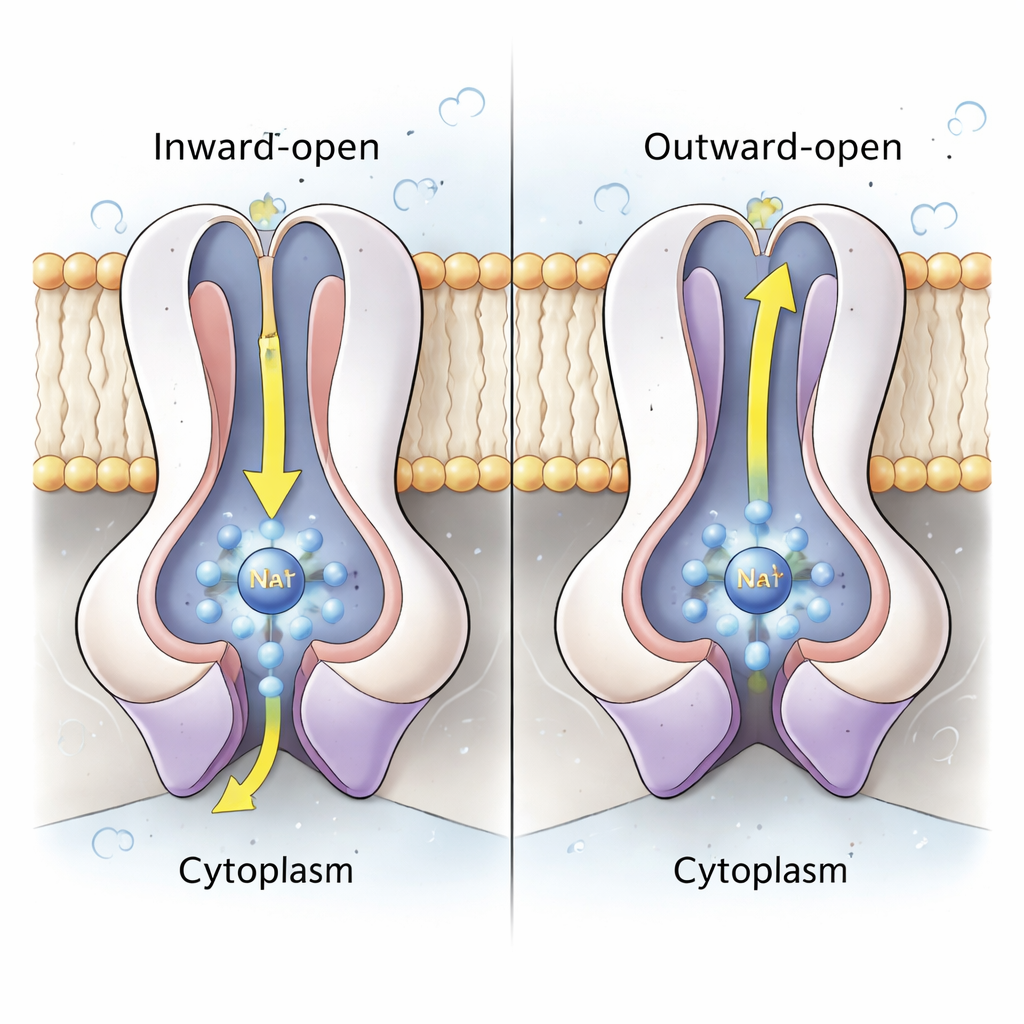
מחזור מתואם שמנע נעילה בכיוון הלא נכון
על‑ידי שילוב כל מצבי המבנה והסימולציות, החוקרים מציעים מחזור בן שישה שלבים. תחילה NADH נקשר ונותן אלקטרונים ל‑NqrF, שמעביר אלקטרון אחד ל‑NqrD/E, מה שמפעיל קליטת Na⁺ מהציטופלזמה וממלא את הכיס המרכזי. מעבר הקונפורמציה הנובע של NqrD/E למבנה הפתוח החוצה גם מגרש את ה‑Na⁺ לפריפלסמה וגם מעודד את NqrC לזוז למיקום המתאים לקבלת האלקטרון. שלבים בהמשך מעבירים אלקטרונים הלאה אל הקופקטורים הפלביניים והריבופלביניים ולבסוף אל הקוינון, שצריך לקבל שני אלקטרונים כדי להפוך לקינול. חשוב שהשינויים הקונפורמציוניים שמזיזים את ה‑Na⁺ גם מקלים ומתקשים לסירוגין על NqrF ו‑NqrC, כך שזרימת אלקטרונים קדימה תהיה סבירה רק כאשר ה‑Na⁺ נשאב החוצה ומנעה החלקה לאחור. קישור זה מסייע לאנזים לשאוב Na⁺ נגד מפל קיים, ולשמור על "הסוללה" החיידקית טעונה.
מדוע זה חשוב לרפואה ולביולוגיה
לא מומחה, עבודה זו ממחישה כיצד החיים בונים מכונות מתואמות להפליא מתוך חלבונים, שבהן שינויים זעירים במטען גוררים תנועות גדולות ושימושיות. עבור מחקר מחלות זיהומיות, היא מבהירה כי העברת ה‑Na⁺ ב‑Na⁺‑NQR מתרחשת בעיקר דרך הליבה NqrD/E, ולא דרך תת‑היחידה NqrB שנחשדה קודם לכן. תובנה זו מחדדת את המיקומים שבהם תרופות עתידיות צריכות להיקשר כדי לשבש בצורה הטובה ביותר את המנוע שמניע את Vibrio cholerae ומזיקים אחרים, תוך שמירה על אנזימים אנושיים. באופן רחב יותר, המחקר מספק שרטוט מבני לאופן שבו תגובות רדוקציה‑אוקסידציה יכולות להיות קשורות לשאיבת יונים — עקרון עיצוב שהטבע משתמש בו בצורות רבות של מכניקת ביואנרגיה.
ציטוט: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
מילות מפתח: משאבת נתרן, נשימה חיידקית, Na+-NQR, קריו‑EM, מטרות אנטיביוטיות