Clear Sky Science · he
מערכת סינתטית לפירופטוזה המגיבה ל‑RNA המבוססת על נוקלאאז‑פרוטאז מסוג III‑E של CRISPR
הפיכת התפוצצויות קטלניות של תאים לכלים ממוקדים
גופנו לעתים מגן על עצמו על‑ידי כך שתאים נגועים או פגועים מתפוצצים בתהליך אוטודממיטיבי דלקתי. הפיצוץ הזה לא רק מסלק תאים מסוכנים אלא גם מזעיק את מערכת החיסון. המחקר החדש מציג מעגל גנטי סינתטי, שנקרא DAMAGE, שיכול לקרוא את מסריו של ה‑RNA בתוך תא ולהחליט האם יש להשמידו. על‑ידי חיבור מערכת הגנה מיקרוביאלית למכונת המוות התאית שלנו, החוקרים מראים דרך להשמיד באופן סלקטיבי תאים נגועים בנגיפים, סרטניים או מזדקנים תוך שמירה על תאים בריאים בסביבה. 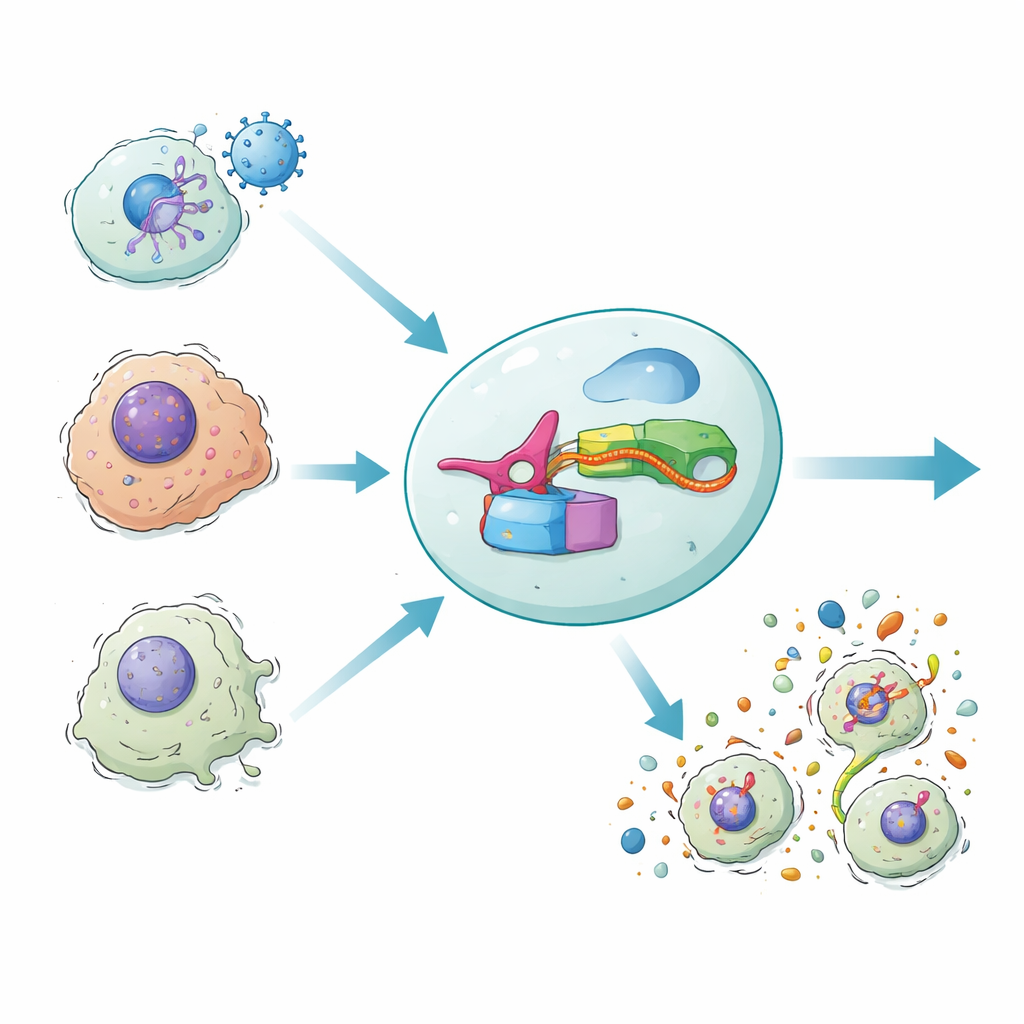
כיצד תאים בדרך כלל מנפצים את עצמם
במוות תאי דלקתי משפחה של חלבונים הידועים כגסטראמינים יושבת בתוך התאים כמו מטענים טעונים. לכל גסטראמין יש חצי קדמי "קטלני" היכול לחורר ממברנות תא, וחצי אחורי "מעצור" ששומר על הקטלן תחת שליטה. כאשר חיישני החיסון מזהים סכנה, אנזימים חותכים את הגסטראמינים לשניים, ומשחררים את החצי הקדמי לאסוף נקבים בממברנה החיצונית. התא מתנפח, מתפוצץ ומשלך אותות אזעקה שמגייסים תאים חיסוניים. תגובה עוצמתית זו מסייעת להילחם בזיהומים ובגידולים, אך רשת השליטה הטבעית שלה מסובכת וקשה לשינוי לצרכי טיפול.
הלוואת הגנות חיידקיות לקריאת RNA
חיידקים פיתחו מודולי הגנה קומפקטיים הידועים היום דרך טכנולוגיית CRISPR. אחד מהם, המערכת מסוג III‑E, משתמש בחלבון בשם Cas7‑11 שיכול להיקשר לרצפי RNA ספציפיים בעזרת RNA מדריך קצר. כאשר Cas7‑11 מוצא RNA מטרה מתאים, הוא מפעיל אנזים מלווה, Csx29, שחותך חלבון שותף, Csx30. הכותבים הבינו ש‑Csx30 יכול לשמש כ"ציר" ניתן להתאמה בין שני חלקי חלבון כלשהם. הם חיברו את הציר הזה בין חציו הקטלני וחציו המעכב של גסטראמין אנושי, ויצרו מבצעים מלאכותיים שנפתחים רק כאשר החיישן בסגנון CRISPR מזהה את ה‑RNA הנבחר בתוך תא.
מתג מוות ניתן לתכנות לתאים חולים
העיצוב הזה, ששמו DAMAGE (קיצור ל‑Death Manipulation Gene), בנוי מחמישה מרכיבים: חיישן Cas7‑11, החותך Csx29, היתוך גסטראמין–Csx30, RNA מדריך ו‑RNA המטרה בתוך התא. כשהמסר ה‑RNA המתאים מופיע, Cas7‑11 נקשר אליו, מפעיל את Csx29, ו‑Csx29 חותך את ציר ה‑Csx30 בחלבון הממוזג. חצי הקטלני של הגסטראמין משתחרר, חורר נקבים בממברנה והתא מת. על‑ידי החלפת ה‑RNA המדריך, הקבוצה ייחסה את DAMAGE למטרות תאיות שונות. הם הראו שהוא מטפל בזיהוי RNA של נגיף הנשימה הסינסיציאלי, ב‑HPV מסוג סיכון גבוה בתאי סרטן צוואר הרחם, ובכמה מוטציות מניעות סרטן ב‑KRAS השונות מהרצף התקין באות יחידה בודדת. בכל מקרה, תאים הנושאים את ה‑RNA החשוד הושמדו באופן סלקטיבי בעוד תאים עוקבים בסביבה נשארו שלמים. 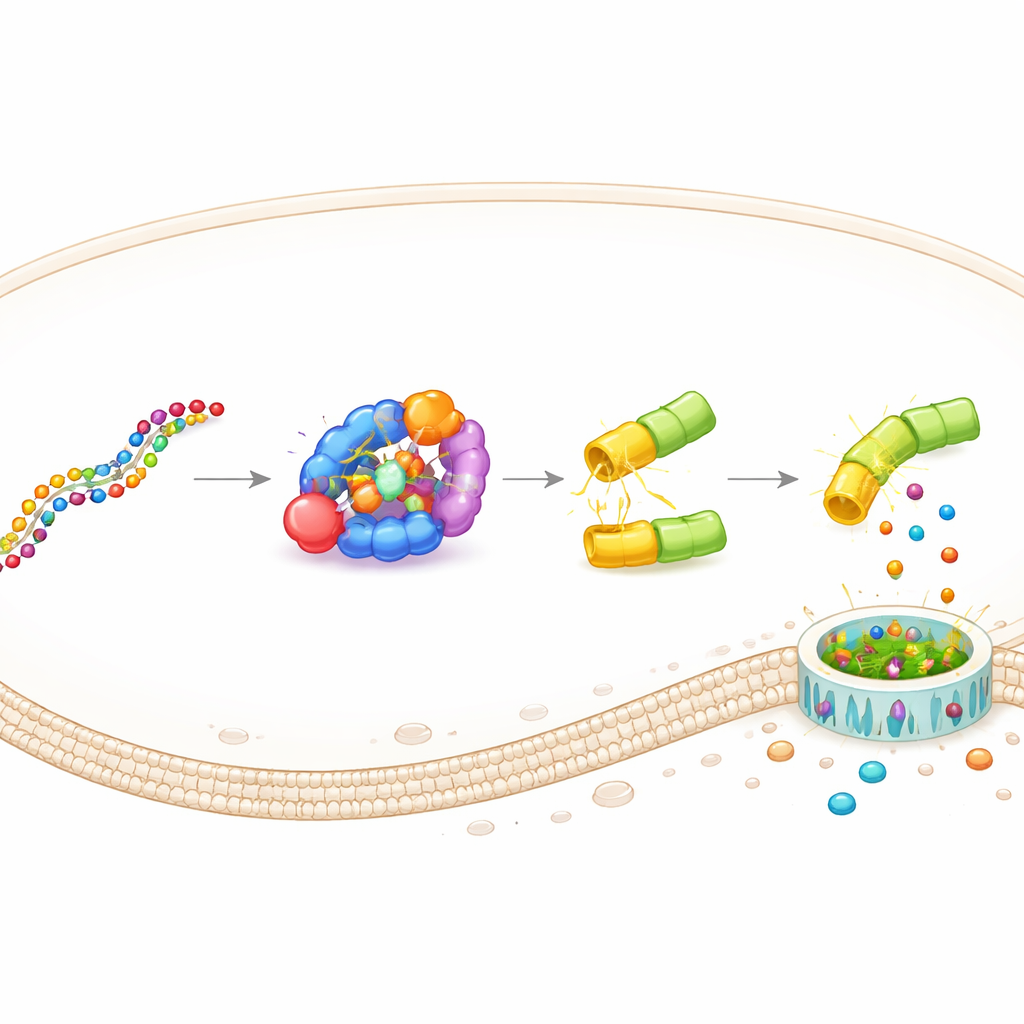
ממוקד בתאים מזדקנים
החוקרים גם בדקו האם DAMAGE יכול לצוד תאים סניסנטיים — תאים מזדקנים או בסטרס שמפסיקים להתחלק אך מצטברים ברקמות ותורמים לשבריריות ומחלות כרוניות. תאים כאלה מייצרים לעתים קרובות רמות גבוהות של שני חלבוני שער, p16 ו‑p21. על‑ידי תכנות מדריכים נגד ה‑RNA של p16 ו‑p21, הקבוצה יצרה גרסה שנקראת DAMAGE‑Aging. המעגל הזה הרג תאים בעלי רמות גבוהות של מסרים אלו בעודו שומר על תאים שבהם p16 הוסר גנטית, ואישר שהמערכת קוראת שפעוליות RNA בזמן אמת ולא שינויים קבועים ב‑DNA. טיפולים תרופתיים שגילו עלו את רמות p16 או p21 הגבירו את הפגיעות של תאים אלו לכתוצאה מהאוטו‑ההרס הממוקד.
חבילה של המערכת לטיפולים עתידיים
על מנת להתקדם לשימוש מעשי, המחברים דחסו את חלקי ה‑DNA של DAMAGE למבנה מקומט, DAMAGE‑Plus, והראו שהוא עודן עובד באמינות. הם לאחר מכן תעתקו את המבנה הזה ל‑mRNA סינתטי, ארזו אותו בננו‑חלקיקים שומניים בדומה לאלה שבחיסונים נגד COVID‑19, והעבירו אותו לתאים בתרבית. גרסת ה‑mRNA הצליחה להרכיב את המעגל ולגרום למוות דלקתי ממוקד בתאים שנשאו RNA ויראלי או הקשור לסרטן. אף על פי שהמערכת הכוללת עדיין מסורבלת ונבדקה רק בקווי תאים, התוצאות מרמזות שאפשר שייושם בעתיד חיסון mRNA הניתן בהזרקה להפעלת רצח תאי מ‑RNA הניתן לתכנות.
דרך חדשה לקרוא ולהגיב למסרים תאיים
בפשטות, DAMAGE הוא שוער מולקולרי הבודק את "תעודת הזהות" של RNA בתוך כל תא ומוציא רק את אלה שנראים מסוכנים — נגועים בנגיף, נושאי מוטציות או סניסנטיים — על‑ידי כיפוף שלהם לצורת אוטודממיטציה מתפוצצת. העבודה מראה שחיישני RNA חיידקיים ניתנים לקישור למכונות המוות של התאים האנושיים בדיוק גבוה, אפילו בהבחנה של הבדלי אות בודד במסרים גנטיים. למרות שעדיין נדרש הנדסה רבה לפני שמערכת כזו תוכל לשמש בבטחה בבעלי חיים או בבני אדם, היא משרטטת אסטרטגיה עוצמתית חדשה: קריאת השיחה החיה של RNA בתוך תאים ותרגומה ישירות להחלטות חיים‑או‑מוות.
ציטוט: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
מילות מפתח: פירופטוזה, CRISPR, טיפול מונחה RNA, אימונותרפיה של סרטן, זקנה תאית