Clear Sky Science · he
אוספים ברזולוציה אטומית של חלבונים בלתי מסודרים פנימית בעזרת AlphaFold
מדוע חלבונים שמשנים צורה חשובים
בתאים שלנו יש שפע של חלבונים שמעולם לא מתייצבים לצורה אחת נוקשה. חלבונים אלה, המכונים "בלתי מסודרים פנימית", מתנהגים יותר כמו אטריות רפויות מאשר כמכונות מקופלות להפליא, אך הם מרכזיים בתהליכים שמתחילים באיתות תאי ומגיעים למחלות נוירודגנרטיביות. מאחר שהם נעים ומתמתחים כל הזמן, תפיסת טווח הצורות שלהם ברזולוציה אטומית קשה מאוד ודורשת בדרך כלל שנות ניסויים וחישובים כבדים. מאמר זה מציג דרך חדשה למנף אינטיליגנציה מלאכותית ופיזיקה יחד כדי למפות מולקולות חסרות מנוחה אלה בצורה יעילה בהרבה.
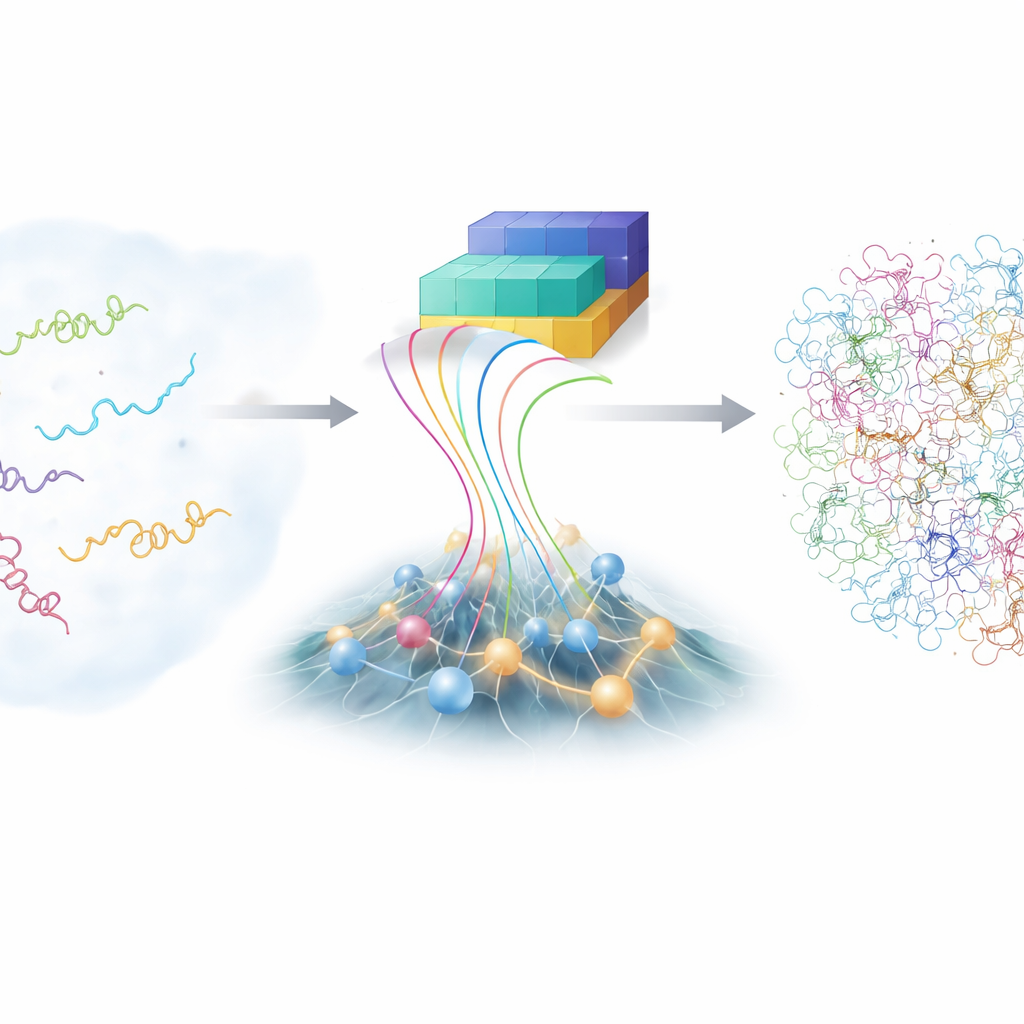
האתגר של מולקולות חסרות מנוחה
בניגוד למודלים בספרי הלימוד שמראים מבנה מסודר אחד, חלבונים בלתי מסודרים פנימית (IDPs) שוטטים בנוף עצום של צורות אפשריות. הגמישות הזו עוזרת להם לזהות שותפים רבים ושונים, אך גם מקשה על חקירתם. טכניקות מעבדה מסורתיות, כמו תהודה מגנטית גרעינית מתקדמת ופיזור רנטגן, יכולות לדווח על ממוצעים על פני מגוון צורות אבל לא על כל צורה בודדת. סימולציות ממדיה אטומית מלאות יכולות, בתיאוריה, לעקוב אחרי כל אטום בזמן שה‑IDP מתפתל, אך הן יקרות מאוד ותלויות במודלים פיזיקליים מאוד מכוילים. כתוצאה מכך, הקהילה המדעית מחזיקה באוסף מוגבל בלבד של אוספי IDP מדויקים ומפורטים ללמוד מהם.
שילוב ניחושים חכמים עם חוקים פיזיקליים
בשנים האחרונות משפחת הכלים של AlphaFold, מבוססת־למידה עמוקה, הכתה את עולם הביולוגיה באמצעות ניבוי מבני חלבון מתוך רצפי חומצות האמינו שלהם. עבור חלבונים לא מסודרים, עם זאת, החוזקה הרגילה של AlphaFold — ניחוש הצורה הטובה ביותר אחת — פחות מועילה, כי ל‑IDP אין רק צורה אחת. מה ש‑AlphaFold כן מספק הוא מידע עשיר לגבי הסבירות שמקטעים שונים של השרשרת יהיו קרובים או רחוקים זה מזה. המחברים בנו מסגרת חדשה, שנקראת bAIes, שמטפלת במידע שמקורו ב‑AI כהדרכה רכה ומשלבת אותו עם מודל פיזיקלי מהיר שמתחיל בכוונה מנקודת מבט של "סליל אקראי", שבה השרשרת בוחנת את כל העקמומויות והסיבובים האפשריים ללא הטייה למבנה מסוים.
מבלגנים אקראיים לאוספים ריאליסטיים
ראשית, החוקרים בנו מודל פיזיקלי יעיל שמשחזר כיצד שרשרת חלבון חסרת מבנה מתנהגת, בהתבסס על סטטיסטיקות שחולצו מאלפי מבני חלבון ידועים. מודל זה משמש כ"פריור" — הציפייה הבסיסית לאופן שבו IDP נע אם אין לנו מידע נוסף. לאחר מכן, bAIes קורא את תחזיות AlphaFold לגבי זוגות שאריות שנוטים להתקרב זה לזה. במקום לכפות על החלבון דפוס יחיד, הוא הופך רמזים אלה לאילוצי מרחק עדינים עם אי־וודאות מובנית, ומאפשר לשרשרת למלא את המלצות ה‑AI רק כאשר הן תואמות את התמונה הפיזיקלית הרחבה יותר.
בדיקה מול ניסויים אמיתיים
כדי לבדוק האם הגישה הזו עובדת, הצוות יישם את bAIes על קבוצת בת 21 חלבונים הנעשים מ‑סלילים כמעט אקראיים ועד מערכות מורכבות יותר עם סלילים זמניים ודומיינים מרובים. עבור כל אחד מהם הם השוו את האוספים שנוצרו במחשב למגוון רחב של מדידות ניסיוניות הבוחנות גם פרטים מקומיים וגם גודל וצורה גלובליים. עבור חלבונים רפויים מאוד, כגון הפפטיד הקשור לאלצהיימר Aβ40, מודל הסליל האקראי הפשוט כבר היה קרוב למציאות, ו‑bAIes שמר על התאמה טובה זו. עבור חלבונים חלקית ממודרים, bAIes שיפר את ההתאמה לניסויים על ידי לכידת המקומות שבהם מקטעי סליל קצרים או כתמים קומפקטיים מופיעים ונעלמים. קריטי מכך, השיטה נשארה חזקה גם כאשר AlphaFold היה בטוח מדי וניבא בטעות קיפולים יציבים בעוד ניסויים בתמיסה מראים אי־סדר, כי bAIes מאפשר במפורש שגיאות בקלט ה‑AI.
נעילת או השוואה לשיטות קיימות
המחברים השוו אז את bAIes לסימולציות אטומיות כבדות המתבצעות על מחשבים-על ייעודיים, למודלים גסים שמפשטים חלבונים לגרגירים, ולמחוללי למידה עמוקה חדשים שאומנו על נתוני סימולציה. במגוון מבחנים, bAIes התאמה או עלתה על גישות אלה בשחזור נתונים ניסיוניים, ובמקביל דרשה הרבה פחות משאבים חישוביים מאשר סימולציות בקנה מידה מלא. היא עבדה גם מעבר ל‑IDP פשוטים, וטיפלה בחלבונים עם כמה דומיינים קשיחים מקושרים באמצעות מחברים גמישים והשיבה את צורתם הכללית בתמיסה. כאשר החוקרים כיווננו עוד יותר את האוספים של bAIes בעזרת נתונים ניסיוניים, ההתאמה השתפרה אף יותר, מה שמראה שהשיטה יכולה לשמש כנקודת מוצא חזקה למידול אינטגרטיבי.
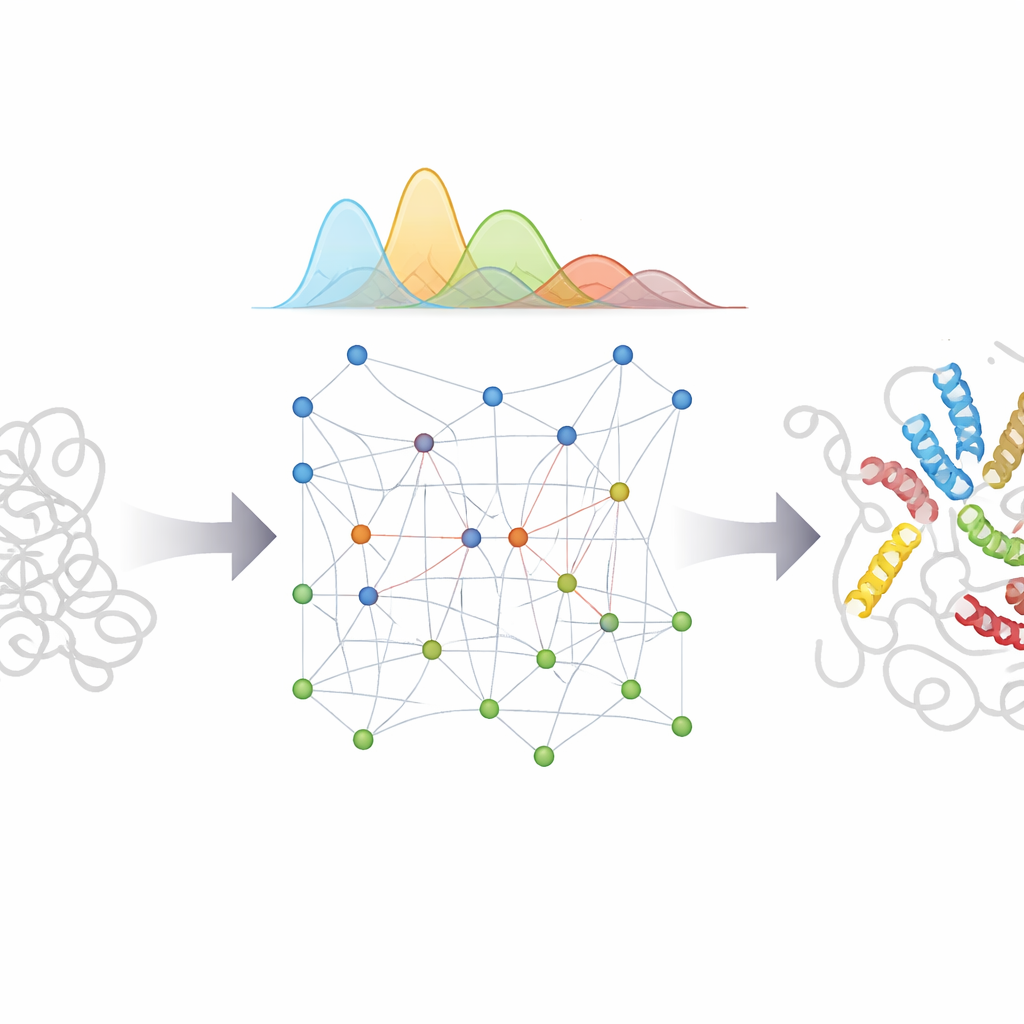
מה משמעות הדבר לביולוגיה ולרפואה
על ידי חיבור כוח זיהוי התבניות של AlphaFold עם מודל פיזיקלי מתוכנן בקפידה וטיפול בייסיאני של אי־ודאות, bAIes מציע מסלול מעשי ל"סרטים" מפורטים של חלבונים בלתי מסודרים במקום תמונות יחידות. אוספים מפורטים ברזולוציה אטומית אלה יכולים לסייע למדענים להבין כיצד אזורים גמישים מזהים שותפים, כיצד מתחילה התיק-folding וההצטברות במחלות כמו פרקינסון ואלצהיימר, וכיצד מולקולות קטנות עשויות לקשור מטרות חמקמקות ומשתנות. מכיוון שהשיטה יעילה ומובנית בתוכנה בקוד פתוח, היא ניתנת לאימוץ נרחב ליצירת אוספים ריאליסטיים עבור חלבונים בלתי מסודרים רבים, להנחות ניסויים ולתמוך במערכות AI עתידיות שמטרתן לחזות לא רק מבנה אחד, אלא את טווח הצורות המלא שחלקיקי החיים הגמישים ביותר יכולים לאמץ.
ציטוט: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
מילות מפתח: חלבונים בלתי מסודרים פנימית, AlphaFold, מידול בייסיאני, אוספי חלבונים, ביולוגיה מבנית