Clear Sky Science · he
מנגנון מולקולרי של ייבוא זרחן על ידי נשא החיידקים PstSCAB
למה מזונות זעירים חשובים לנו
כל תא חי, מתאי עצב אנושיים ועד לחיידקי קרקע, זקוק לפוספורוס להפעלה. היסוד הזה מסייע לאחסון אנרגיה, לבניית DNA ולשמירה על שלמות ממברנות התא. עם זאת, בסביבה אזור הפוספט הזמין — הצורה של הפוספורוס שתאים יכולים לייבא בפועל — לעיתים נדירה. חיידקים רבים שגורמים למחלות מסתמכים על מכונה מולקולרית יעילה מאוד, הנקראת נשא PstSCAB, כדי לשאוב פוספט כאשר הוא במחסור. הבנה מדויקת של אופן פעולת המכונה אינה שאלה מדע בסיסית בלבד; היא עשויה לפתוח דרכים חדשות לנטרל זיהומים על ידי הרעבת החיידקים ממזין חיוני זה.
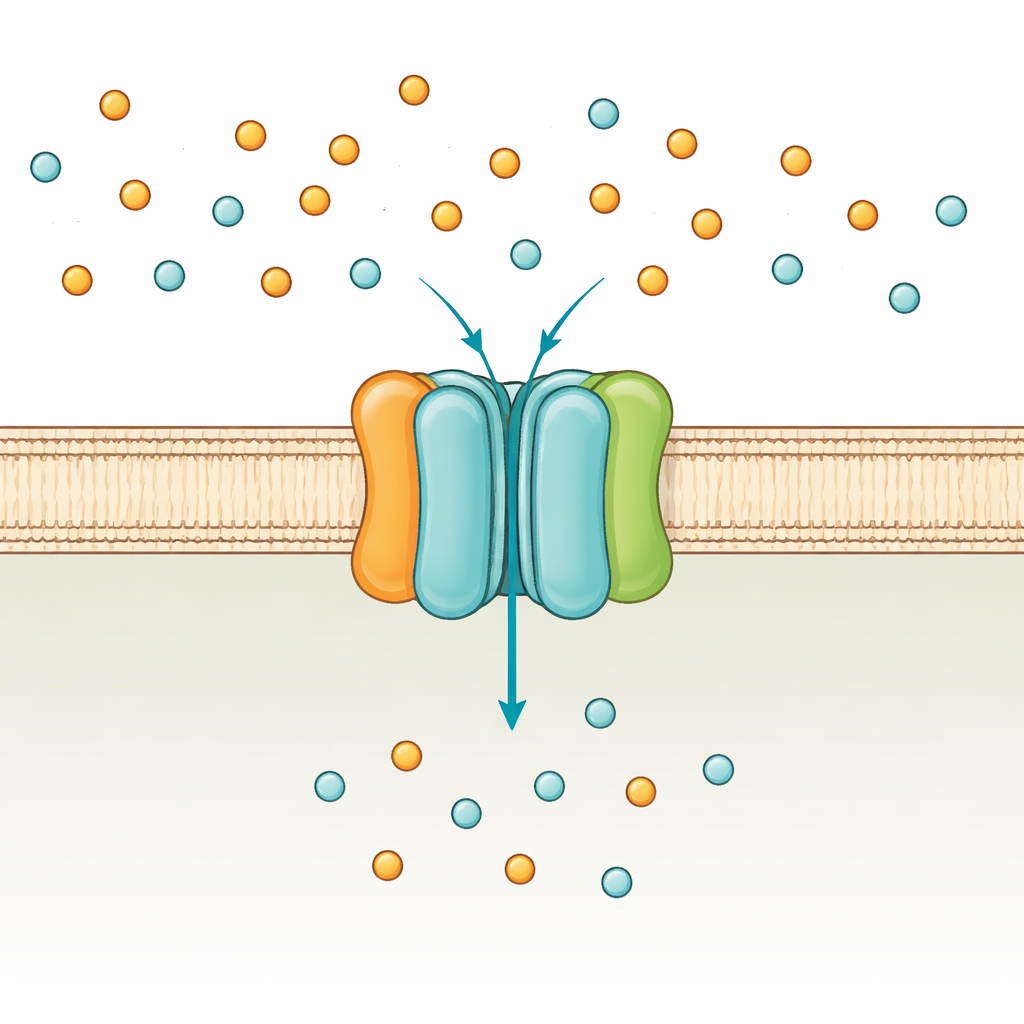
שומר השער של התא על זרחן
חיידקים כגון Escherichia coli משתמשים בשני מסלולים עיקריים לקליטת פוספט: מערכת בעלת זיקה נמוכה שפועלת כאשר פוספט רב, ומערכת PstSCAB בעלת זיקה גבוהה שנכנסת לפעולה בעיתות מחסור. PstSCAB מושתל בממברנת התא ומונע על ידי ATP, מטבע האנרגיה האוניברסלי של התא. הוא בנוי מחמשת חלקים: שני תת־יחידות מושתלות בממברנה (PstA ו־PstC) שיוצרות את תעלת המעבר, חלבון "לוכד" מסיס מחוץ לממברנה (PstS) שתופס את הפוספט, וזוג תת־יחידות פנימיות (PstB) שורפות ATP להנעת הטרנספורט. מאחר שמערכת זו מסייעת גם בשליטה על גנים רבים הקשורים לוירולנציה של חיידקים, מוטציות ב־PstSCAB יכולות להחליש פתוגנים הגורמים לזיהומי דרכי שתן, ספסיס בבעלי חיים ביתיים ושחפת.
לתפוס את המכונה בפעולה
עד כה, המדענים ראו רק תצפיות חלקיות של PstSCAB, בעיקר של חלבון הלכידה PstS לבדו. בעבודה זו השתמשו החוקרים במיקרוסקופ אלקטרונים קפוא ברזולוציה גבוהה כדי להמחיש את כל הנשא בכמה שלבים מרכזיים של מחזור הפעולה שלו. הם השיבו את חלבוני החיידק לתוך "ננודיסקים" ממברנליים מלאכותיים והקפיאו אותם במהירות עד שהמולקולות נלכדו בתנועתן. על ידי כוונון מדויק של החלבונים והוספה או הוצאת ATP, הם השיגו מבנים של שלוש מצבים עיקריים: צורה מנוחה הפונה פנימה ללא הלכיד, מצב טרנסלוקציה מוקדם שבו PstS שטעון בפוספט מתחבר למורכב הממברנה, ובין־ביניים קטליטי קשור ל־ATP שבו הפוספט מוחזק בתוך הנשא.
כיצד שינויים בצורה מזיזים פוספט
התמונות מגלות כיצד שינויים מתואמים בצורה מעבירים את הפוספט מחוץ לפנים התא. במצב המנוחה, תעלת המעבר שנוצרת על ידי PstA ו־PstC פתוחה רק כלפי פנים התא; הצד החיצוני אטום על ידי קבוצת "שער" של שאריות, כלומר פוספט עדיין לא יכול להיכנס מבחוץ. כאשר PstS שטעון בפוספט מתחבר במצב הטרנסלוקציה המוקדם, הוא מושחל בין לולאות גמישות של PstA ו־PstC אך, באופן מפתיע, תת־היחידות הממברנליות כמעט שאינן משנות צורה. המעבר האמיתי מתרחש כאשר PstS מתחיל לפתוח את שתי אונותיו כדי לשחרר את הפוספט ובמקביל שתי תת־יחידות PstB נעות יחד כדי לקשור ATP. קשירת ה־ATP מהדקת את PstB לדימר ומתיחה של הסלילים המחברים ב־PstA וב־PstC, מה שמפליפ את כל הנקבובית לקונפורמציה הפונה החוצה החושפת לכיוון החוץ כיס קשירה ספציפי לפוספט.
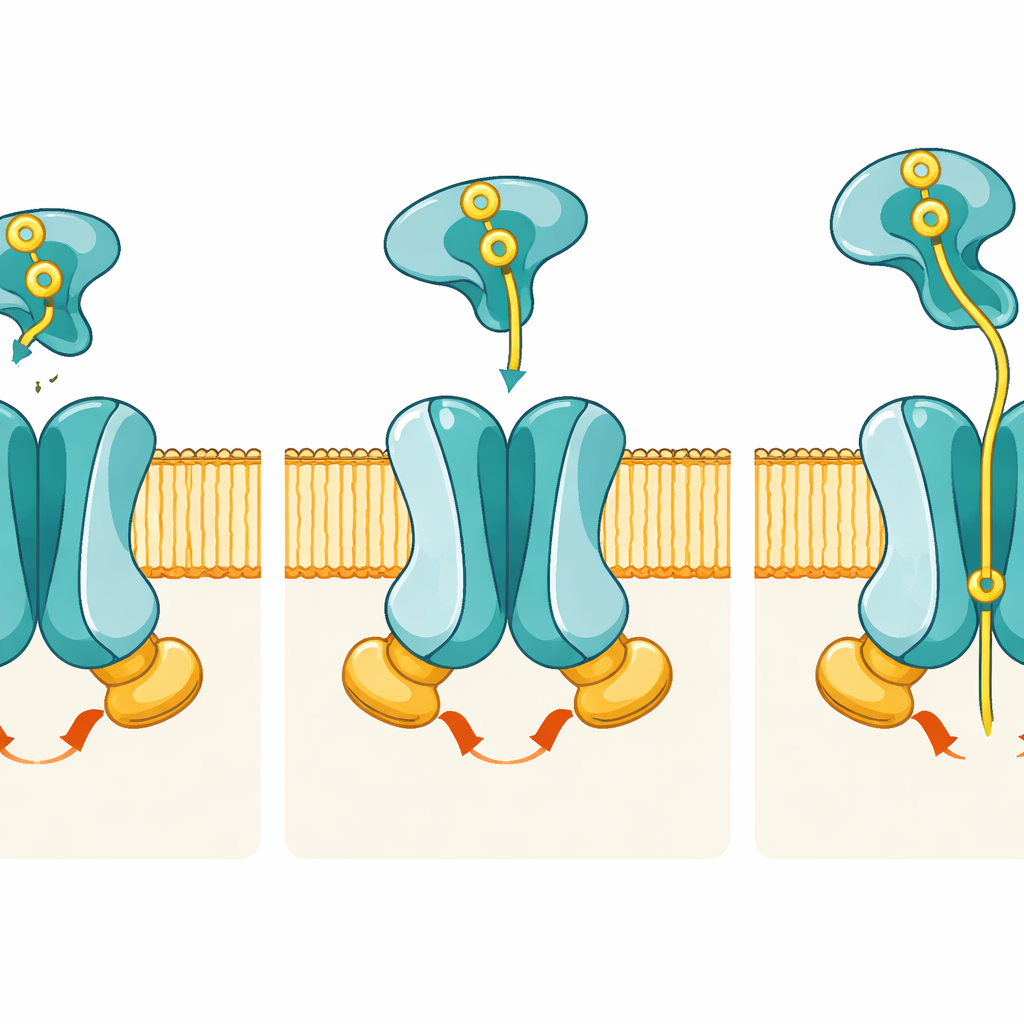
כיס מותאם אישית לפוספט
במבנה הפונה החוצה וקשור ל־ATP, המחברים מוצאים צפיפות באזור האמצעי של אזור הממברנה שמתאימה ליון פוספט. יון זה מוחזק בקרבת חומצות אמינו טעונות בחיוב — במיוחד שתי ארגינינות, אחת מ־PstA ואחת מ־PstC — שפועלות כמו קצות אצבע מולקולריות האוחזות בפוספט בעל המטען השלילי. סימולציות ממוחשבות מראות שהפוספט נשאר קשור בייצוב לכיס זה על פני מיקרו־שניות, וניסויים גנטיים מאשרים את חשיבותו: כאשר שאריות מפתח אלה מוטציות, הנשא עדיין שורף ATP אך מייבא פוספט בצורה ירודה מאוד. הפרדה זו בין "מקום שבו מנוצלת אנרגיה" ל"מקום שבו מוכר המטען" מדגישה עד כמה המכונה מכוילת בדיוק עבור פוספט.
ממפת מבנים אל הבטחה רפואית
ביחד, המבנים והמבחנים הביוכימיים התומכים מסכמים מחזור מלא: PstS תופס פוספט בחוץ, מתחבר לנשא הפונה פנימה, ואז — בקישור ובשבירה של ATP על ידי PstB — מעורר הפיכה שמעבירה את הפוספט אל כיס הממברנה ולבסוף אל פנים התא. לאחר הידרוליזת ה־ATP, המכונה נרגעת חזרה למצב המנוחה, מוכנה לסיבוב נוסף. עבור הקורא הלא מומחה, המסר המרכזי הוא שעכשיו יש לנו שרטוט ברמת האטום של האופן שבו חיידקים רבים שורדים בסביבות דלות פוספט ומווסתים את וירולנצייתם. המפה המפורטת הזו יכולה להנחות עיצוב של תרופות, נוגדנים או פפטידים שיחנוקו את הנשא או יחסמו את חלבון הלכידה שלו, ובכך יהפכו שער חיוני למטרה טיפולית פגיעה.
ציטוט: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
מילות מפתח: הובלת זרחן, קליטת מזון חיידקי, נשא ABC, PstSCAB, מטרות אנטיבקטריאליות