Clear Sky Science · he
אלקנילציה ואלקינילציה סלקטיבית בשלב מאוחר של N-Me בתרופות ובאמינים גבוהים לא מונעים באמצעות קטליזה פוטורדוקס
מדוע עדיין חשוב לשנות תרופות ישנות
רבות מהתרופות של היום פועלות היטב אך יש להן עדיין מקום לשיפור בבטיחות, באפקטים הלוואי או בדיוק שבו הן פוגעות ביעדים בגוף. כימאים מגלים יותר ויותר עניין ב"כיוונון" עדין של תרופות קיימות בשלב מאוחר של תהליך הפיתוח, במקום להמציא מולקולות חדשות מאפס. המחקר הזה מראה כיצד קרני אור נראה-גל יכולות לשמש לחיבור קטעים חדשים אל יחידת בנייה נפוצה בתרופות, וליצור מועמדים אנטידפרסנטיים משופרים ולפתוח מסלול מהיר יותר לטיפולים משופרים.
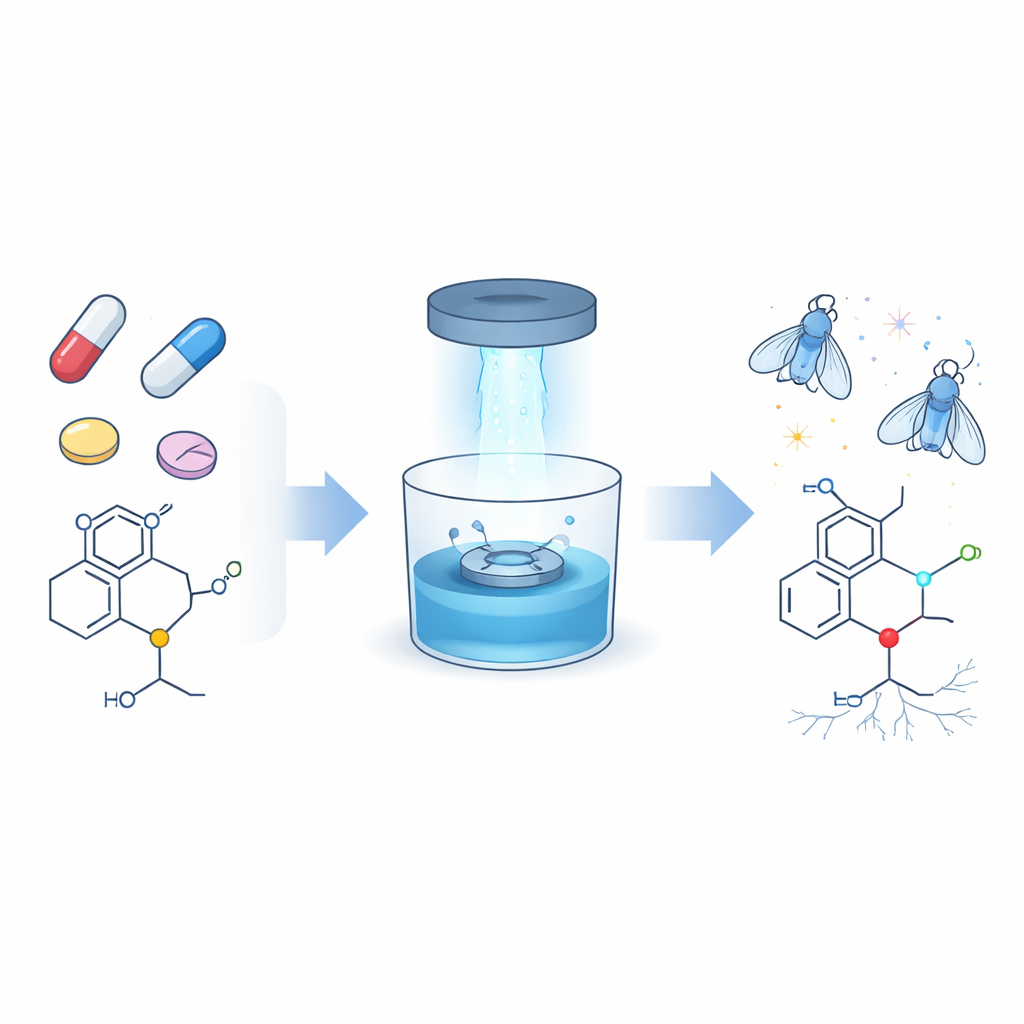
שדרוג תכונה נפוצה בהרבה תרופות
מגזר מפתיע של תרופות מודרניות — יותר משניים מתוך כל חמישה — מכיל שברים עשירים בחנקן הנקראים אמינים, ולרובם תת-סוג הידוע כאמינים שלישוניים. הם מופיעים באנטיביוטיקה, בתרופות לסרטן, נגד אלרגיה, משככי כאבים ואנטידפרסנטים. עד היום התקשו כימאים לשנות באופן סלקטיבי רק חלק זעיר מהקבוצה הזו, יחידת N-מתיל, כאשר היא נמצאת בין כמה קשרי פחמן־מימן כמעט זהים. החוקרים שאפו לפתח דרך עדינה ואמינה לחבר "ידיות" חדשות, ספציפית קשרי פחמן־פחמן כפולים (אלקנים) ומשולשים (אלקינים), למיקום ה‑N‑מתיל בלי להפריע לשאר מולקולת התרופה.
שימוש באור כדי לשנות קשר אחד בכל פעם
הקבוצה פנתה לקטליזה פוטורדוקס, טכניקה המשתמשת באור נראה ובקטליזטור רגיש לאור להזזת אלקטרונים יחידים ולהנעת תגובות בתנאים עדינים. במערכת שלהם, אור כחול מעורר קטליזטור אורגני שמושך זמנית אלקטרון מהאמין השלישוני. שלב זה יוצר רדיקל קצר-חיים באתר ה‑N‑מתיל שיכול להצטרף למולקולות שותפות נבחרות הנושאות קבוצות ויניל או אלקיניל. באמצעות כוונון תנאי התגובה — בחירת ממס, בסיס ותוספים — השיגו החוקרים תשואות גבוהות ושליטה מצוינת, כך שהקבוצה החדשה נקשרת כמעט באופן בלעדי למיקום ה‑N‑מתיל, גם כשיש מספר אתרים דומים. הם הדגימו זאת על מגוון רחב של אמינים פשוטים ולאחר מכן על תרופות אמיתיות, כולל אנטיהיסטמינים, תרופות לב, אנטי-מיקרוביאליות ומספר אנטידפרסנטים.
מהכיוון הכימי לשיפור הפעילות האנטידפרסנטית
כדי לבדוק האם השינויים המבניים הללו יכולים להיות בעלי משמעות רפואית, התמקדות החוקרים הייתה באימיפרמין, אנטידפרסנט טריציקלי ותיק. הם תכננו ודגמו יותר מעשרים וריאנטים של אימיפרמין שבהם התוספת הוינילית או האלקינילית נשאה טבעות ארומטיות שיכולות להתאים בנוחות לכיס הידרופובי של מוביל הסרוטונין האנושי, חלבון השולט ברמות המוליך הקשרי סרוטונין. חיזורי מולקולות במחשב הציעו שרבים מהמולקולות המותאמות הללו ייקשרו לפחות באותה מידה, או טוב יותר, מהתרופה המקורית. המועמדים המבטיחים ביותר סונתזו באמצעות השיטה המונעת באור ונבדקו במערכות חיות: דגם זבוב פרי של דיכאון המבוסס על בידוד חברתי, ועבור שני התרכובות הטובות ביותר, תאי עצב עכבריים שמובילים סרוטונין באופן פעיל.
כיצד זבובים ותאים גילו תרופות חזקות יותר
בזבובים זכרים מבודדים, התנהגות הדמויית דיכאון מתבטאת בהתנהגות תוקפנית מוגברת. הזנת אימיפרמין מקטינה תוקפנות זו, מה שמשקף את פעולתו האנטידפרסנטית בבני אדם. באופן מרשים, מספר מהנגזרות של אימיפרמין שהופקו בשיטה החדשה הפחיתו תוקפנות באותה המידה, וארבע מועמדות פעלו אף טוב יותר מאימיפרמין עצמו. בתאים היפוקמפאליים מעובדים של עכבר, שתי תרכובות מובילות חסמו החזרת סרוטונין ביתר עוצמה מאשר אימיפרמין, כפי שאושש הן במדידות כימיות ישירות של הסרוטונין והן על ידי צבע פלואורסצנטי המאיר כאשר הוא נלקח לתאים. המבחנים הללו מצביעים על כך ששינויים עדינים בשלב מאוחר באתר ה‑N‑מתיל יכולים באמת להגביר את עוצמת האנטידפרסנט ולא רק לשנות את המבנה על הנייר.
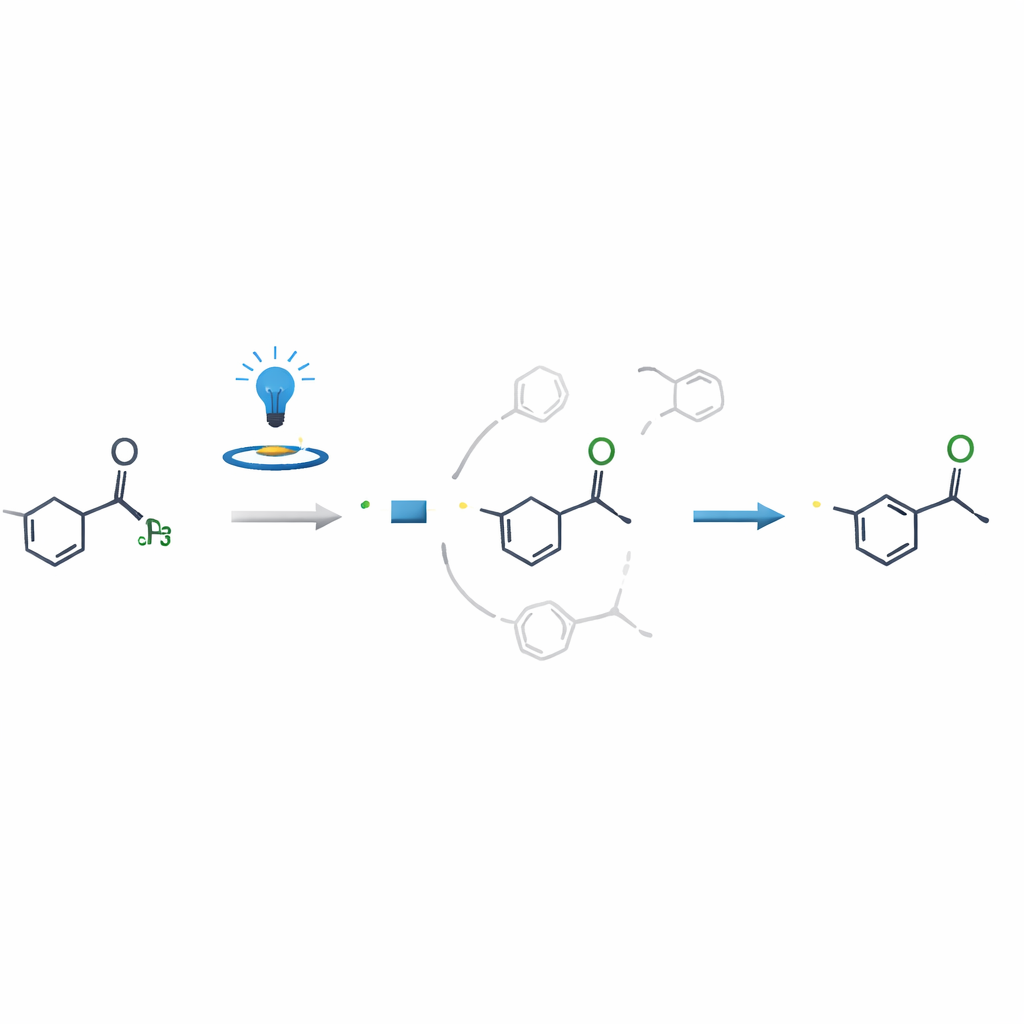
מדוע התגובה כל כך סלקטיבית
שאלה מדעית מרכזית הייתה מדוע התגובה משנה את קבוצת ה‑N‑מתיל כל כך נקי כאשר עמדות סמוכות נראות ככאלה בעלות ריאקטיביות דומה. באמצעות ניסויי בקרה, מדידות ספין אלקטרוני וחישובים מפורטים במחשב, הראו החוקרים כי נקודת ההחלטה הקריטית אינה ברגע שבו הרדיקל נוצר לראשונה, אלא כאשר אותו רדיקל מוסיף למולקולת הויניל או האלקיניל. הנתיב המוביל מהרדיקל של ה‑N‑מתיל למוצר הסופי הוא גם אנרגטית קל יותר והרבה יותר מהיר מזרמים מתחרים, ובאופן יעיל מייצב את התגובה לתוצאה אחת. תובנה זו מסבירה את הסלקטיביות הגבוהה ויכולה להנחות אסטרטגיות דומות על מולקולות מורכבות אחרות.
מה העבודה הזו אומרת לגבי תרופות עתידיות
בסך הכול, המחקר מציג דרך מעשית לשדרוג סלקטיבי של תרופות קיימות המכילות אמינים שלישוניים, בהוספת "ידיות" כימיות קומפקטיות שיכולות לכוונן את האינטראקציה שלהן עם יעדים ביולוגיים או לקשרן לרכיבים אחרים. על ידי הצגה שעדכונים בשלב מאוחר מסוג זה יכולים להפוך אנטידפרסנט מבוסס לוריאנטים יעילים יותר במודלי בעלי חיים ותאים פשוטים, העבודה מצביעה על שילוב רב-עוצמה של כימיה סינתטית מודרנית, חישוב וביולוגיה. ככל שהגישה תורחב לתרופות נוספות, היא עלולה לזרז את השיפור של מועמדי תרופות ולעזור לרענן תרפיות ישנות בביצועים ובבטיחות משופרים.
ציטוט: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
מילות מפתח: קטליזה פוטורדוקס, פונקציונליזציה בשלב מאוחר, אמינים שלישוניים, עיצוב תרופות נגד דיכאון, מוביל הסרוטונין