Clear Sky Science · he
אסטרטגיה סינתטית קומבינטורית לפיתוח נשאים חלבוניים לעריכת גנום המיועדים לרשתית של עכבר
תקווה חדשה לטיפול בעוורון תורשתי
צורות רבות של עוורון תורשתי מתחילות בגֵן בודד פגום בתאים החושיים לאור שבחלק האחורי של העין. כלי העריכה הגנטית המודרניים כמו CRISPR יכולים, מבחינה עקרונית, לתקן שגיאות אלה, אך הובלת המכשור העריכה בבטחה אל התאים המתאימים הייתה מכשול מרכזי. המחקר המתואר כאן מציג דרך חדשה לשנע עורכי גנים רבי-עוצמה ישירות אל רשתית העכבר באמצעות חלקיקים מיוחדים הדומים לשומן, ומעלה את האפשרות לטיפולים חד-פעמיים המשחזרים ראייה באנשים עם מחלות עיניים תורשתיות.
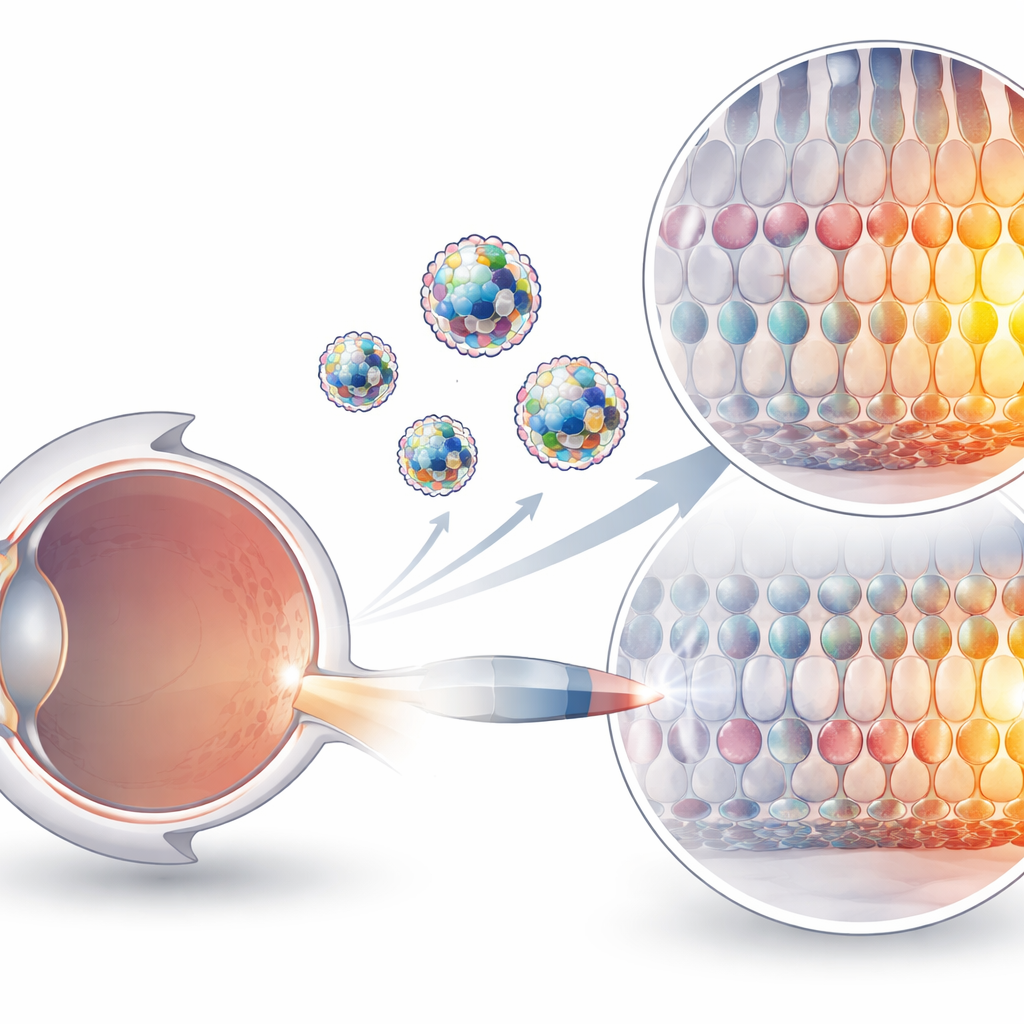
מדוע קשה כל כך להעביר עורכי גנים
כעת כלים מבוססי CRISPR יכולים לשנות אותות בודדים בדנ"א מבלי לחתוך את שני הגדילים, קידמה שהופכת אותם לאטרקטיביים לטיפול במחלות גנטיות. אך כלים אלה הם מכונות חלבון–RNA מגושמות, טעונות חשמלית ורגישות בתנאי הגוף. שיטות ההעברה הנפוצות כיום מסתמכות בעיקר על וירוסים מותאמים או על חלקיקים הנושאים את המתווה הגנטי של העורך במקום העורך עצמו. וירוסים עלולים לעורר תגובות חיסוניות ומוגבלים בגודל, בעוד העברת mRNA פועלת היטב בכבד אך נותרת לא יעילה ברקמות רבות אחרות, כולל העין. הזרקה ישירה של קומפלקסי חלבון–RNA מורכבים מראש היא רעיון נקי ובעל פוטנציאל ביטחון גבוה יותר, אך הם חסרו נושאים מתאימים המסייעים להם לחצות ממברנות תאים ולהגיע ליעדיהם.
מעבורת חלבונים בהשראת צבע
החוקרים פנו לנקודת התחלה בלתי צפויה: Coomassie Brilliant Blue, צבע כחול עמוק המשמש במעבדות ביולוגיה ואשר כבר מאושר לשימוש בניתוחי עיניים מסוימים. צבע זה נקשר בחוזקה לחלבונים רבים. הצוות קישר כימית "ראשי" Coomassie ל"זנבות" שומניים כדי ליצור משפחה של מולקולות חדשות שנקראות ליפידואידים. במים, ליפידואידים אלה נוטים להצטבר לחלקיקים, כשהחלקים השומניים קבורים בפנים וקבוצות ה-Coomassie חשופות מבחוץ, שם הן יכולות לתפוס חלבונים. על ידי שינוי אורך, הסתעפות והמטען של הזנבות, הביאו המדענים לעשרות תרכובות מועמדות שנועדו לקשור חלבוני עריכה מצד אחד ולהתקשר עם ממברנות תאים מצד שני.
בדיקת העברת חלבונים לתאי העין
כדי לראות אילו עיצובים עובדים בפועל, השתמשה הקבוצה תחילה בחלבון בדיקה פשוט בשם Cre recombinase, שמחליף מתג גנטי מהבהוב ירוק לאדום או להפך בתאים ומהנדסים ומבעכברים דיווחים. מספר ליפידואידים מבוססי Coomassie העבירו את Cre ביעילות לתאים בתרבית, והפכו אחוזים גדולים של תאים מירוק לאדום. כאשר הוזרקו מתחת לרשתית של עכברי דיווח, תרכובות נבחרות עוררו שינויים מרשימים בצבע גם בשכבת הפיגמנט התומכת בראייה וגם בתאי הפוטורצפטורים החושיים לאור, והראו שהחלבונים הגיעו אל התאים שנפגעים ברבים ממחלות העיוורון. ניסויים מוקדמים אלה גם חשפו ששינויים עדינים במבנה הליפידואיד עשויים להזיז אילו סוגי תאים ממוקדים, רמז לכך שגרסאות עתידיות יכולות להיות מכוונות לשכבות רשתית מסוימות.
הגברה של עריכת גנים והצלת הראייה
בהמשך הטעינה הקבוצה את המערכת בעריכת בסיסים של אדנין, וריאנט משוכלל של CRISPR שיכול לתקן את המוטציה החד־אותית הספציפית שגורמת לאובדן ראייה בעכברים מסוג rd12, מודל של עוורון תינוקות חמור. ברמתה הבודדת, קומפלקס החלבון–RNA של העורך חדר לתאים באופן גרוע. ליפידואיד אחד, שכונה CBB11, שיפר את ההעברה אך נטה להצטבר בתמיסה. כדי לייצב אותו, הטמיעו החוקרים את CBB11 בתוך ליפוזומים קטנים ומוגדרים היטב—כדורים חלולים העשויים ממספר סוגי ליפידים, כולל מרכיבים הנמצאים בשימוש קליני בחיסוני mRNA. בניסוחים אלה, CBB11 על פני השטח של הליפוזום תפס את רכיב החלבון של העורך, בעוד שליפידים אחרים סייעו בקשירת מנחה ה-RNA, ויצרו מעטפת שיתופית שהחזיקה את כל הקומפלקס על פני החלקיק.
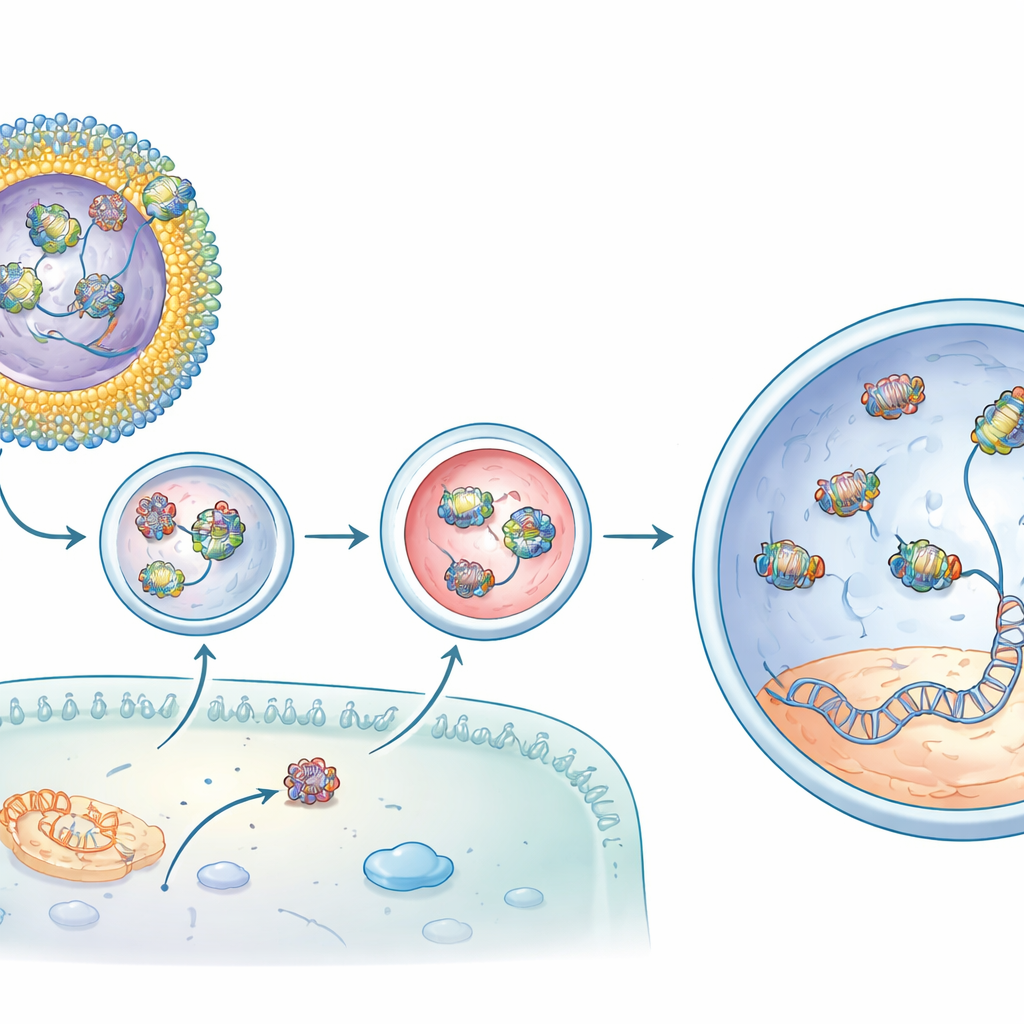
מתיקון מולקולרי לתגובות אור משוחזרות
כאשר ליפוזומים המכילים CBB11 ונושאים את עורך הבסיס הוזרקו מתחת לרשתית של עכברי rd12, התוצאות היו מרשימות. בהשוואה לעריכה שהוזרקה לבדה, הניסוח המותאם הגדיל את התיקון הרצוי בדנ"א בגן היעד ביותר מסדר גודל ואף הניב רמות גבוהות יותר של mRNA מתוקן. ניתוח כימי הראה התאוששות של הפיגמנט הרגיש לאור ברשתית שנעדר במחלה. החלק המרשים ביותר: הקלטות חשמליות מעיניהם של בעלי החיים הראו שתאי ה-rod שלהם החזירו חלק גדול מיכולתם להגיב לאור עמום—עד כשלושה רבעים מהאות של עכבר נורמלי במקרים הטובים. שינויים מחוץ ליעד במקומות אחרים בגנום היו ברמות רקע, מה שמרמז שהעריכה הייתה גם עוצמתית וגם מדויקת.
מה זה עשוי להצביע לגבי טיפולים עתידיים לעיניים
ללא מומחיות, המסר המרכזי הוא שהמחברים בנו "אוטובוס שאטל" רב-שימושי לחלבוני עריכת גנים שפועל ישירות בעין חיה. על ידי קישוט חלקיקים בטוחים הדומים לחיסון בצבע המחזיק חלבון, הם יצרו מערכת שיכולה ללכוד עורכים שונים על פני השטח שלה, להעבירם לתאי הרשתית, לתקן מוטציות הגורמות למחלה, ולהשיב ראייה בעכברים לאחר טיפול חד-פעמי. למרות שנדרש עוד מחקר כדי להעריך במלואו את הבטיחות, לשפר את המיקוד ולהתאים את השיטה לשימוש אנושי, הפלטפורמה הזאת מצביעה לעבר תרופות דיוק חד-פעמיות עתידיות למחלות רשתית תורשתיות ואפשרי גם למצבים גנטיים אחרים שבהם תיקון DNA מקומי ומדויק יכול להכריע בין עיוורון לראייה.
ציטוט: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
מילות מפתח: תרפיה גנטית לרשתית, עריכת בסיסי CRISPR, ליפוזומים, העברת חלבון, עוורון תורשתי