Clear Sky Science · he
מיופיברובלסטים חיוביים ל-tenascin C מחמירים היפרפלזיה ניאו-אינטימלית וסקולרית על ידי הפצת אינטראקציות בין עצבים ומאקרופגים בעכברים
כשכלי דם מתרפאים בדרך הלא נכונה
הליכים שמחזירים את הזרימה לעורקים סתומים, כמו אנגיופלסטיקה וניתוח מעקפים, מצילים חיים רבים. עם זאת, לעתים קרובות הם משאירים בעיה סמויה: עם הזמן, הכלי המטופל עלול להצטלק פנימה, להיצרות חוזרת ולהחזיר את הסיכון למטופלים. המחקר הזה בעכברים חושף שיחה תלת-כיוונית בלתי צפויה בין תאי תמיכה, עצבים ותאי מערכת החיסון בדופן הכלי שמניעה את ההתרפאות המופרזת הזו, ומצביע על מולקולה בשם tenascin C כמטרה מבטיחה לשבור את המעגל.
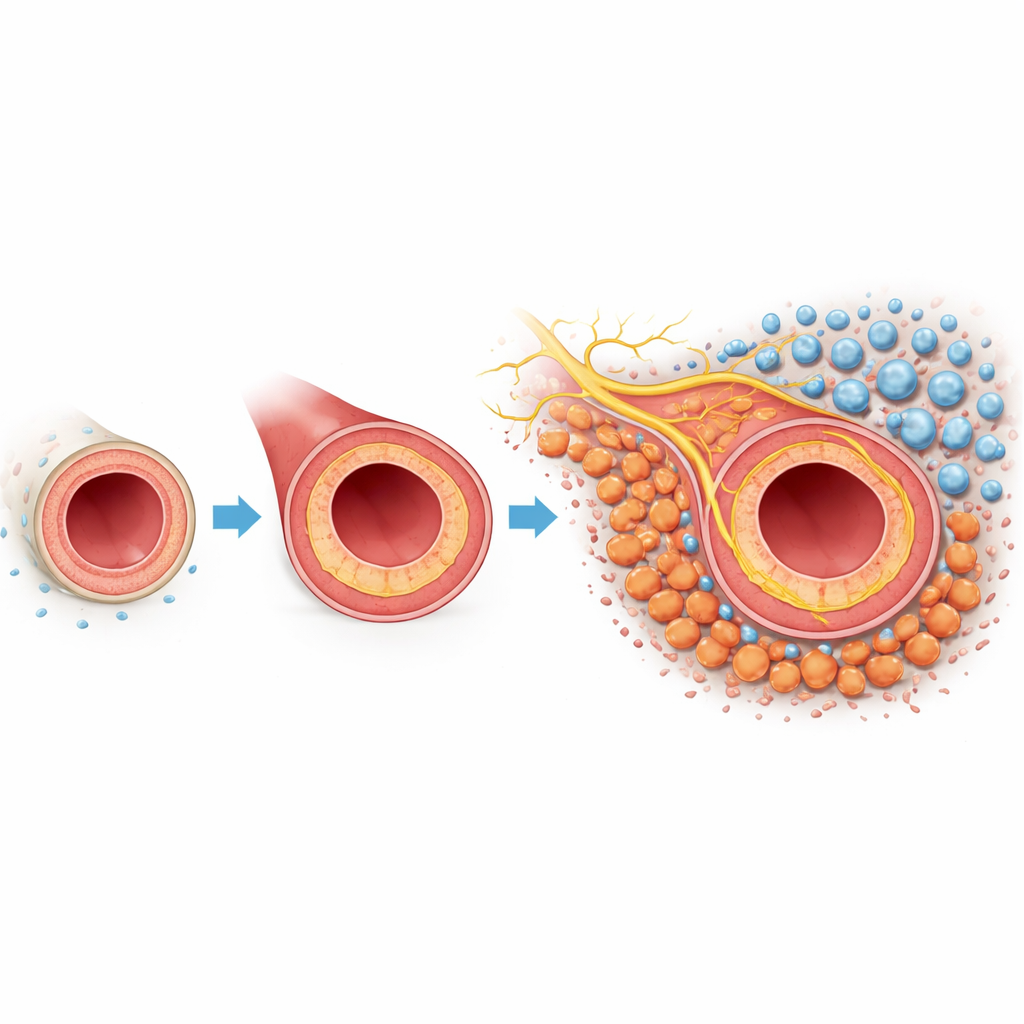
מבט מקרוב על הצלקת הבעייתית בעורקים
כאשר עורק נפגע או ממושך במהלך ניתוח, השכבה הפנימית יכולה לגדול בחזרה בצורה מוגזמת. צמיחה פנימית זו, שנקראת היפרפלזיה ניאו-אינטימלית, מעבה את דופן הכלי ומצמצמת את התעלה שדרכה זורם הדם. השכבה החיצונית של הכלי, האדוונציטיה, מכילה פיברובלסטים — תאי תמיכה ששומרים בדרך כלל על מבנה הכלי. במודל העכבר הזה, שבו עורק הקרוטיד נקשר בחלקו כדי לדמות פגיעה, החוקרים השתמשו בפרופיל גנטי בתא יחיד ובמיפוי מרחבי כדי למיין כל סוג תא משמעותי המעורב. הם מצאו שפיברובלסטים היו בשפע במיוחד ושינו את התנהגותם באופן דרמטי לאחר הפגיעה, מה שמרמז שתאים אלה עשויים להיות שחקנים מרכזיים בתגובה הצלקתית.
עליית תאי tenascin C שיוצרים צלקת
בהעמקה באוכלוסיית הפיברובלסטים גילו הצוות תת-קבוצה מובחנת שהופיעה רק לאחר הפגיעה. תאים אלה נשאו מאפיינים של מיופיברובלסטים — רמות גבוהות של חלבון הכיווץ α-פעולת שריר חלק וסמן נוסף שנקרא פריאוסטין — דבר שמצביע על כך שהחליפו למצב של יצירת צלקת. באופן מפתח, תת-קבוצה זו גם ייצרה כמויות גדולות של tenascin C, חלבון מטריצי שנמצא בדרך כלל בדלילות ברקמות בוגרות בריאות אך שפעיל במחלות ובתיקון רקמות. ניסויים במעבדה הראו שחשיפת פיברובלסטים אדוונציאליים נורמליים ל-transforming growth factor beta או ל-tenascin C נוסף דחפה אותם להפוך לאותם מיופיברובלסטים חיוביים ל-tenascin C. התאים לאחר מכן הפרישו אף יותר tenascin C, ויצרו לולאה מחזקת-עצמית דרך זוג קולטני-מעטפת ספציפי, אינטגרין αvβ1, שהרחיבה באופן מתמשך את האוכלוסייה היוצרת צלקת.
עצבים ותאי חיסון עוקבים אחרי השכונה
הסיפור לא הסתיים ביצירת הצלקת. באמצעות הדמיה תלת-ממדית של כל המקטע וטרנסקריפטומיקה מרחבית, החוקרים מצאו שהמיופיברובלסטים העשירים ב-tenascin C צברו בקלסטרים בקרבת סיבים עצביים נובטים ותאי חיסון הנקראים מאקרופגים בדופן החיצונית של הכלי. עורקים פגועים הציגו עצבים סנסוריים צפופים ומסולסלים ומבנים דמויי סינפסה רבים יותר מהרגיל, הן בעכברים והן במדגמי עורקים אנושיים עם היפרפלזיה ניאו-אינטימלית. מאקרופגים באזורים אלה נשאו חתימת דלקתית, והפרישו מולקולות כגון IL-1β ו-TGF-β1 שיכולות להאיץ עוד את היווצרות הצלקת. יחד, הנתונים ציירו תמונה של מיקרו-סביבה מאורגנת מחדש שבה תאים יוצרי צלקת, עצבים ומאקרופגים מתערבבים פיזית ומשפיעים זה על זה.
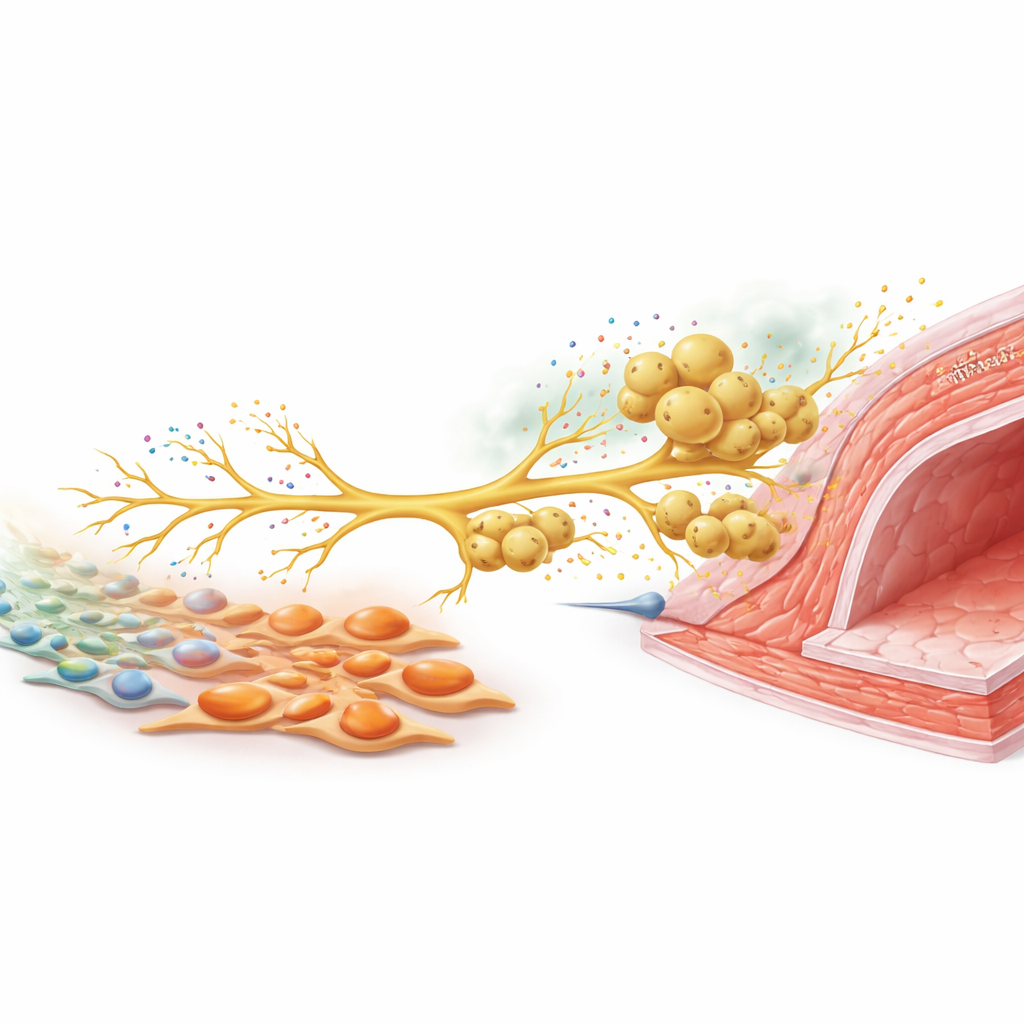
אות עצבי שמזמין מגינים נוספים
כדי להבין כיצד סוגי התאים האלה מתקשרים זה עם זה, הצוות התרכז בעצבים סנסוריים החשים גירויים מזיקים. בתרבית, מיופיברובלסטים עשירים ב-tenascin C הגבירו את הגדילה של סיבי עצב מגנגליוני שורש גבי. בעכברים פגועים, הנוירונים הסנסוריים הללו הגדילו את הייצור של CCL2, אות כימי הידוע כמדלל מאקרופגים. כאשר נוירונים ומאקרופגים גודלו יחד, מאקרופגים נדדו לאורך סיבי העצב הגדלים, בדומה למה שראו סביב עורקים בבע"ח. השתקת CCL2 בנוירונים הקטינה באופן דרמטי את הגיוס של מאקרופגים. בבעלי חיים, צמצום פעילות עצב סנסורי באמצעות רעלת עצבים, או מחיקה סלקטיבית של tenascin C רק בפיברובלסטים, שניהם הפחיתו את צפיפות העצבים, רמות CCL2, הצטברות מאקרופגים ולבסוף את העיבוי של דופן הכלי. שילוב שתי ההתערבויות לא הוסיפו יתרון ניכר, מה שמרמז שהן פועלות באותו מסלול.
מדוע המסלול החדש הזה חשוב
במבט כולל, הממצאים חושפים מעגל אכזרי: פגיעה דוחפת פיברובלסטים להפוך למיופיברובלסטים המייצרים tenascin C; תאים אלה מעצבים מחדש את המטריקס ומגרים עצבים סנסוריים; עצבים פעילים משחררים CCL2, שמושך מאקרופגים; והמאקרופגים מפרישים גורמי דלקת ופיברוזה שמחריפים את הצלקת ומצמצמים את העורק. על ידי זיהוי tenascin C והציר העצב–מאקרופג כמניעים מרכזיים של הלולאה הזו, העבודה מציעה שטיפולים המכוונים מולקולה זו או שותפיה ברמז יכולו לעזור לשמור על פתיחות העורקים שתוקנו לאורך זמן רב יותר, ולספק למטופלים הגנה עמידה יותר לאחר פרוצדורות קרדיו־וסקולריות.
ציטוט: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
מילות מפתח: היפרפלזיה ניאו-אינטימלית, tenascin C, עיצוב מחדש של כלי דם, עצבים סנסוריים, דלקת מאקרופגים