Clear Sky Science · he
שימוש אמין מחדש באינטראקטום הנוגדנים בתוך התא
הפיכת נוגדנים לכלים זעירים בתוך התאים שלנו
נוגדנים מוכרים כנשקים מדויקים בזרם הדם, המתמקדים בנגיפים ובאיומים אחרים. אך רוב הפעולה ברבות ממחלות, כולל אלצהיימר, פרקינסון וחלק מהסוגים של סרטן, מתרחשת בתוך התאים, שם נוגדנים רגילים לעתים נדירות מגיעים או פועלים ביעילות. המחקר הזה מראה כיצד לבנות מחדש שיטתי נוגדנים קיימים ל"אינטראבודים" קטנים שמיועדים לפעול באופן מהימן בתוך תאים חיים של בני אדם, ופותח אפשרות לאבחון חדש, כלים מחקריים ואולי בעתיד טיפולים שפועלים ישירות בלב תהליכי המחלה.
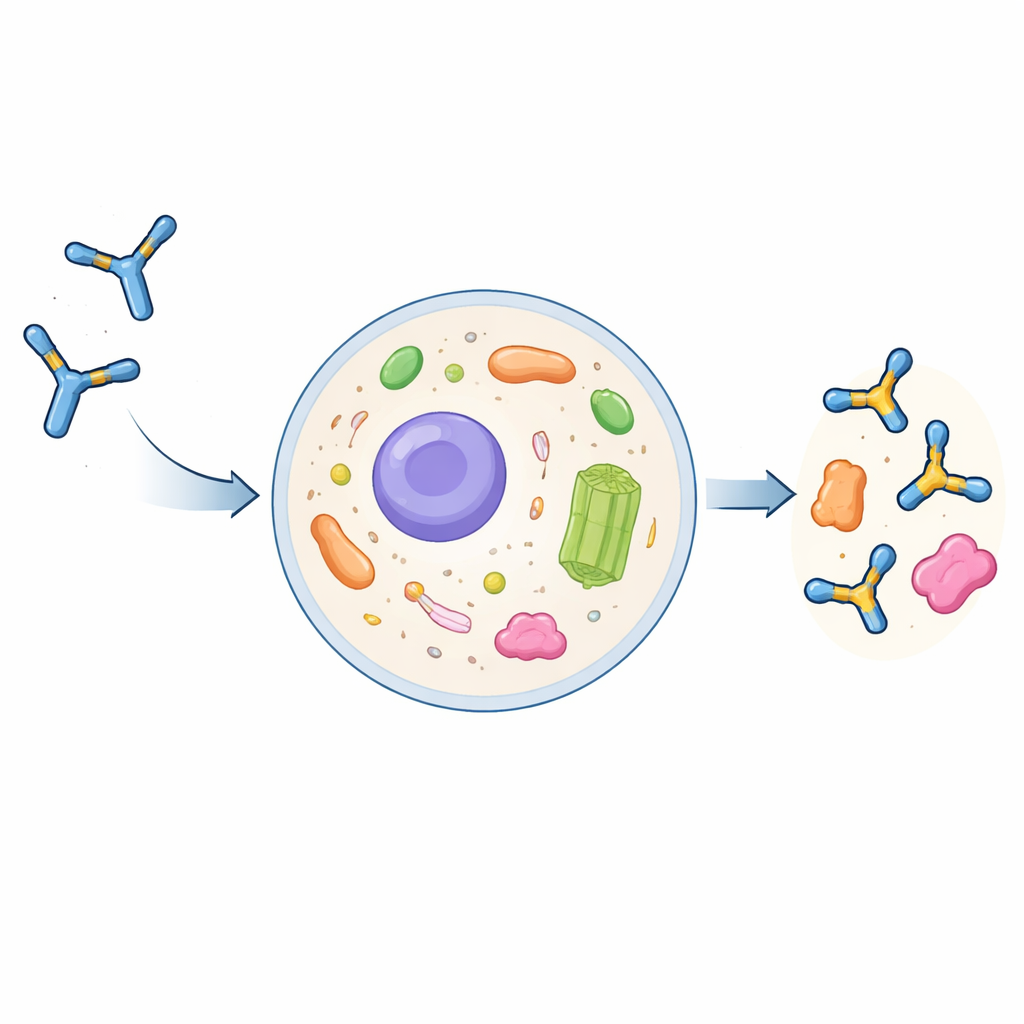
מדוע נוגדנים רגילים מתקשים בתוך התאים
נוגדנים בגודל מלא הם חלבונים גדולים בצורת Y שהתפתחו לפעול מחוץ לתאים. הם מורכבים ומעובדים כימית במסלול ההפרשה של התא ואז משתחררים לדם. אם הם נספגים חזרה לתאים, הם בדרך כלל מסתיימים במחלקות פירוק במקום בנוזל הפנימי של התא, הציטופלזמה. מדענים יכולים לקצץ נוגדנים לחלקי ההכרה החיוניים שלהם, הנקראים שברי משתנה בשרשרת יחידה (scFvs), ולהביע אותם כאינטראבודים בתוך תאים. עם זאת, אינטראבודים אלה לעתים מתגבשם, הופכים לבלתי מסיסים ומאבדים את יכולת הקשירה שלהם למטרות. עד כה לא הייתה מתודולוגיה כללית ומהימנה להפוך נוגדן קונבנציונלי לאינטראבוד מתנהג היטב.
ממצאים לגבי כללי העיצוב לאינטראבודים מסיסים
החוקרים התחילו במדידת מידת המסיסות של 45 אינטראבודים שונים כשהם מיוצרים בתאים אנושיים. הם השוו בצורה שיטתית תכונות חלבון רבות — כגון הידרופוביות כוללת, איכות מבנה חזויה ותכונות לולאות הקשירה — כדי לראות אילו מהן מסבירות בצורה הטובה ביותר האם אינטראבוד נשאר מסיס. גורם פשוט אחד בלט: המטען החשמלי הכולל סביב pH קרוב לפיזיולוגי. אינטראבודים עם מטען נקי שלילי חזק היו בעלי סבירות גבוהה יותר להישאר מסיסים, בעוד אלה עם מטען ניטרלי או חיובי נטו להתגבש. מנבאים מתוחכמים אחרים, כולל ציוני ביטחון מבניים ממערכת AlphaFold, לא הראו קורלציה עם המסיסות. הדבר איפשר לצוות לבנות מודל פרקטי המבוסס על מטען שיכול להעריך כמה מהאינטראבוד יימצא בחלק המסיס של תמצית התא.
שינוי קישורים ודומיינים לשיפור ההתנהגות
מצוידים בתובנה זו, הצוות התרכז בתכונות שניתן לכוונן בקלות מבלי לשבש את האופן שבו האינטראבוד מזהה את מטרתו. אלמנט מרכזי הוא הפפטיד הקצר "קישור" שמחבר בין שני הדומיינים המשתנים. ברוב העיצובים הקיימים משתמשים בקישורים ניטרליים שאינם משנים את המטען. על ידי החלפה של חומצות אמינו טעונות שלילית במקומות אלו, החוקרים יכלו להוריד את המטען הכולל של האינטראבוד, ולשפר באופן דרמטי את המסיסות תוך שמירה על קשירת המטרה. הם גם גילו שסדר הדומיינים המשתנים (האם החלק הכבד או הקל בא קודם) ומיקומים מסוימים במסגרת מחוץ ללולאות הקשירה משפיעים על קלות הקיפול והיכולת להישאר מסיסים. בחירה בסדר דומיינים שמגן על אזורים שפיציים והכנסת מוטציות להחלפת מטען במקומות מתוכננים שיפרו עוד יותר את הביצועים.
שימוש בבינה מלאכותית לבניית אינטראבודים בקנה מידה גדול
כדי לצאת מהניסיון של אחד־אחד, המחברים שילבו את כללי המטען הפשוטים שלהם עם תוכנות עיצוב חלבון מתקדמות המבוססות על למידת עומק. בהתבסס על גבישי נוגדן ידועים, הם השתמשו בגישת "קיפול הפוך" כדי להציע רצפים חדשים שעדיין יאמצו את הצורה הרצויה אך יישאו תכונות פני שטח — בעיקר תבניות מטען — המעדיפות יציבות ומסיסות. הם הגבילו שינויים בלולאות הקישור העיקריות כדי לשמר הכרה, ואפשרו לאלגוריתם לעצב מחדש את המשטחים הסובבים. בדיקות הראו שרבים מהאינטראבודים המונחים על ידי ה‑AI היו לא רק מסיסים מאוד אלא גם יציבים תרמית יותר מווריאנטים שתוכננו על ידי בני אדם, ושמרו על היכולת לקשור מטרות רלוונטיות למחלות כמו SOD1 מפוצל, p53, α‑synuclein וחלבונים אחרים הקשורים בניורודגנרציה.
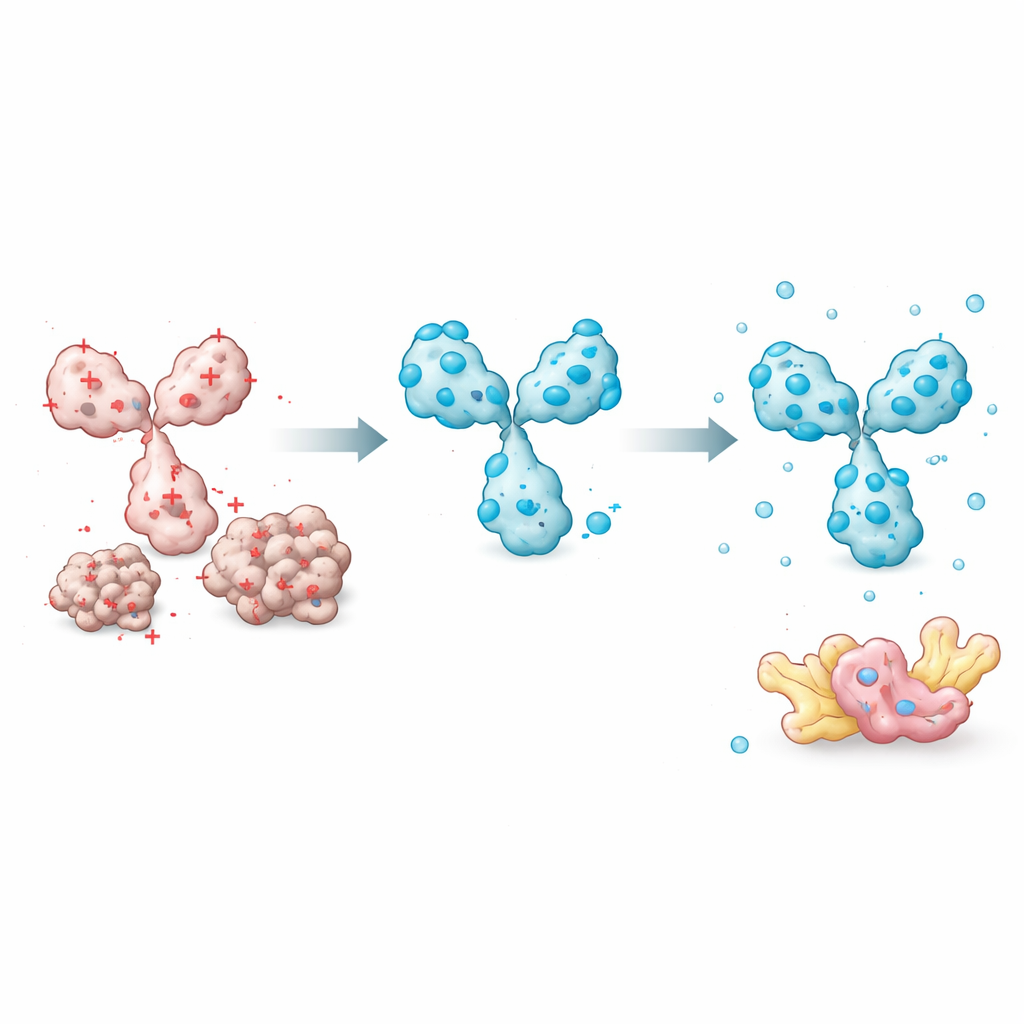
בניית ספרייה של "תופסי חלבון" בתוך התא
בהפעלת הכללים והכלים האלה בקנה מידה גדול, הצוות עיצב חישובית 672 נוגדנים מחדש כאינטראבודים החזוים לפעול היטב בתוך תאים. המולקולות המהונדסות הללו מכסות יותר מ‑60 מטרות תוך‑תאיות שונות, כולל חלבונים המעורבים במחלות אלצהיימר, פרקינסון והנטינגטון, כמו גם גורמים הקשורים לסרטן ושינויים לאחר תרגום כמו זרחון ואצטילציה. בניסויים, אינטראבודים שנבחרו הצליחו לתפוס צורות חלבון ספציפיות הקשורות למחלות, כגון SOD1 מוטנטי או צורות מסוימות של α‑synuclein, תוך התעלמות מהגרסאות הנורמליות. כל הרצפים שוחררו באופן פתוח, והמחברים מספקים כלי אינטרנט שמאפשר לאחרים להעריך את מסיסות האינטראבוד מתוך רצף באמצעות אותו מודל מבוסס‑מטען.
מה זה אומר עבור תרופות ומחקר עתידי
מבחינה מעשית, עבודה זו הופכת את אוסף הנוגדנים הקיים העצום — רבים מהם כבר נחקרו בבתי חולים — לכלי שניתן להתאים באופן אמין לשימוש בתוך תאים. על ידי ביצוע סדרה פשוטה של כללי עיצוב, חוקרים יכולים כעת ליצור אינטראבודים שסביר שיעבדו בניסיון הראשון, ובכך לחסוך זמן ועלות. עבור הקוראים הכלליים, המסר המרכזי הוא שמדענים מצאו דרך פשוטה "לרתום" את גלאי החלבון הטובים ביותר שלנו כך שיעבדו במרחב הצפוף של תאים חיים, שם רבות מהמחלות מתחילות. הדבר עשוי לזרז פיתוח של דרכים חדשות לעקוב, לחקור ולבסוף לטפל במצבים המונעים על‑ידי חלבונים מקופלים או בלתי תקינים.
ציטוט: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
מילות מפתח: אינטראבodies, הנדסת נוגדנים, מסיסות חלבון, מחלות ניווניות עצביות, בינה מלאכותית בביולוגיה