Clear Sky Science · he
ריצוף RNA כפול ב־vivo חושף אפקטורים מרכזיים בשיבוש מחסום האפיתל על ידי פתוגן חיצוני
איך חלק מהחיידקים חולפים על פני גדרות התאים שלנו
האיברים שלנו מצופים בתאים הדוקים שמפעלים כקירות, ושומרים על הדם, המיקרובים והרעלנים במקום המתאים להם. עם זאת, חיידקים מסוימים עדיין מחליקים בין תאים אלה ומתפשטים בגוף. המאמר הזה מגלה בפרטי פרטים כיצד החיידק הגורם ללבפטוספירוזה, מחלה עולמית קשה, מגיע באופן שקט לאיברים כמו הכבד והכליות, ואז משתמש במניפולציה מתוחכמת של הסידן בתוך התאים שלנו כדי לפתוח את המחסומים המגינים הללו.
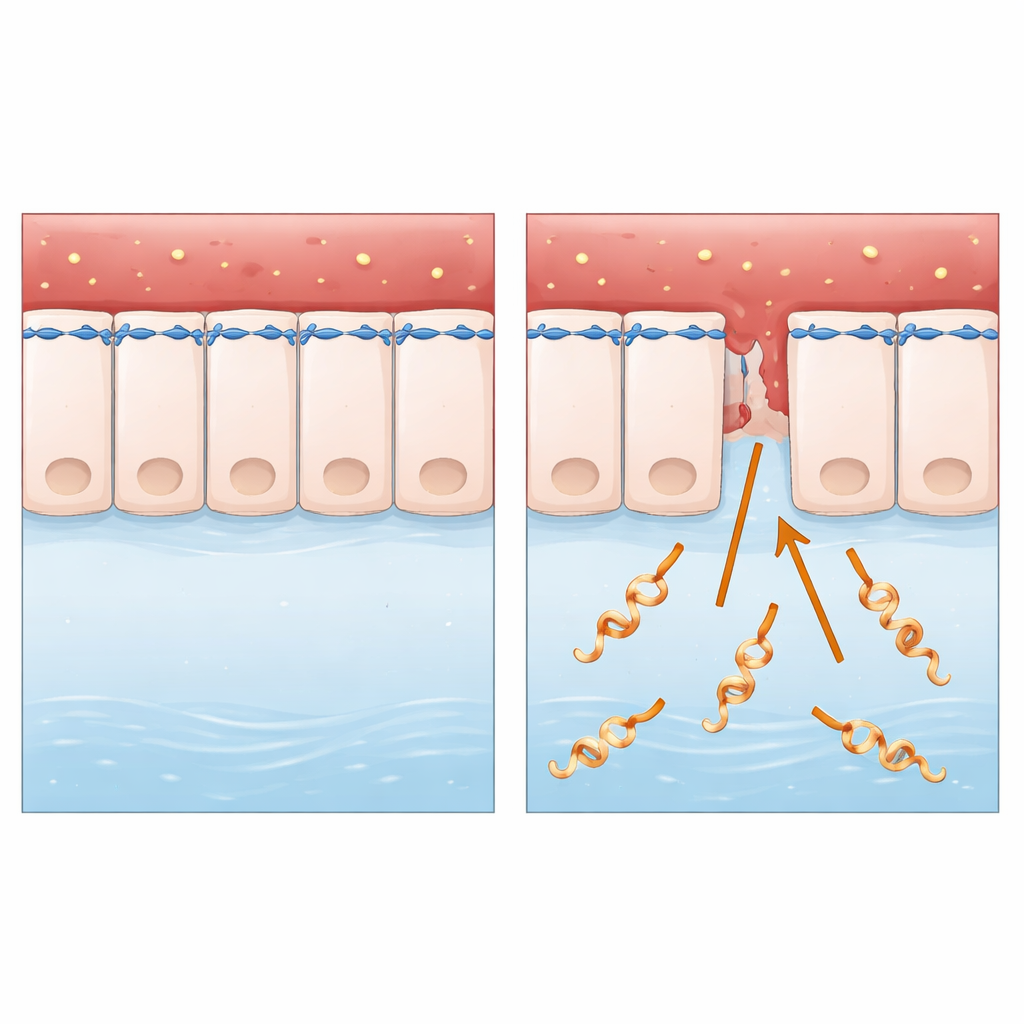
פולש שקט לרקמות בעלי חיים ובני אדם
המחקר מתמקד ב־Leptospira interrogans, חיידק בצורת סליל שמועבר בעיקר מבעלי חיים לאדם דרך מים או אדמה מזוהמים. לאחר כניסה דרך פגיעות עור זעירות או ריריות, הוא נוסע במחזור הדם ועלול לגרום למחלה קשה, כולל כשל כבד וכליות ודימומים פנימיים. בשונה מהרבה מיקרובים שנחקרו היטב, Leptospira חי מחוץ לתאים וחסר חלק מ"הנשקים המולקולריים" הקלאסיים שהמדענים בדרך כלל מחפשים. זה הפך אותו למקן מבחן אידיאלי לשאלה בסיסית: איך חיידק פשוט לכאורה, החי מחוץ לתאים, חוצה שכבות תאים שלמות ביעילות כזו?
צפייה בשיח הגנים של המארח והפתוגן בו‑זמנית
כדי ללכוד את תהליך ההדבקה בתוך בעל חיים חי, הצוות השתמש בריצוף RNA כפול (dual RNA‑Seq) בחמוסים, מודל ללבפטוספירוזה חריפה. שיטה זו קוראת אילו גנים מופעלים או מדוכאים הן במארח והן בפתוגן בו־זמנית. המדענים הדביקו חמוסים ואספו דגימות כבד וכליה יום אחד ושלושה ימים לאחר מכן. בשלבים המוקדמים, למרות כמות גבוהה של חיידקים, פעילות הגנים של התאים כמעט שלא השתנתה, מה שמרמז ש‑Leptospira בתחילה מחליקה מתחת לרדאר של המערכת החיסונית. עם זאת, ביום השלישי שני האיברים הראו תגובה חזקה, ובעיקר הכבד: גנים שמעורבים בדלקת, בקשרים בין‑תאיים ובשלד הפנימי של התאים השתנו בחדות, דבר שמצביע על עיצוב פעיל של מחסומי הרקמה.
שבירת רוכסן התאים מהחוץ פנימה
שכבות תאים ננעלות על‑ידי צמתי הדוקות וצמתי הדבקה, שמקשרות בין תאים סמוכים ומעגנות אותם לטבעת של אקטין ומיוזין — אותו זוג חלבונים שעוזר לשרירים להתכווץ. מיקרוסקופיה של תאים אפיתליאליים אנושיים שהודבקו ב‑Leptospira הראתה ששמם השתנה, נפתחו מרווחים בין התאים וחלבוני צומת מרכזיים נחלשו או הוזזו ממקומם. חשוב לציין שהתאים לא מתו, מה שאומר שהמחסום פורק ולא נהרס לחלוטין. החוקרים גם הבחינו בסימני לחץ במפעלים לקיפול חלבונים בתאים, אך חסימת הלחץ הזה לא החזירה את הצמטים לעמדם, מה שהוביל אותם לחשוד באשם אחר.
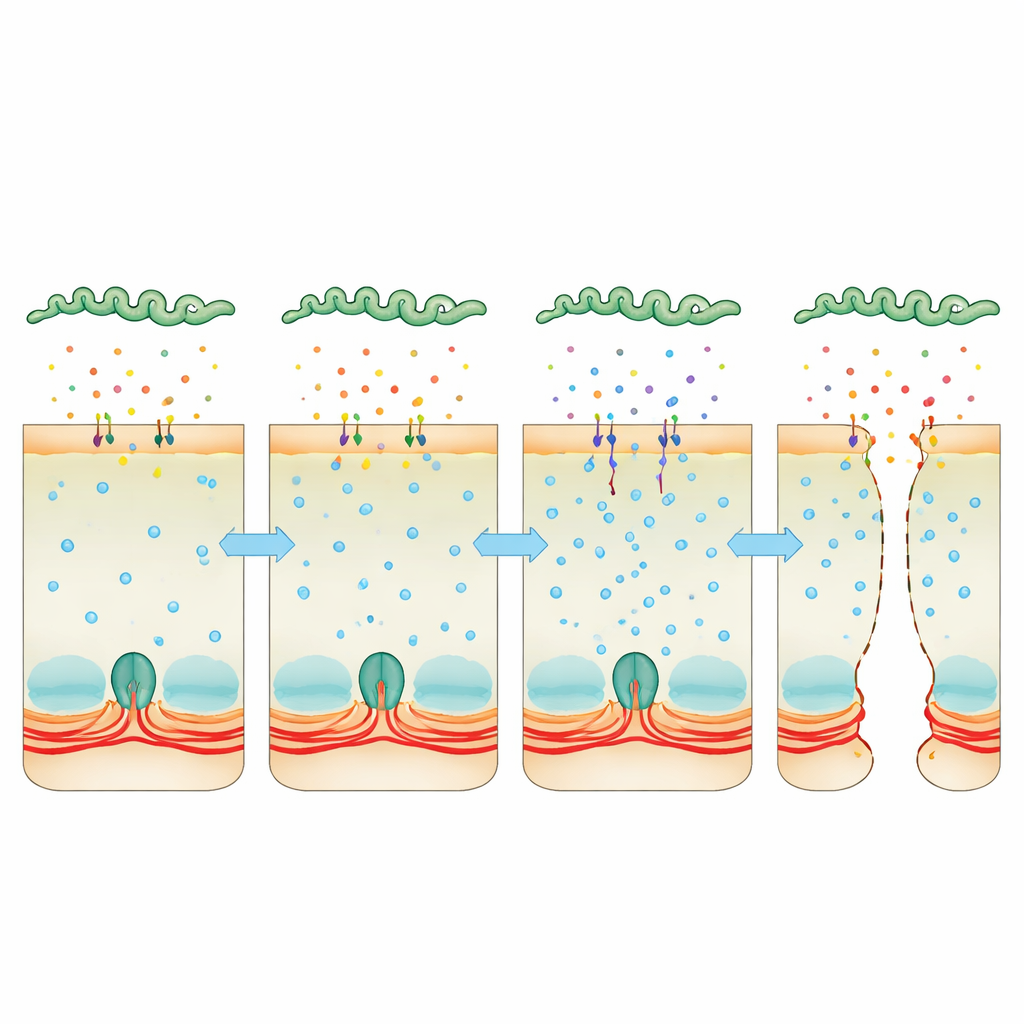
חטיפת הסידן כמפרץ סמוי
הקשב הופנה לסידן, אות אוניברסלי בתוך התאים שיכול להדק או להרפות את טבעת האקטין–מיוזין. תאים מודבקים צברו יותר סידן, וזה קושר לפעילות מוגברת של קינאזת השרשרת הקלה של מיוזין (myosin light chain kinase), אנזים שגורם לטבעת הכיווצית למשוך על הצמתים. כאשר הצוות השתמש בחומר שמקנן סידן, או בתרופות המעכבות קאלמודולין או את הקינאז הזה, שכבות התאים נותרו שלמות יותר והחיידקים התקשו לחמוק דרכן. במקביל, ריצוף עמוק של RNA חיידקי חשף שבתוך המארח Leptospira מעלה בעוצמה את ייצורם של שני חלבונים "משני אלימות" (Virulence‑Modifying) המזכירים רעלנים. חלבונים אלה מופרשים לסביבה, נקשרים לתאי המארח ונמצאים בתוכם. כאשר חיידקים חסרו אחד או גם שני חלבונים אלה, הם היו פחות מסוגלים לחצות שכבות תאים או לגרום למחלה קטלנית, והמרק החוץ‑תאי שהם הפרישו כבר לא העלה רמות סידן או פירק צמטים ביעילות כבעבר.
ממצאים משמעותיים למחלה ולהגנות עתידיות
במכלול, הממצאים מספרים סיפור ברור. אחרי כניסה לגוף כמעט ללא הד, Leptospira מתחילה להפריש חלבוני משני‑אלימות דמויי רעלן. חלבונים אלה נקשרים לתאי אפיתל ומפריעים לאיזון הסידן בתוכם, מה שמדליק מסלול כיווצי שמושך ומפרק את "הרוכסן" התאי שקושר בין התאים השכנים. כאשר הצמתי ההדוק וההדבקה מרפים, מופיעים מרווחים מיקרוסקופיים שמאפשרים לחיידקים לעבור בין התאים, להתיישב באיברים ולגרום למחלה קשה. על ידי זיהוי המנגנון המונע על ידי סידן והחלבונים החיידקיים האחראים לו, המחקר פותח נתיב לאסטרטגיות חדשות — כגון חסימת חלבונים אלה או נתיב האותות שלהם — לחיזוק ה"גדרות" התאית שלנו ולהגבלת התפשטות הלבטוספירוזה ואולי זיהומים אחרים המנצלים שיטות דומות.
ציטוט: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
מילות מפתח: לבפטוספירוזה, מחסום אפיתלי, אותות סידן, רעלני חיידקים, אינטראקציות מארח–פתוגן