Clear Sky Science · he
nDIA-MS משופר באמצעות סופרצ׳ארג׳ינג מאפשר פרופיל גלובלי של שינויים בסולוביליות הפרוטאום המושרים על ידי תרופות
מדוע התנהגות חלבונים חשובה מעבר למספרים הנקיים
תרופות יכולות לשנות לא רק כמה חלבון תא מייצר, אלא גם לאן החלבון נודד והאם הוא חופשי או נצמד למבנים תאיים. שינויים אלו ב"איפה" ו"איך" החלבונים קיימים בתא נקשרים באופן הדוק למחלות כמו סרטן ומחלות ניווניות, אך קשה למדודם בקנה מידה רחב. המחקר הזה מציג שיטה מהירה ועוצמתית לסרוק אלפי חלבונים אנושיים במקביל כדי לראות כיצד הסולוביליות שלהם — האם הם במצב חופשי או במצב נצמד יותר — משתנה כאשר התאים נחשפים לשתי תרופות ניסיוניות נפוצות.
דרך מהירה וחדה יותר להסתכל על חלבונים
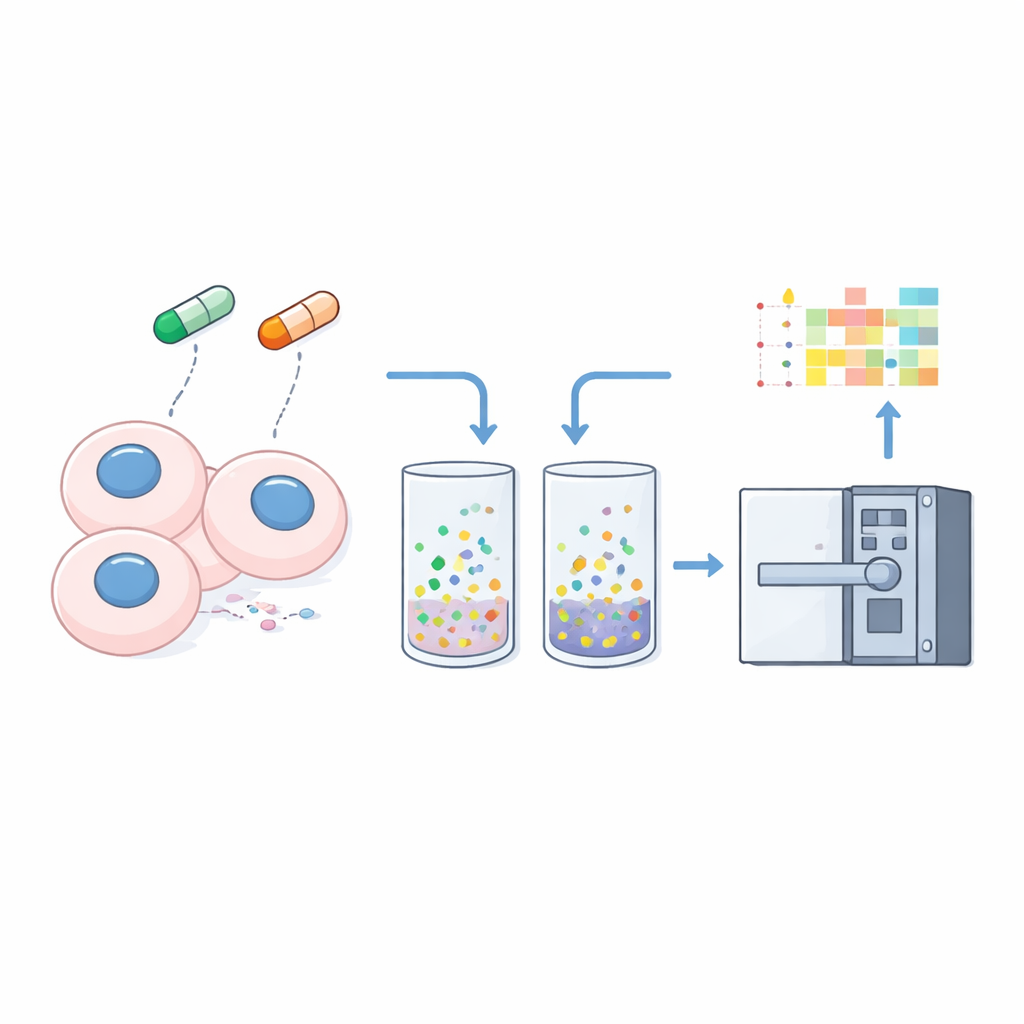
המחברים בונים על טכנולוגיה מרכזית בביולוגיה מודרנית: ספקטרומטריית מסה, טכניקה ששוקלת ומספירה שברי חלבון. שיטות סטנדרטיות כבר מצטיינות בליידע אותנו כמה מכל חלבון נוכח, אך מתקשות לגלות שינויים במצב החלבון, כמו היקשרות ל־DNA או כניסה לאסמבליות צפופות. כאן החוקרים מחדדים גרסה של ספקטרומטריית מסה הנקראת narrow-window data-independent acquisition (nDIA-MS). באמצעות הוספת מסייעים כימיים קטנים, שנקראים סופרצ׳ארג׳ינג ריאגנטים, לנוזל הנושא את הפפטידים במכשיר, הם מגבירים את המטענים החשמליים על השברים ומעצימים משמעותית את האות.
לאחר בדיקה של שני תוספים סופרצ׳ארג׳ינג נפוצים, דימטיל סולפוקסיד (DMSO) ו‑m‑ניטרובלנזיל אלכוהול (mNBA), הם מוצאים ש־3% DMSO נותן את עליית האות הכוללת הגדולה ביותר ואת מספר החלבונים הגבוה ביותר שזוהו, בעוד mNBA עדיף בהגברת מספר ומטען של שברי פפטידים בודדים. עם התצורה המותאמת, הצוות יכול לזהות כ־9,600 חלבונים אנושיים מתוך מיקרוגרם אחד של עיכול תאי סטנדרטי בהרצה של 15 דקות — שילוב מרשים של מהירות ועומק לניסויים שגרתיים. הביצועים הללו פותחים את הדרך לשימוש ב‑nDIA-MS לא רק לספירת חלבונים, אלא גם לחקירת האופן שבו מצבם הפיזי מגיב ללחץ.
הפיכת הסולוביליות למדד לשינוי בתא
כדי להפוך את הסולוביליות לאות מדיד, החוקרים מטפלים בתאים בעדינות עם דטרגנט עדין שמחלץ חלבונים הניתנים להמסה חופשית, ומשאיר חומר שנקשר בחוזקה ל־DNA, ממברנות או מבנים אחרים. הם מנתחים גם את הלקט הכולל של התא וגם את הגרגיר ה"לא־מסיס" הזה משלוש שורות תאי סרטן באמצעות שיטת nDIA-MS המותאמת. על ידי השוואת השפע של כל חלבון בגרגיר יחסית לדגימת הלקט הכולל, הם מחשבים "יחס אי־מסיסות" פשוט — ערכים גבוהים מצביעים על היקשרות חזקה יותר למבנים תאיים, ערכים נמוכים מרמזים על מצב יותר מסיס וחופשי.
הצוות חשף לאחר מכן את התאים למשך שעה בלבד לשתי תרופות: MG132, חוסם פרוטאזום שמונע מהתאים לפרק חלבונים בלתי רצויים, ו‑ML‑792, מעכב הפעלת SUMO שמפריע למערכת תיוג חלבונים מרכזית. חשיפה קצרה זו מכוונת במכוון; היא שואפת ללכוד שינויים מהירים וראשוניים בהתנהגות החלבונים לפני ששינויים בביטוי גנים התפתחו במלואם. גם בחלון זמן זה הם יכולים לכמת שינויים בסולוביליות ובשפע עבור 8,694 חלבונים ולאשר שהפרקציה שלהם מפרידה באופן נקי חלבונים מסיסים קלאסיים, כמו טובולין, מחלבונים הקשורים לקרומטין, כמו היסטונים.
תרופות שמעצבנות את הנוף החלבוני של התא
MG132 ו‑ML‑792 מייצרות עיבוד נרחב אך מובחן של סולוביליות חלבונים. MG132 הופך יותר מאלף חלבונים לפחות מסיסים ויותר מ־600 לחלבונים מסיסים יותר across שלוש שורות התאים. חלבונים רבים מושפעים נמצאים בצמתים של בקרת איכות חלבון, תגובת נזק לדנ״א, ויסות גנים ואוטופגיה — מערכת הניקוי העצמית של התא. לדוגמה, מרכיבים של קומפלקס פעיל הפרוטאזום ומתאמים שעוזרים לתייג חלבונים פגומים הופכים לפחות מסיסים, מה שמעיד שכאשר הפרוק נחסם, גורמי בקרת איכות מרכזיים עצמם נלכדים על מבנים כגון קרומטין או ממברנות תאים. חלבוני אוטופגיה ושחקני תגובת נזק, כולל ביקר הלחץ HSF1, גם הם נעים לכיוון מצבים פחות מסיסים בדומה לעיבוי/קונדנסציה, בהתאמה להיווצרות גופים גרעיניים של לחץ.
לעומת זאת, ML‑792 מכוון בעוצמה לחלבונים שמעורבים בתעתוק ובמערכת SUMO עצמה. מאות חלבונים הופכים או ליותר לא־מסיסים או ליותר מסיסים כאשר הפעלת SUMO נחסמת, וחלבוני SUMO ליבות עוברים לבריכת החלבונים המסיסים, כפי שמצופה. המחקר מדגיש התנהגויות בולטות: תת־יחידות של RNA פולימראז III נעשות פחות מסיסות, מה שמרמז על שינוי ביבוא גרעיני או בהיקשרות לקרומטין; מדכאים מרכזיים המקושרים לגופים גרעיניים, כגון SP100 ו‑DAXX, הופכים למסיסים יותר, מצביע על כך שסימוני SUMO מסייעים לשמור אותם מבודדים במחיצות אלו. כאשר שתי התרופות מוחלות לבדן או ברצף, חלק מהחלבונים, כולל NAB2, SMAD2 ו‑RB1, מראים שינויים מסולוביליות מתואמים או אף מנוגדים, וחושפים משחק עדין בין מערכות תיוג האוביקוויטין ו־SUMO בשליטה על תיוג מקומי של חלבונים.
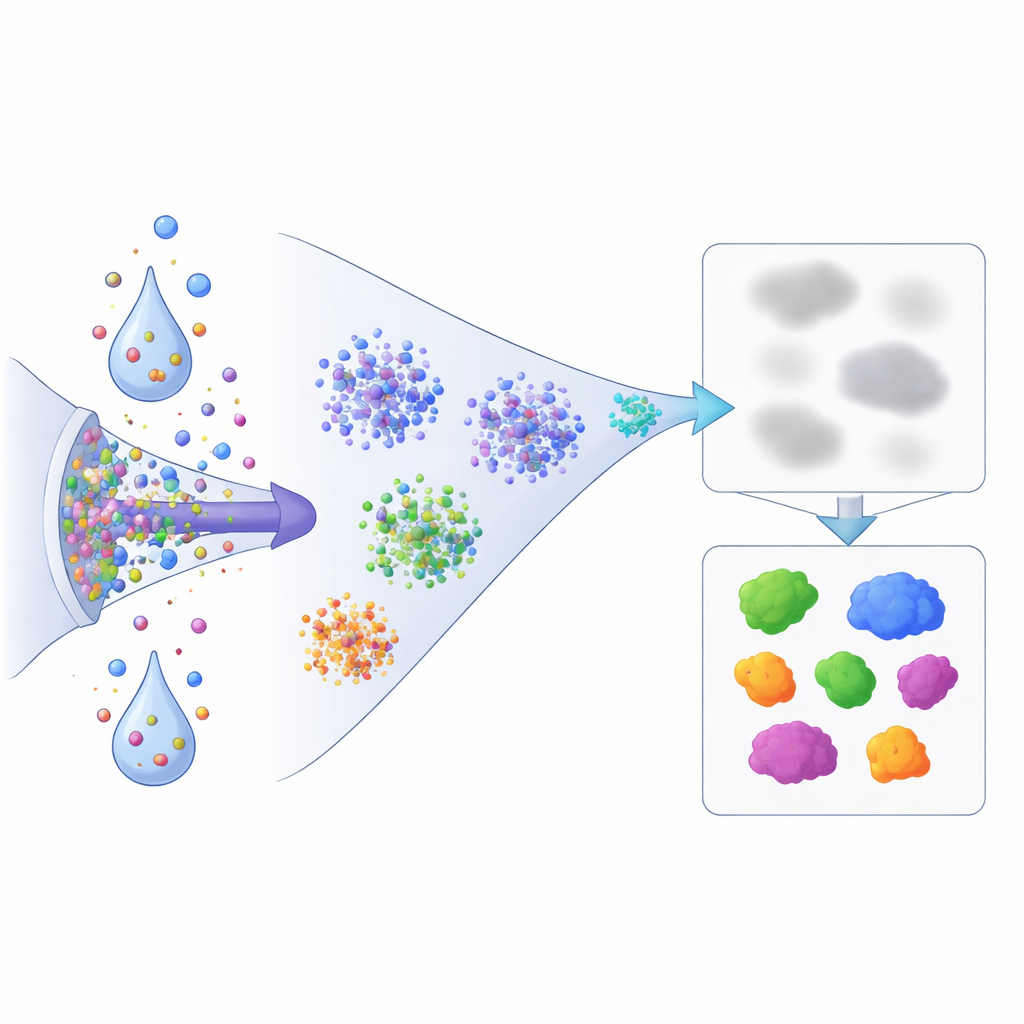
מה המשמעות לכך עבור גילוי תרופות עתידי
למי שאינו מומחה, המסר המרכזי הוא שחלבונים אינם רק עולים או יורדים בכמות כשהתאים נלחצים או מטופלים בתרופות; הם גם נעים, מתעבים ומשנים עד כמה בחוזקה הם קשורים למבנים תאיים. עבודה זו מספקת דרך מהירה וברחבי הפרוטאום לצפות בשינויים אלה. בשילוב של עבודת ספקטרומטריית מסה מותאמת והשוואה פשוטה בין מסיס ללא־מסיס, המחברים מראים כי תרופות ניסיוניות נפוצות מארגנות מחדש במהירות את הנוף הפנימי של החלבונים באופן שמדידות שפע סטנדרטיות היו מפספסות. הגישה פותחת דלת למיפוי כיצד תרופות מועמדות מעצבות מצבי חלבון בכל חלקי התא, ועוזרת לחוקרים לגלות מטרות בלתי צפויות, מסלולי לחץ ונקודות כשל שעשויים להיות מכריעים להבנת אפקט תרפי וטקסיות.
ציטוט: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
מילות מפתח: סולוביליות הפרוטאום, ספקטרומטריית מסה, חוסם הפרוטאזום MG132, מעכב SUMOylation ML-792, מעברים במצב החלבון