Clear Sky Science · he
המטריצה החוץ־תאית מתווכת צבירת תאי הגידול הנשאפים במחזור הדם במטסטזיס של סרטן השד טריפל־נגטיבי
איך תאי סרטן השד הפרועים מצטרפים בצורת שיירות בזרם הדם
כשסרטן השד מתפשט, לרוב זה קורה משום שתאים רופפים של הגידול בורחים לכלי הדם ונוחתים כגידולים באיברים מרוחקים. המחקר הזה שואל שאלה לכאורה פשוטה עם השלכות גדולות: איך התאים האלימים ביותר של סרטן השד, שאיבדו את ה"וולקרו" הטיפוסי שלהם להידבקות זה לזה, מצליחים עדיין לנוע בצברים הדוקים — ומדוע זה הופך אותם למסוכנים כל כך?
ציפוי סוכרי דביק שמחליף את הדבק התאי הקלאסי
המחברים מתמקדים בסרטן השד טריפל־נגטיבי (TNBC), צורה אגרסיבית במיוחד של מחלה שלרוב משליכה לתוך הדם תאי גידול נישאים (CTCs). בצורות רבות של סרטן, צברי CTCs נוטים יותר ליצור גרורות מאשר תאים בודדים. בדרך כלל, צברים כאלה מוחזקים יחד על ידי צמתי הידבקות אפיתליאליים — קומפלקסים חלבוניים מיוחדים שפועלים כריבטים מולקולריים בין תאים שכנים. אך תאי TNBC לעתים קרובות מאבדים חלבונים אלה, מה שיוצר פרדוקס: ללא הדבק הרגיל, מה שומר על הצברים של אלה? באמצעות כרייה של מאגרי גנים גדולים של סרטן, החוקרים גילו כי גידולי TNBC מועשרים בגנים המעורבים בשלד החיצוני של התאים, המכונה המטריצה החוץ־תאית. גן בולט, HAS2, מקודד לאנזים המייצר היאלורונאן (HA), פולימר סוכרי ארוך שמצפה תאים. רמות גבוהות של HAS2 ו‑HA נקשרו בעוצמה למאפיינים אגרסיביים ומטסטטיים של הגידול.
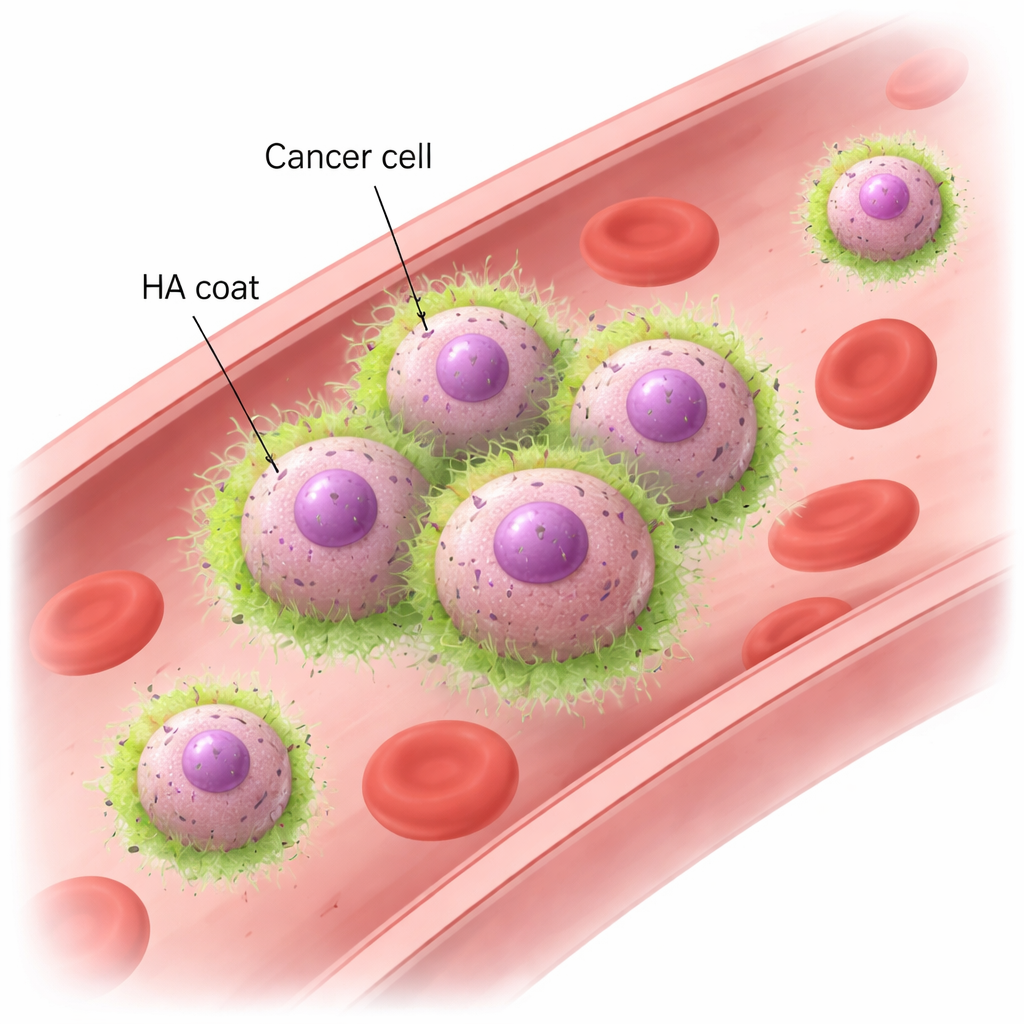
היאלורונאן ו‑CD44: דרך חדשה שתאים אוחזים ידיים
באמצעות דגמי עכבר וקווי תאים של סרטן השד האנושי, הקבוצה הראתה שתאי TNBC מטסטטיים יוצרים במהירות צברים כאשר נחשפים לזרימה מסתובבת המדמה זרימת דם. צברים אלה נשארים שלמים גם תחת כוחות דומים לאלו בכלי דם אמיתיים, בעוד שתאי סרטן פחות אגרסיביים מתפרקים ונעים כיחידים. במיקרוסקופ נצפו התאים המטסטטיים עטופים ב"מעיל" HA, שמתרכז בדיוק במקום שבו התאים נוגעים זה בזה. הסרה של HA באמצעות אנזימים, או השתקת HAS2, השביתה את יכולת הצבירה תחת זרימה, אף שקבוצות התאים יכלו עדיין לשקוע יחד כאשר הושארו ללא הפרעה. השותף המרכזי בצד התא הוא CD44, קולט תאי נפוץ הקושר HA. תאים חסרי CD44 לא יכלו לשמור HA על משטחם או ליצור צברים. להיפך, תאים שאינם נוטים לצבור ובהם הונדסו כדי להפיק גם HAS2 וגם CD44 רכשו יכולת חזקה ליצור צברים. ניסויים אלה הראו כי האינטראקציה בין HA ל‑CD44 הכרחית ומספיקה כדי שהתאים הסרטניים ידביקו זה את זה בזרם דם מהיר.
בליטות זעירות ומנעולים מכאניים בונים צברים איתנים
דימות ברזולוציה גבוהה חשף את הכוריאוגרפיה הפיזית של היווצרות הצברים. תאי TNBC בודדים מייצרים בליטות דקיקות רבות על הממברנה המבוססות אקטין — מעין חיישנים — מלאות ב‑CD44 ומקושטות בקצוות ב‑HA. כאשר שני תאים מתקרבים, החיישנים הללו נפגשים ראשונים ויוצרים גשרי HA–CD44 התחלתיים. עם הזמן הבליטות מחליקות האחת ליד השנייה, מושכות את גופי התאים זה כלפי זה עד שאזורים רחבים של הממברנות נשכבים כמעט זו לצד זו. התהליך מחזיר לפעולה את אופן בניית צמתי ההידבקות באפיתל רגיל, אך כאן הוא מונע על ידי ציפוי סוכרי גמיש במקום שרשראות חלבוניות נוקשות. כאשר אזור המגע מתבגר, מערכת נוספת מצטרפת: דסמוזומים, צמתי חיבור חזקים שמקשרים את הממברנה לתשתית פנימית. חלבוני הדסמוזום מצטברים רק לאחר שנוצר המגע המבוסס על HA ופועלים כמנעולים מכניים שמסייעים לצברים לעמוד בפני כוחות הגריפה של הזרימה. כשהרכיבים הדסמוזומליים הושמטו, הצברים נוצרו אך התפרקו תחת מתח גזירה גבוה יותר.
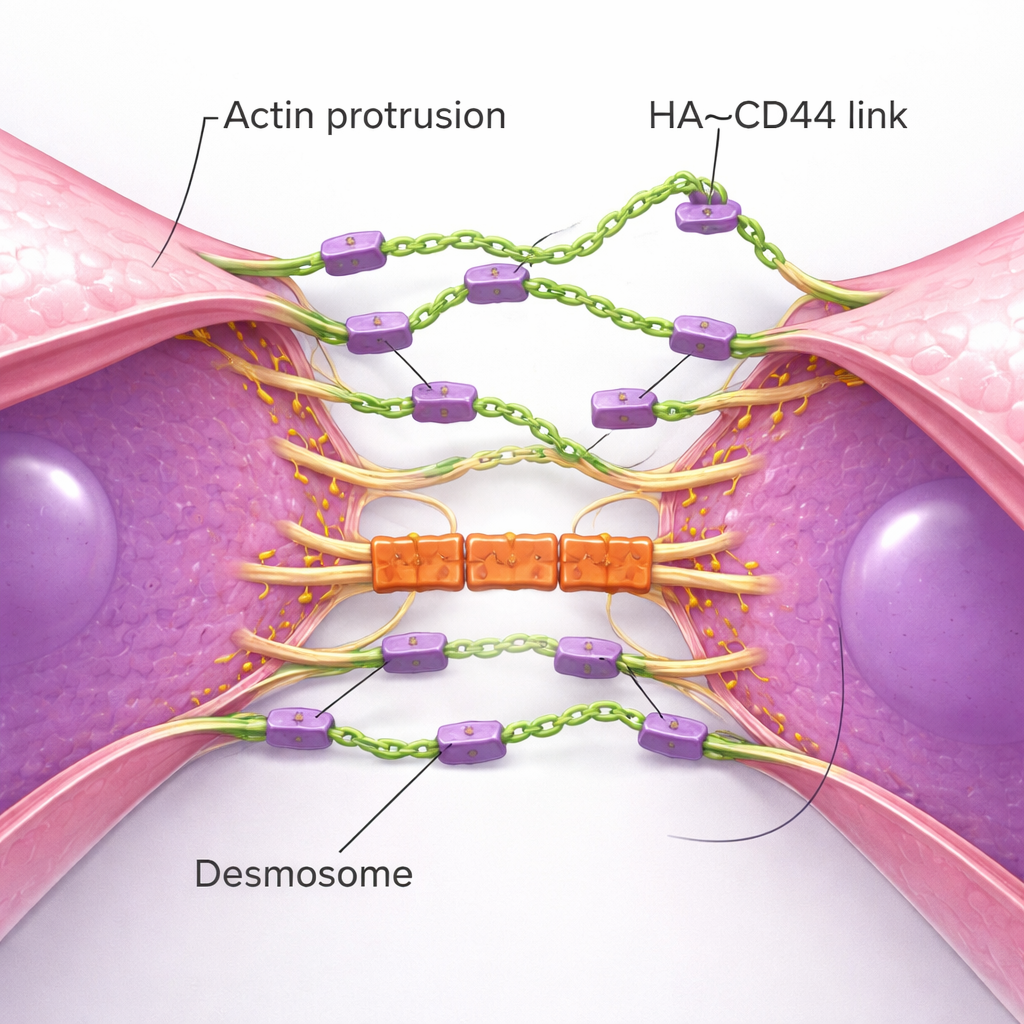
מדוע צבירה חשובה להישרדות ולמטסטזיס
מערכת הצבירה המבוססת על HA הייתה יותר מאשר דרך להישאר יחד; היא שיפרה ישירות את ההישרדות. תחת זרימת דם מדומה ממושכת, צברי HA־עשירים הראו רמות נמוכות בהרבה של סוגי חמצון מזיקים ושל מוות תאי מאשר תאים בודדים דלים ב‑HA. בדגמי עכבר, תאי TNBC חסרי HAS2 ייצרו כמות קטנה בהרבה של CTCs, יצרו צברים זעירים בלבד וגרמו בהרבה פחות גרורות לריאות — אף כי הגידולים הראשוניים שלהם גדלו באותו קצב. כשהוחדרו לעכברים צברים מוכנים מראש של תאים בקרה ותאים חסרי HAS2, התאים העניים ב‑HA היו פחות סבירים להתישב בריאות. יתר על כן, CTCs מצופים ב‑HA יכלו "לגייס" תאים נוספים — הן תאי סרטן חסרי HA והן תאים חיסוניים נורמליים כמו נויטרופילים — לצברים מעורבים, בתנאי שהשותפים הביעו CD44. דגימות דם ממטופלות עם TNBC מטסטטי הראו את אותו דפוס: CTCs לעתים קרובות נשאו ציפוי HA, עם ריכוז HA בנקודות המגע בין תאי הגידול ובין תאים סרטניים ולא־סרטניים.
מה המשמעות של זה עבור מטופלות וטיפולים עתידיים
ללא רקע מקצועי, המסקנה המרכזית היא שלפני חלק מהתאים המסוכנים של סרטן השד אינם נוסעים כרווקים אלא כצוותים קטנים ושיתופיים, הנחזקים יחד על ידי ציפוי סוכרי חיצוני וקולטתו, במקום על ידי "הריבטים" התאיים הקלאסיים שנמצאים ברקמות נורמליות. המנגנון המבוסס HA–CD44 מסייע לתאי הגידול לשרוד את הזרימה העזה, להתאחד זה עם זה ועם תאים תומכים בדם, ולהניח גרורות במקומות מרוחקים בצורה יעילה יותר. פגיעה בייצור HA (למשל על‑ידי עיכוב HAS2) או חסימת האינטראקציה עם CD44 עשויות, בעקרון, להחליש את הצברים ולהקשות על מטסטזיס של TNBC, ומציעות זווית חדשה לטיפולים אנטי‑מטסטטיים בעתיד.
ציטוט: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
מילות מפתח: סרטן השד טריפל־נגטיבי, תאי גידול נישאים במחזור הדם, היאלורונאן, CD44, מטסטזיס