Clear Sky Science · he
עיצוב מעכבי קובאלנטיות מעניק פעילות כנגד שני המצבים של KRAS G12C הקשורים ל‑GDP ול‑GTP
מדוע זה חשוב לטיפולים בעתיד בסרטן
סרטן שמנוהל על‑ידי מוטציות בגן בשם KRAS נחשב מזה זמן רב לאחד הקשים ביותר לטיפול. לאחרונה, תרופות חדשות שסוגרות צורה מוטантית נפוצה אחת, KRAS G12C, הגיעו לחולים והחלו לשנות תמונה זו. מאמר זה בוחן רעיון שאפתני עוד יותר: האם ניתן לעצב תרופות שחוסמות את KRAS G12C בשני מצבי הפעולה העיקריים שלו בתוך התא, והאם הדבר יהפוך את הטיפול בסרטן למהיר, חזק או עמיד יותר?
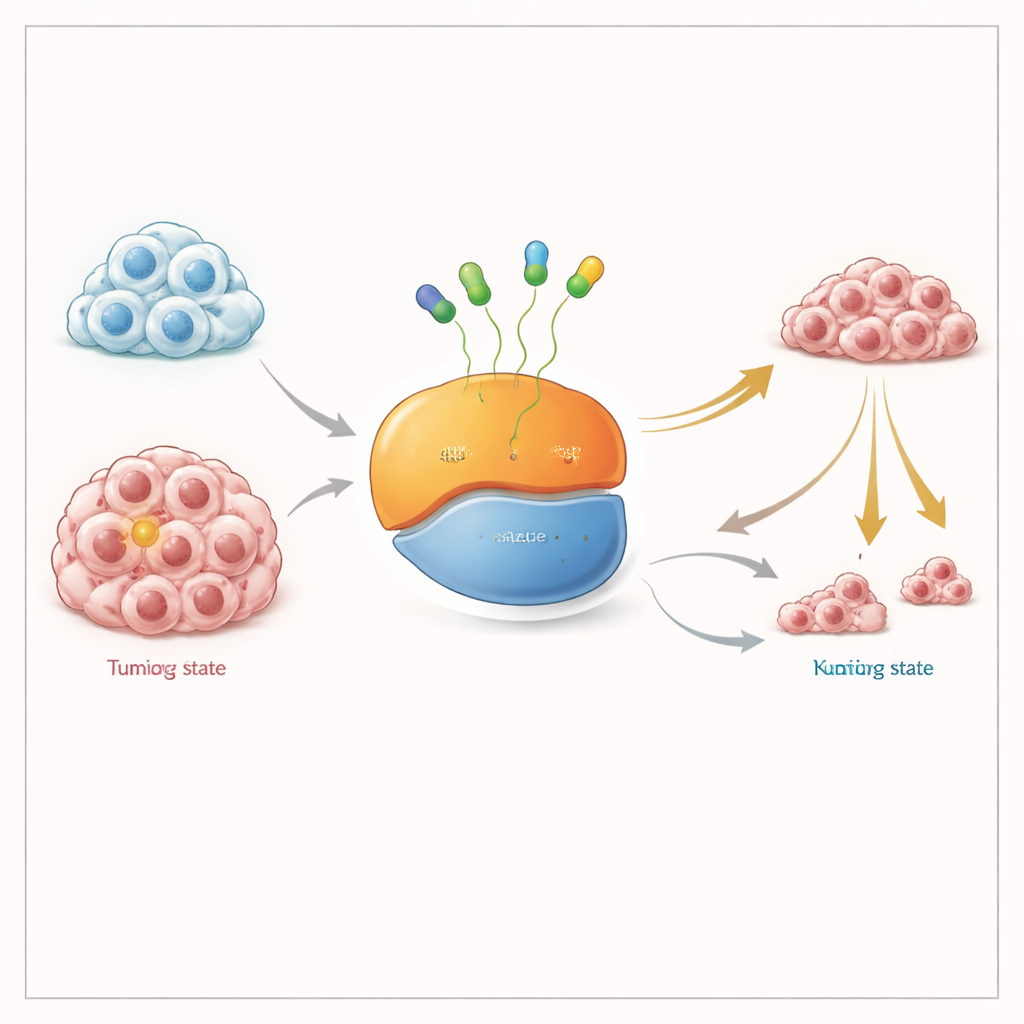
כביית מתג מולקולרי בשני מצבים
KRAS מתפקד כמו מתג קטן שמדליק ומכבה אותות גדילה תאיים. הוא מקפיד בין מצב "כבוי", שבו הוא אוחז במולקולת נשא אנרגיה אחת (GDP), ובין מצב "דלוק", שבו הוא אוחז במולקולה אחרת (GTP). המוטציה KRAS G12C גורמת לכך שהמתג נשאר חלקית בדלוק ומניע את צמיחת הגידול. התרופות הקיימות שאושרו על‑ידי ה‑FDA נקשרות לצורה ה"כבויה" ונועלות אותה; עם הזמן, ככל שיותר KRAS עובר דרך הצורה הזו, מאגר החלבון המוטנטי מנוטרל. רבים מהמדענים טענו שתרופה היכולה לתפוס את KRAS גם במצבים ה"דלוק" וגם ה"כבוי" צריכה לעבוד טוב יותר, במיוחד בגידולים שמסתגלים על‑ידי שמירה של יותר KRAS במצב הדלוק.
עיצוב וו מולקולרי חדש
המחברים הציבו לעצמם מטרה לבנות תרופות דו‑שימושיות כאלה. הם התמקדו בשקע קטן סמוך לאזור גמיש של KRAS שנקרא Switch II, בו כבר נקשרות התרופות הנוכחיות. במקום לשנות עד כמה המולקולות שלהם מתיישבות בשקע, הם שדרגו את קטע ה"ראש" הכימי (warhead) שיוצר קשר קובאלנטי קבוע לציסטאין המוטנטי בעמדה 12. באמצעות דגמים ממוחשבים וסינתזה של עשרות וריאנטים, הם גילו ראש תלת‑חלקי מיוחד שמתקרב לציסטאין מזווית מעט שונה. ההסטה העדינה הזו יוצרת מספיק מקום למולקולת GTP הגדולה יותר, ומאפשרת לתרכובות החדשות לקשור את KRAS הן כשהוא נושא GDP והן כשהוא נושא GTP. בדיקות ביוכימיות אישרו שהתרכובות המובילות יכולות לשבש את השותפות של KRAS עם שותף איתות מרכזי, RAF, בשני המצבים.
לראות כיצד החלבון משנה את צורתו
כדי להבין מדוע המולקולות הללו פועלות, הצוות קבע מבני גביש ברזולוציה גבוהה של התרופה קשורה ל‑KRAS. הצילומים הללו הראו שהראש החדש מגיב באתר לא שגרתי על השלד הכימי, בשבילו נושר אטום פלואור ויוצר קשר קובאלנטי בפחמן שונה מזה של תרופות סרטן טיפוסיות המתמקדות בציסטאינים. הכימיה המותאמת הזו מסייעת לתרופה להשתלב בכיס Switch II גם בנוכחות GTP. המבנים גילו גם שכאשר המעכב נקשר, הוא דוחף מולקולת מים זעירה ומסדר בעדינות לולאת נוספת, Switch I, שאופן ההתקשרות הרגיל שלה הוא עם חלבונים שמעבירים את האות הלאה. שינוי allosteric זה מקרב שני חומצות אמינו ליצירת גשר מלח הדוק, מעוות את המשטח כך ש‑RAF כבר לא יכול לעגן ולהעביר אותות גדילה.
השבתה מהירה, אך ללא השפעה חזקה יותר בטווח הארוך
מצוידים בתובנות המבניות הללו, החוקרים שיפרו שתי מולקולות מובילות הנצמדות ביעילות ובבררנות ל‑KRAS G12C, תוך פגיעה מועטה בחלבונים אחרים הנושאים ציסטאינים. בקווי תאים סרטניים, מעכבים דו‑מצביים אלה חסמו במהירות מסלול איתות מרכזי הידוע כ‑MAPK, כפי שנמדד באובדן תג כימי על חלבון ERK ובהדכאה חזקה של גדילת התאים. הם השביתו את KRAS בתאים מהר יותר מתרופה ייחוס שמטרתה רק את המצב הלא פעיל. במודלים של גידולים בעכברים, מולקולה מובילה אחת הראתה זמינות אורלית טובה, יצרה במהירות קשרים קובאלנטיים ליעד וקטנה גידולים או האטה את גדילתם. עם זאת, כאשר הצוות השווה בין מעכבים דו‑מצביים למעכבים של המצב הלא פעיל על פני זמנים ארוכים יותר, שני הסוגים הגיעו בסופו של דבר לרמות דומות של השבתת KRAS, עיכוב מסלול ויכולת שליטה על הגידול.
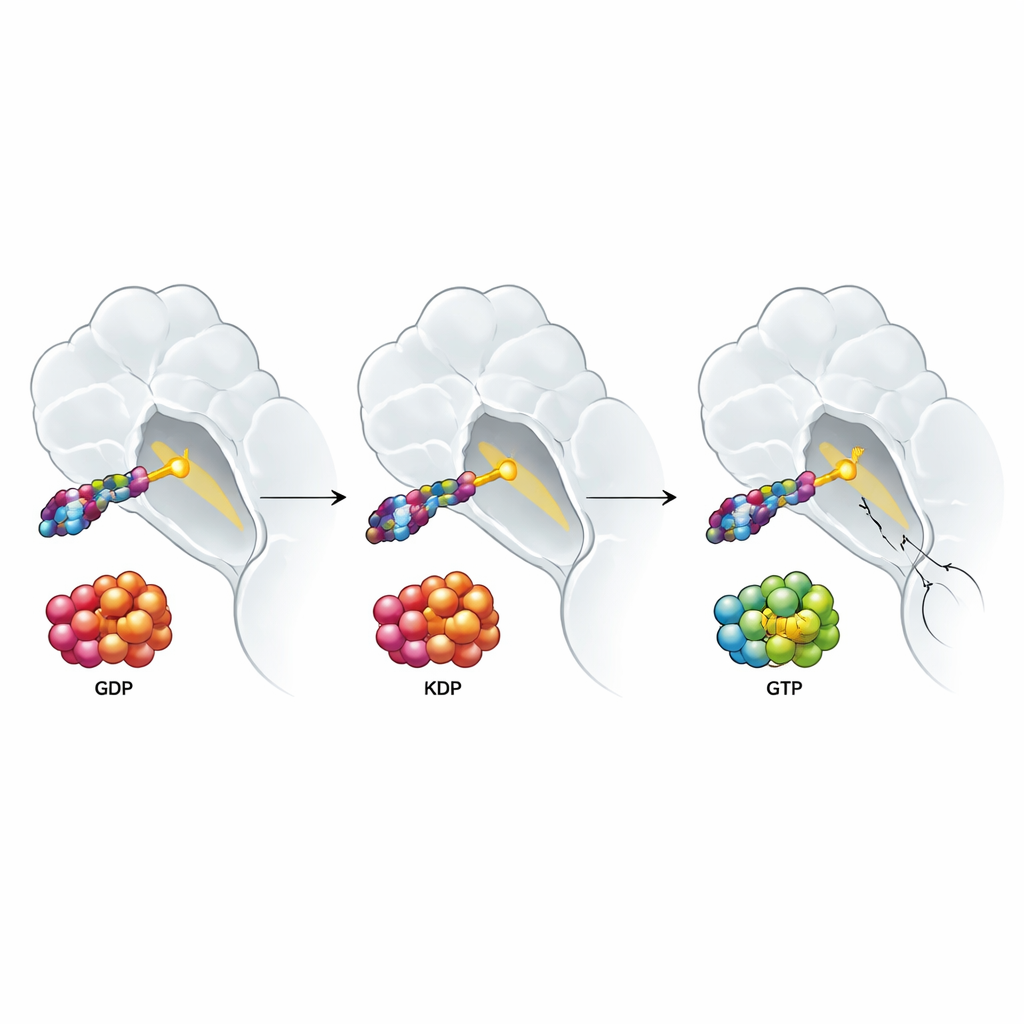
מדוע אותות גדילה מהסביבה של הגידול עדיין גוברים
המחקר בדק גם כיצד אותות מהסביבה של הגידול משפיעים על תרופות אלו. גורמי גדילה כמו EGF ו‑HGF, השכיחים סביב גידולים רבים, דוחפים את חלבוני RAS לכיוון הצורה הפעילה הטעונה ב‑GTP ומוכרים כמחלישים תגובות לטיפולים ממוקדים. אפשר היה לצפות שתרופה שנקשרת לצורה הפעילה של KRAS G12C תעקוף בעיה זו. במקום זאת, המחברים מצאו ששני המעכבים — הדו‑מצבי והמעכב של המצב הלא פעיל — איבדו את העוצמה שלהם בנוכחות גורמי גדילה אלה. ניסויים מפורטים הצביעו על אשמה מפתיעה: הפעלה של צורות RAS הנורמליות ולא המוטנטיות (H‑RAS ו‑N‑RAS), שיכולות לעקוף את KRAS G12C ולהמשיך להזרים אותות גדילה. כאשר החוקרים השמיטו את H‑RAS ו‑N‑RAS בקו תאי סרטן ריאה, העמידות המונחית על‑ידי גורמי גדילה נעלמה ברובה עבור כל סוגי התרופות שמטרתן KRAS G12C, בעוד שתרופה שחוסמת שלב יורד במסלול הושפעה פחות מלכתחילה.
מה זה אומר עבור חולים ופיתוח תרופות
בסך הכל, העבודה מדגימה כי מבחינה כימית ומבנית אפשרי לבנות תרופות קובאלנטיות ל‑KRAS G12C שתופסות את החלבון גם במצב ה"דלוק" וגם במצב ה"כבוי", ושהמעכבים הדו‑מצביים הללו יכולים להשבית את האיתות במהירות רבה יותר מהתרופות הקיימות. עם זאת, ההיצמדות המהירה לא תורגמה לשליטה בולטת יותר בגידולים או לפתרון של בעיית העמידות המונעת על‑ידי גורמי גדילה במודלים פרה‑קליניים. עבור חולים, זה מרמז שלהוסיף פעילות כנגד הצורה הפעילה של KRAS לבדה עשוי להיות לא מספיק; אסטרטגיות משולבות שיטפלו גם בחברי משפחת RAS אחרים או בצמתים יורדים במסלול עשויות להיות נחוצות. ראש הכימיה החדש והתוכנית המבנית המוצגת כאן מרחיבים את ארגז הכלים להתמקדות ב‑KRAS וימליצו על הדורות הבאים של טיפולים מותאמי‑דיוק בסרטן.
ציטוט: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
מילות מפתח: KRAS G12C, מעכב קובאלנטי, עיכוב דו‑מצבי, אותות MAPK, עמידות לתרופות