Clear Sky Science · he
שינוי קוולנטי של חומצה גלוטמית בהשראת טכנולוגיית HaloTag
להפוך "עוגנים" חלבוניים למטרות תרופתיות
רבות מהתרופות המודרניות לסרטן פועלות על ידי הצמדות לחלבונים בתוך התאים שלנו. אולם חלק מהחלבונים החשובים ביותר חסרים "ידיות" נוחות לתרופות לתפוס. במחקר זה מוצג טריק כימי מתוחכם, בהשראת כלי מעבדה פופולרי בשם HaloTag, שמאפשר להצמד לנקודה בדרך‑כלל קשה‑להשגה על חלבון המשפיע על אותות גדילה הרלוונטיים לסרטן. העבודה עשויה לפתוח דרכים חדשות לפיתוח תרופות החוסמות מסלולי גידול ממאירים באופן יציב יותר.
מדוע רוב התרופות הקוולנטיות מכוונות לאותו אתר
בשנים האחרונות מה שמכונה תרופות קוולנטיות ממוקדות הפכו לסוג מרגש של תרופות. הן נושאות קבוצת כימית מועטה‑תגובתית היוצרת קשר קבוע לחומצת אמינו ספציפית בחלבון, ומנעלת את התרופה במקומה. כמעט כל התרופות האלה מייעדות את הציסטאין, חומצת אמינו נדירה יחסית אך תגובתית מאוד. לאמור, שתי חומצות אמינו אחרות, אספרטאט וגלוטמט, נפוצות הרבה יותר ולעתים קרובות חשובות לצורת החלבון ותפקודו, אך הקבוצות החומצתיות (קרבוקסילאט) שלהן פחות תגובתיות בסביבה מימית בתוך התא. זה מקשה על שינוי סלקטיבי שלהן, ורק מעט דוגמאות מוצלחות של מעכבים קוולנטיים המכוונים לגלוטמט או לאספרטאט היו קיימות לפני עבודה זו.
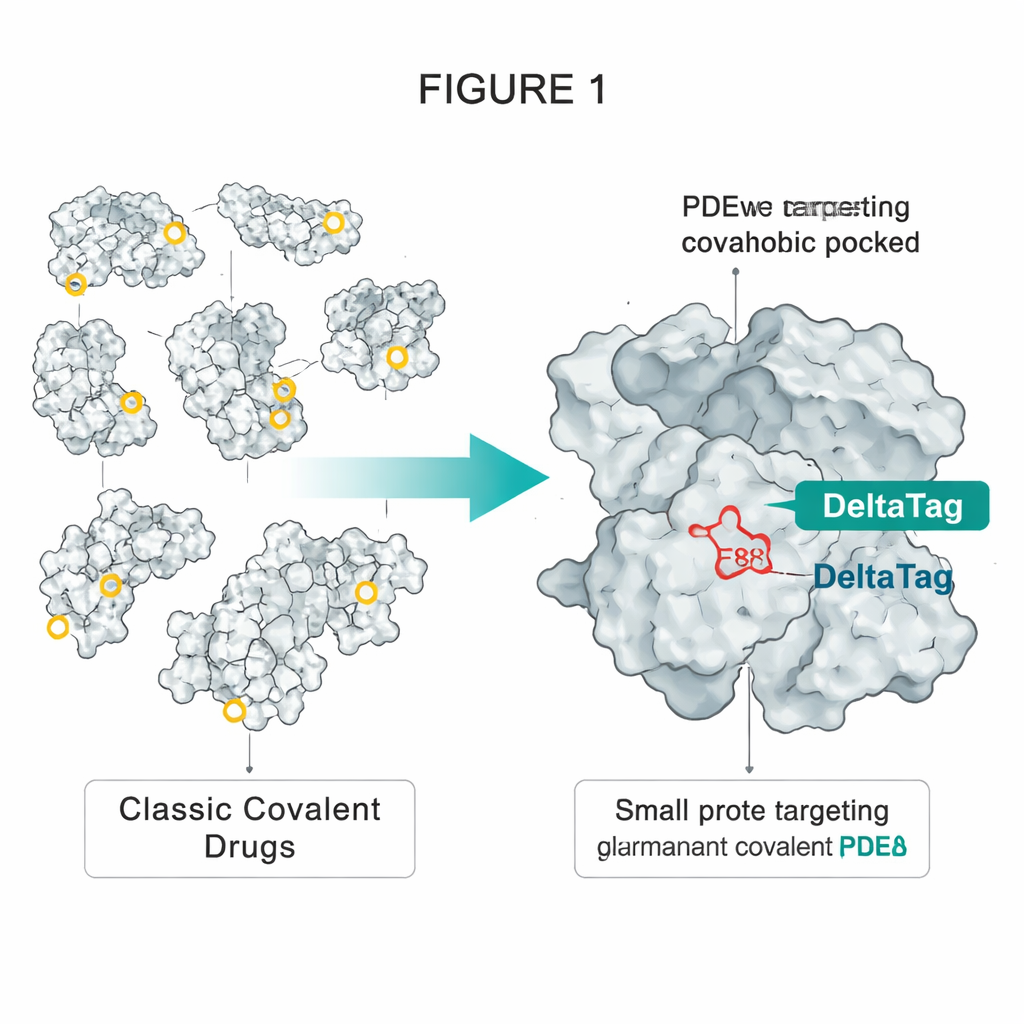
שימוש בטריק מ‑HaloTag
המחברים שאבו השראה מ‑HaloTag, חלבון מהונדס הנפוץ שיכול להיות מתוייג לצמיתות בדיאז פלואורסצנטיים. ב‑HaloTag, אספרטאט שממוקם בעמוקה בתוך כיס הידרופובי מגיב עם שרשרת כלורו‑אלקאן פשוטה על הצבע, ויוצר קשר אסטר יציב. הצוות הבחין שלחלבון אחר, PDEδ, יש כיס הידרופובי דומה יחסית שמכיל גלוטמט בודד ונגיש, הנקרא E88. PDEδ מלווה חלבונים ממותגים בשומנים כגון GTPase הקטן Rheb בתא, ועוזר להם להגיע לממברנות שבהן מקובצים קומפלקסים מקדמי גדילה כמו mTORC1. מעכבים לא‑קוולנטיים קודמים של PDEδ יכלו לחסום את ההסעה הזו, אך האפקט שלהם היה מוגבל מפני חלבון אחר, Arl2, שיכול להוציא אותם מהכיס עם הזמן.
עיצוב DeltaTag לנעילה על גלוטמט
כדי להתגבר על בעיית ההוצאה הזו, החוקרים התחילו ממחסום PDEδ ידוע בעל קיבולת קשירה גבוהה ושינו אחת מהשרשרות הצדדיות שלו כך שתישא "ראש מלחמתי" של חלאואלקאן בדומה לאלו שבליגנדים של HaloTag. דרך מספר סבבי כיוונון מבני מונחים על ידי מבני גבישי חלבון הם הגיעו למולקולה שנקראת DeltaTag. המאפיין המרכזי שלה הוא קבוצת פנאתיל ברומיד הממוקמת כך שכאשר המולקולה מתמקמת בכיס השומני של PDEδ, הברומיד מיושר במדויק להגיב עם E88. מדידות ביופיזיקליות ומבני קרני רנטגן ברזולוציה גבוהה אישרו ש‑DeltaTag יוצר קשר אסטר קוולנטי באופן סלקטיבי עם גלוטמט זה ושהחומצות האמיניות הפוטנציאלית‑יותר תגובתיות ב‑PDEδ נשארות לא מושפעות. התרכובת תגובתית דיין כדי לתייג את החלבון ביעילות, אך יציבה דיו במים ובנוכחות הנוגד‑חמצון העיקרי מבוסס הגופרית בתא, גלוטתיון, כדי להימנע מנזק נרחב ולא בררני.
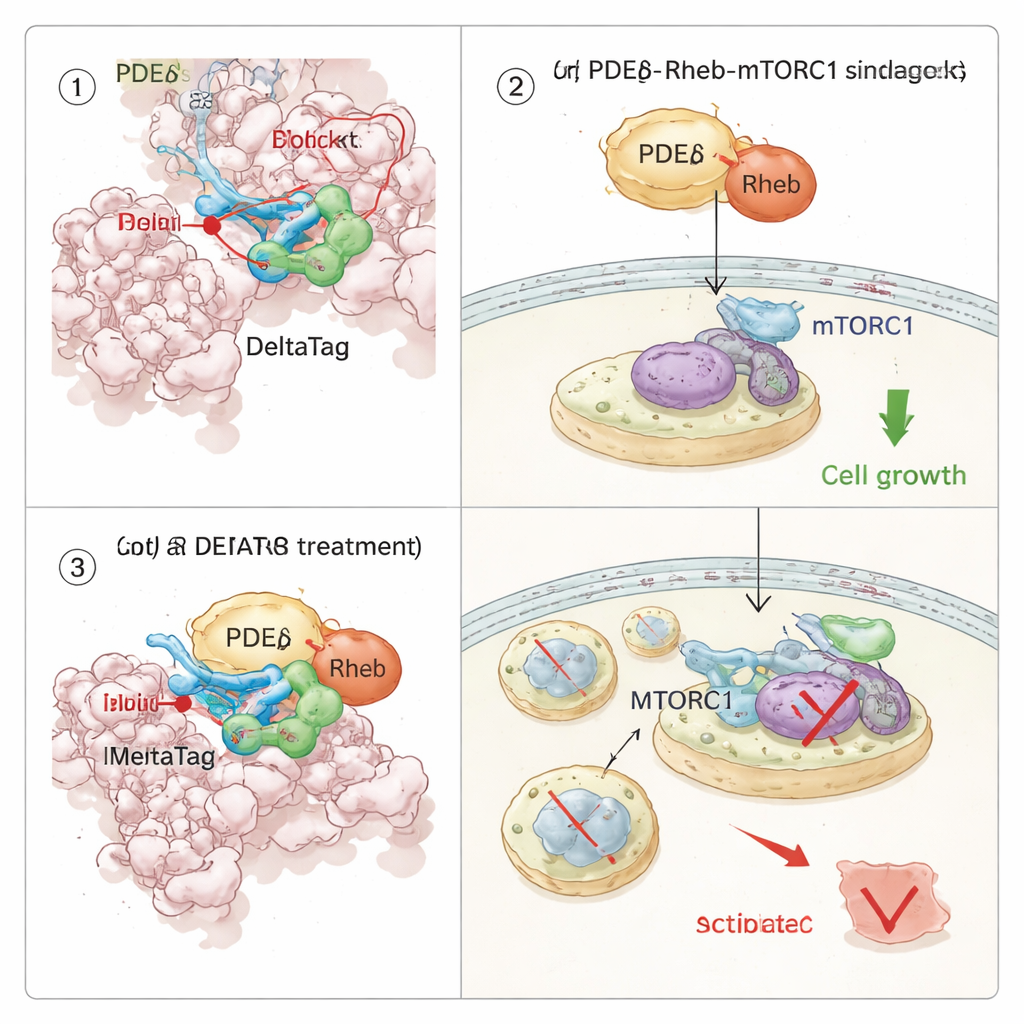
חיבור מחדש של מסלול גדילה בתוך תאי סרטן
מכיוון ש‑PDEδ מלווה את Rheb, ו‑Rheb בתורו מפעיל את מסלול הגדילה mTORC1, הצוות בדק כיצד עיכוב קוולנטי של PDEδ ישפיע על איתות התא. באמצעות פרופיל יציבות תרמית על אלפי חלבונים הם הראו ש‑DeltaTag נקשר באופן סלקטיבי ל‑PDEδ לחץ‑תא ומשבש חלבונים הקשורים לציר Rheb–mTOR. בניסויי הדמיה בתאים חיים, DeltaTag גרם ל‑Rheb לעבור מהתפלגות מפוזרת בחלק הפנימי של התא להצטברות בממברנות פנימיות, תואם לפגיעה בהסעה הטיפוסית שלו. פרוטאומיקה פוספורילציה גלובלית ובדיקות ווסטרן מדויקות הראו שפעילות mTORC1, שמדידה על‑ידי פוספורילציה של חלבון הריבוזומלי S6, ירדה עם הזמן, בעוד אותות פיצוי במסלולים קשורים עלו. באופן חשוב, בכמה שורות תאים של סרטן אנושי המונעות על‑ידי מוטנט KRAS ותלויות באיתות mTOR חזק, DeltaTag האט את התרבות התאים ביעילות גבוהה יותר ממעכבים הפיכים קרובים, והשפעתו הייתה חלשה יותר בתאים חסרי PDEδ, תומך בכך שהפעולה העיקרית שלו היא על‑היעד.
פתיחת דלת לסוגים חדשים של מטרות תרופתיות
העבודה מראה שאפשר לבנות מולקולות קטנות היוצרות קשר קבוע וסלקטיבי מאוד לגלוטמט יחיד שקבור בכיס שומני בחלבון, באמצעות כימיה יחסית פשוטה של חלאואלקאן שנשאבה מ‑HaloTag. במערכת המודל PDEδ הקשר הקוולנטי הזה מספק חסימה עמידה יותר של מסלול גדילה רלוונטי לסרטן מאשר תרופות הפיכות קודמות. באופן רחב יותר, אותה לוגיקת עיצוב יכולה להיות מיושמת על חלבונים אחרים שיש להם חללים הידרופוביים אך חסרים חומצות אמינו "תגובתיות" רגילות, כל עוד הם מציגים גלוטמט או אספרטאט ממוקם באופן אסטרטגי. עם אופטימיזציה נוספת, מעכבים קוולנטיים המכוונים לגלוטמט כמו DeltaTag עשויים להפוך לכלים שימושיים בביולוגיה כימית ובסופו של דבר לעופרת לתרופות חדשות המתמודדות עם חלבונים הקשים כיום לטיפול.
ציטוט: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
מילות מפתח: מעכבים קוולנטיים, מיקוד בגלוטמט, PDEδ, איתות mTOR, עיצוב תרופות לסרטן