Clear Sky Science · he
שינויים בקצה ה-C של חלבונים משפיעים על פרוטאוסטאזיס
איך קצה הזנב של חלבונים מעצב בריאות
כל חלבון בתאים שלנו מסתיים בזנב קטן המורכב רק ממספר מצומצם של אבני בניין. זנבות אלה עשויים להיראות כשוליים, אך המחקר הזה מגלה שהם בקול שקט קובעים אילו חלבונים נשארים ואילו מוסרים במהירות. מכיוון שרמות חלבונים עומדות בבסיס סרטן, מחלות גנטיות ואופן תגובת התאים ללחץ, הבנה של זנבות אלה פותחת דרכים חדשות לקריאת סיכון למחלות ואפילו לעיצוב טיפולים עתידיים.
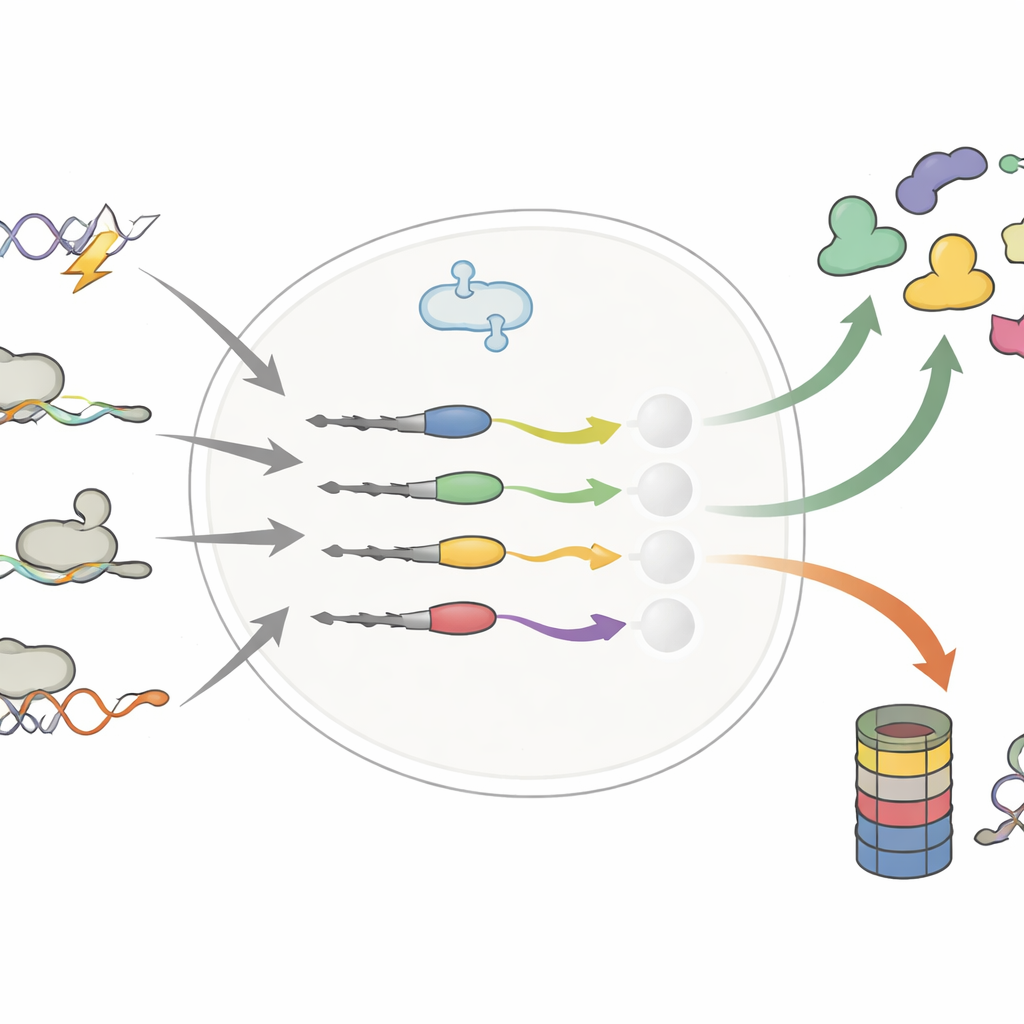
שינויים זעירים בזנב החלבון, שינויים גדולים באורך החיים
המחברים התמקדו בקצה הרחוק של החלבון — ה-C-טרמינוס — שבו גם מספר בודד של אבני בניין נוספים או מוחלפים יכולים להופיע כתוצאה ממוטציות ב-DNA, מספlicing חלופי של RNA, או מקריאת ריבוזומים מעבר לסימן העצירה הרגיל. עבודות קודמות הצביעו על כך שזנבות כאלה, שלכאורה שגויים, פועלים בעיקר כתוויות סילוק ושולחים חלבונים פגומים למטחנת התא. בהשוואה שיטתית של אלפי זנבות רגילים ומשונים, המחקר הזה מערער על התמונה הפשוטה הזו. הקבוצה מראה כי זנבות משונים יכולים לקצר או להאריך את חיי החלבון, ולעתים לייצב מנגנוני סרטן או דווקא לא-instabilize מדכאי גידול.
מתי שגיאות גנטיות עוזרות או מזיקות לחלבונים
מקור מרכזי לשינויי זנב הוא מוטציות nonstop, שמוחקות אות עצירה רגילה כך שהריבוזום ממשיך לתוך מקטע RNA שבדרך כלל שתקן. החוקרים בדקו יותר מ-3,000 וריאנטים nonstop המקושרים למחלות בעזרת דוחף דו-צבעי שמודד עד כמה כל זנב מגן על חלבון מודל או מחליש אותו. בממוצע, זנבות מוטנטיים הפכו את החלבונים לפחות יציבים מאשר אלה הרגילים, אבל חלק משמעותי עשה בדיוק את ההפך: בערך אחת מכל עשר מוטציות nonstop יצרה חלבון יציב יותר, בעוד שכמעט שליש גרמו לטריס־יציבות. השינויים הללו השפיעו על אונקופרוטאינים ומדכאי גידול ידועים, הרומזים שמוטציות שנראו זניחות יכולות בפועל להשפיע על מאזן צמיחת התאים ומותם.
גיוון מובנה משחלוף וקריאת-מעבר
בלא כל ההבדל, לא כל הבדלי הזנב הם תאונות. הגנים שלנו מייצרים באופן שגרתי גרסאות חלבוניות מרובות באמצעות רצפי שחלוף אלטרנטיביים וקריאת-מעבר מתוכננת של קודוני העצירה. על ידי כריית מאגרי גנים אנושיים, המחברים מצאו שכמעט שני שלישים מהגנים מייצרים חלבונים עם יותר מתכנון זנב אחד, ורבים מהם שונים רק בכמה אבני בניין אחרונות. בדיקת דוגמאות נבחרות הראתה שגרסאות כמעט זהות אלה לעתים קרובות שונות באופן בולט במחצית החיים שלהן. חלק מהזנבות הנוצרים בקריאת-מעבר הפכו חלבונים ליציבים יותר, אחרים הפכו אותם לפחות יציבים. ממצא זה מצביע על כך שהתאים משתמשים במודע בגיוון זנבים ככלי לכיול עדין, המכוון כמה זמן צורות חלבון מסוימות מתקיימות ברקמות או בתנאים שונים.
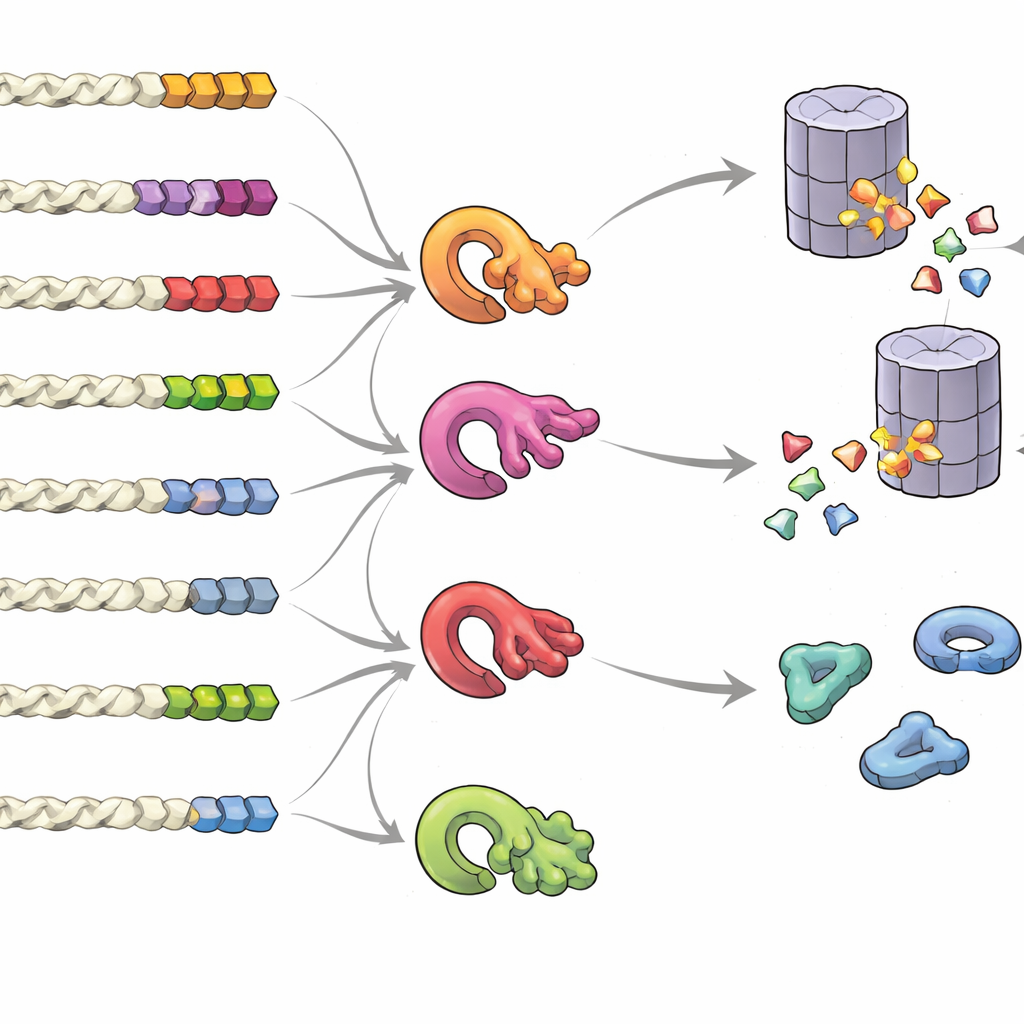
מה עושה זנב להיות אות "שמרו אותי" או "זרקו אותי"
כדי להבין אילו תכונות של זנב משפיעות על גורל החלבון, הקבוצה יצרה ספריות של זנבות אקראיים ומדדה את השפעתם בכמויות גדולות. הם מצאו שמדובר לא במוטיב אחד קשיח אלא בהרכב כללי, מיקום וצביריות של אבני בניין מסוימות. זנבות עשירים ברכיבים קטנים או שומניים, או בחומצות אמינו נדירות כמו ציסטאין וטיריפטופן, נטו לקרב לפירוק, במיוחד כאשר שיירים אלה הצטברו בקבוצה. לעומת זאת, זנבות עשירים ברכיבים חומציים העדיפו יציבות. בבחינה רחבת-ממדים במגוון מינים, זנבות חלבון רגילים הראו סימני לחץ אבולוציוני להימנעות מתבניות מסוכנות, בעוד שזנבות שגיאותיים מסוג קריאת-מעבר או frameshift נטו להרכבים שגורמים לאי-יציבות. הקבוצה גם גילתה שכמה אנזמי בקרה על איכות — ליגאזות ubiquitin שונות — מתמחים בזיהוי תבניות הידרופוביות שונות בזנב, ויוצרים רשת מסובכת שמחליטה אילו חלבונים יושמדו.
מדוע זה חשוב לרפואה וביוטכנולוגיה
העבודה משנה את הפרספקטיבה: זנבות חלבון אינם נקודות סיום פסיביות אלא בקרים פעילים של רבבות חלבונים. עבור הקורא הכללי, משמעות הדבר היא שרבות מהמחלות עשויות לנבוע לא רק מחלבונים פגומים אלא גם משינויים עדינים במשך הזמן שבו חלבונים נשארים, מונעים על ידי הבדלים זעירים בסופם. המחקר גם מזהיר שטיפולים המקדמים במתכוון קריאת-מעבר של סיגנלי עצירה, המשמשים לטיפול בהפרעות גנטיות מסוימות, עלולים לשנות בלי כוונה את חיי הרבים מהחלבונים הרגילים. באותו זמן, הממצאים מציעים אסטרטגיות חדשות וחזקות: על ידי עיצוב רצפי זנב או עידוד תאים להעדיף צורות שחלוף או אירועי קריאת-מעבר מסוימים, מדענים עשויים בעתיד לכוון רמות חלבון כלפי מעלה או מטה בדיוק מרשים.
ציטוט: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
מילות מפתח: יציבות חלבון, זנב קצה-ג, פירוק חלבונים, מוטציות גנטיות, פרוטאוסטאזיס