Clear Sky Science · he
ניצול אלוסטריה של פוקוסילטרנספראזת האדם 8 באמצעות מעכבת קוולנטית לדיכוי פוקוזילציה גרעינית
מדוע חסימת סוכר קטן יכולה להיות חשובה בסרטן
התאים שלנו מקשטים באופן קבוע חלבונים בשרשרות סוכר קטנות שמעדנות את אופן פעולתם. סימון סוכרי מסוים, המכונה פוקוזילציה גרעינית, מסייע לגידולים לגדול, להתפשט, להתחמק ממערכת החיסון ואפילו לפתח עמידות לתרופות מודרניות לסרטן. מאמר זה מתאר כיצד חוקרים גילו נקודת בקרה סמויה על האנזים האנושי שמוסיף סוכר זה, ובנו מולקולה חדשה בעלת רעילות נמוכה שנקשרת לנקודת הבקרה כדי לנטרל את האנזים. עבודתם פותחת נתיב חדש לתרופות שמעוותות בעדינות את דפוסי הסוכרים על פני התא במקום לתקוף ישירות את ה‑DNA או את החלבונים.
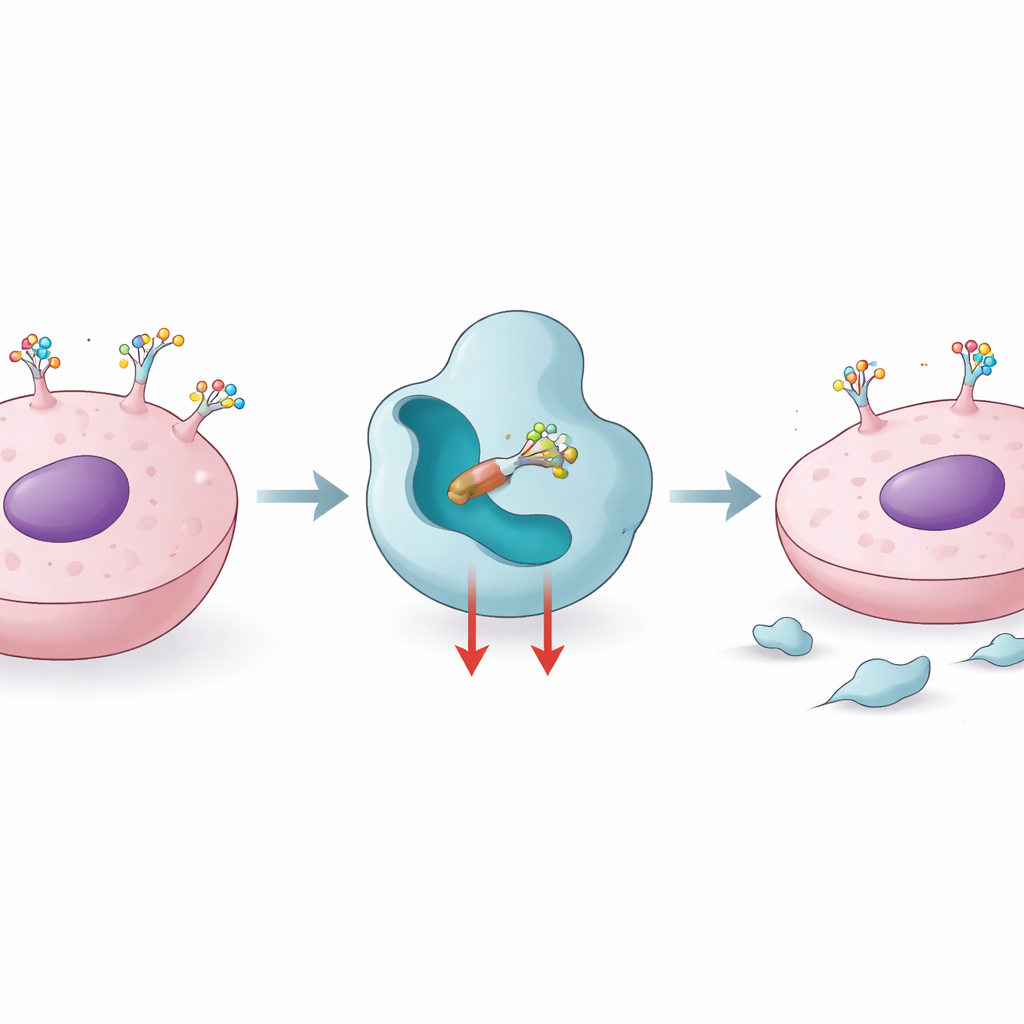
כיצד תאים משתמשים בתגי סוכר לעיצוב מחלות
חלבונים היוצאים ממפעל הפנים של התא עוברים "קו גימור" מולקולרי שבו מוסיפים ומעבדים שרשרות סוכר. פוקוזילציה גרעינית היא אחד מהצעדים האלה, שמבוצע על ידי אנזים בשם FUT8, המוסיף יחידת פוקוזה למיקום מרכזי על גליקנים מקושרי חלבון. כאשר רמות FUT8 עולות, סימון סוכרי זה הופך נפוץ יותר על מולקולות שמווסתות גדילה תאית, תנועה וזיהוי חיסוני. מחקרים קישרו פעילות גבוהה של FUT8 למלנומה אגרסיבית, סרטן שד טריפל‑נегטיבי, סרטן ריאה ולעמידות לתרופות ממוקדות ולחלק מהטיפולים בנוגדנים. חסימת FUT8 יכולה להסיר חלבוני בלימה חיסונית, כגון PD‑1, מפני התא ולגרום לגידולים להיות גלויים יותר למערכת החיסון, מה שהופך את FUT8 למטרה אטרקטיבית באימונותרפיה ובשיפור תרופות ביולוגיות.
הצורך בחוסמים חכמים וסלקטיביים יותר
עיצוב תרופות נגד FUT8 היה מאתגר כיוון שרבים מהאנזימים הקרובים משתמשים באותה דלק סוכרי בסיסי. מעכבים מוקדמים חיקו לעתים את הדלק הזה, מה שהוביל לשיתוק רחב ולא סלקטיבי של מסלולי פוקוזילציה רבים ותופעות לוואי לא רצויות, כולל בעיות קרישה שבלמו ניסוי קליני. המחברים סברו כי אסטרטגיה טובה יותר תהיה להימנע מהאתר הפעיל הצפוף ולחפש במקום זאת אתר "מרוחק" ייחודי ב‑FUT8 שיכול לשמש כמפסק בקרה. באמצעות בדיקת סריקה מהירה שעקבה אחר פעילות האנזים, הם סיננו מעל שישה אלפים תרכובות וסימנו כמה מולקולות בצורת שרשרת שאטו את FUT8 ובאותו זמן הפחיתו פלישה של תאי סרטן במעבדה.
גילוי כיס בקרה מוסתר
באמצעות קריסטלוגרפיית רנטגן, הצוות פתר את המבנים התלת‑ממדיים של FUT8 קשור לשתי מעכבות אלה. להפתעתם, אף אחת מהתרכובות לא ישבה במקום המקובל שבו נקשרים התורם והמקבל של הסוכר. במקום זאת, שתיהן יישבו בכיס ארוך בדומה לתעלה בין שני אונות מרכזיות של האנזים, קרוב אך נבדל מהמרכז הפעיל. קשירה באתר זה הזיזה לולאות וחומצות אמינו מפתח ממיקומן, במיוחד מרכיבים שעוזרים בדרך כלל לאחוז את תורם הסוכר. סימולציות ממוחשבות הראו שכאשר הכיס מלא, התנועה הכוללת ונוף האנרגיה של FUT8 השתנו, והעדיפו צורות שמקשות על קטליזה. במילים אחרות, המעכבים פעלו אלוסטרית: הם לחצו כפתור מרוחק שגרם לחלקי העבודה של האנזים להימצא במצב לא תואם.
הפיכת מולקולת ״מסע טור״ לכלי קוולנטי מדויק
מצוידים במפת המבנה הזו, החוקרים חיפשו מולקולות שלא רק יתפסו את הכיס אלא גם ייצרו קשר קוולנטי עם שארית ליזין קרובה (K216) שבראייה טבעית נעה לכיוון התעלה. הם מצאו כי תגובה בשם SSO, שנושאת אתרי אסתר N‑הידרוקסי‑סוקצינימיד תגובתי, נקשרה באותו חריץ ויצרה קשר קוולנטי עם K216, מה שנעץ את האנזים במצב לא פעיל. בהתבסס על התכונות המשותפות של SSO ושל המולקולה הראשונית שלהם NH125, הם מיזגו מקטעים משניהם ליצירת מולקולה חדשה שנקראת CAIF. מבני קריסטל אישרו כי CAIF נמתחת לאורך התעלה, מתיישבת בנוחות בין שאריות הידרופוביות ויוצרת קשר קוולנטי עם K216. העיצוב הזה חיזק את עיכוב FUT8 פי כמה בהשוואה למולקולות האב שלו, תוך חיסכון באנזימים קרובים דמיון, והדגיש את הצורה הייחודית של כיס האלוסטרי של FUT8.
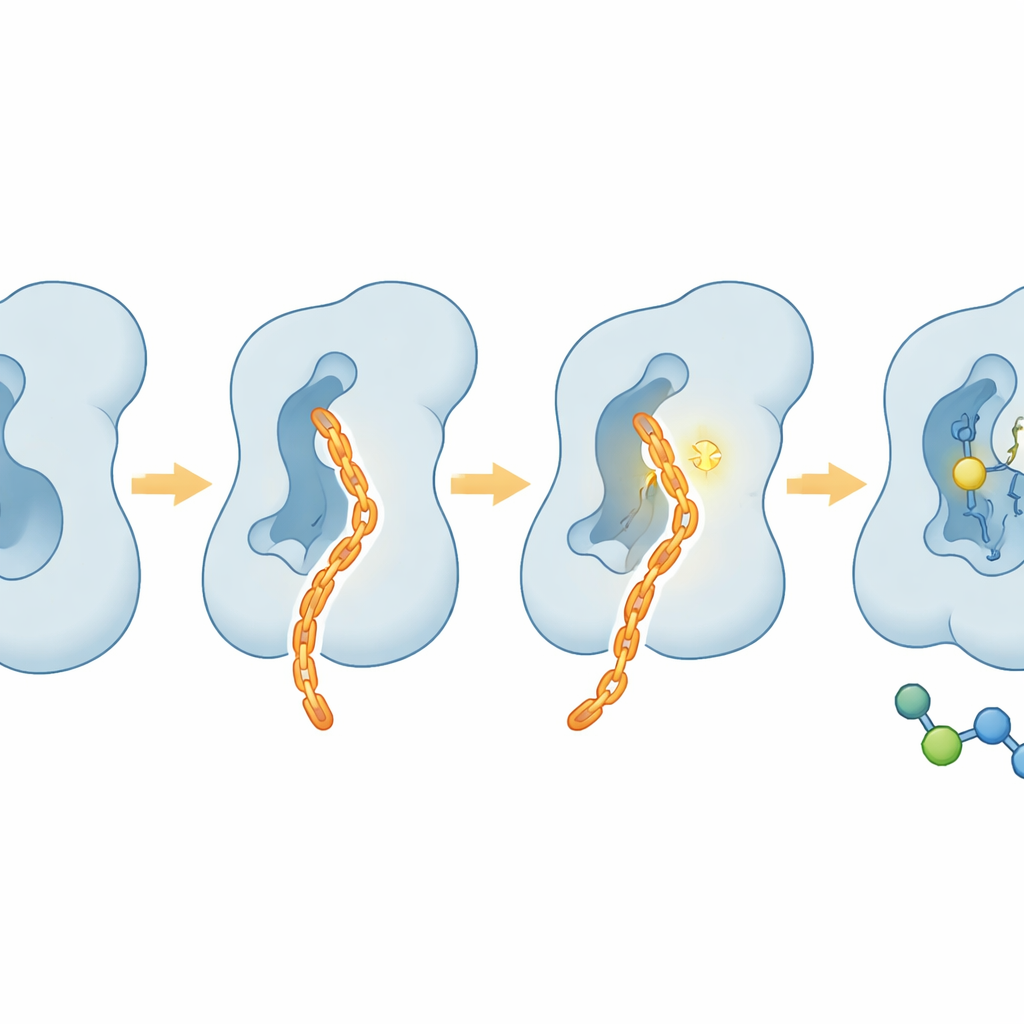
רך כלפי תאים, קשה בהתנהגות הגידול
מעבר לצינורות מבחנה, הצוות בדק כיצד CAIF מתנהג בתאים חיים. במספר שורות תאים אנושיות, CAIF הראה רעילות מזערית גם במינונים גבוהים, מה שמצביע על כך שאינו מרעיל באופן כללי את מכניקת התא. עם זאת, הוא הפחית באופן משמעותי את הפוקוזילציה הגרעינית על פני התא, כפי שנחשף על ידי צובעים הקושרים סוכרים, ועשה זאת בסלקטיביות טובה בהרבה ל‑FUT8 לעומת מעכבים כלליים מוקדמים. בבדיקות פלישה של תאי סרטן, CAIF הצליח יותר ממחסום מבוסס סוכר שנפוץ בשימוש במניעת יכולת התאים לנוע דרך מטריצה — מאפיין של פוטנציאל גרורתי. השפעות אלה תואמות את התפקיד הידוע של FUT8 בהגברת פלישה והתחמקות חיסונית ולא ככוח שמניע ישירות חלוקת תאים.
מה משמעות הדבר לטיפולי סרטן עתידיים
מחקר זה אינו טוען ש‑CAIF עצמו מוכן להיות תרופה. במקום זאת, הוא מראה כי FUT8 מכיל כיס אלוסטרי שניתן לטפל בו ושהיה קודם לכן לא מוכר, שניתן למקד אותו עם מולקולות מעוצבות בקפידה שיוצרות קשר עמיד לליזין יחיד. על ידי ניצול האתר הזה, חוקרים יכולים להנמיך באופן סלקטיבי אנזים שמשנה סוכרים ועומד בצומת של התקדמות סרטן, התחמקות חיסונית ועמידות לתרופות, תוך השארת אנזימים קרובים יחסית בלתי מושפעים. העבודה מספקת תבנית לעיצוב מעכבים בדור הבא שמעצבבים דפוסי סוכר רלוונטיים למחלה על חלבונים ועלולה להרחיב בסופו של דבר את ארגז הכלים לאימונותרפיה סרטן ולשיפורי תרופות בנוגדנים.
ציטוט: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
מילות מפתח: עיכוב FUT8, פוקוזילציה גרעינית, מעכבים אלוסטריים קוולנטיים, גליקוזילציה בסרטן, עיצוב תרופות לגליקוזילטרנספראזות