Clear Sky Science · he
FANCD2 מגביל את התקדמות הזנב ומונע שבירות במקורות מוקדמים בעת שכפול-מחדש
כשעותקי DNA חורגים מעט מהתסריט
בכל חלוקת תא יש להעתיק את כל ספריית ה‑DNA פעם אחת בדיוק. אם חלקים מהספרייה מועתקים פעמיים, או מועתקים במהירות ובחוסר דיוק, התוצאה עלולה להיות כרומוזומים שבורים ומוטציות שמזינות סרטן. המחקר הזה בוחן מה קורה כשמנגנוני ההגנה נגד סיבובי שכפול נוספים מתחילים לכשל, וחושף כיצד חלבון תיקון בשם FANCD2 מתערב כדי למנוע מתאים שמסטים במעט להידרדר לכאוס גנומי מלא.
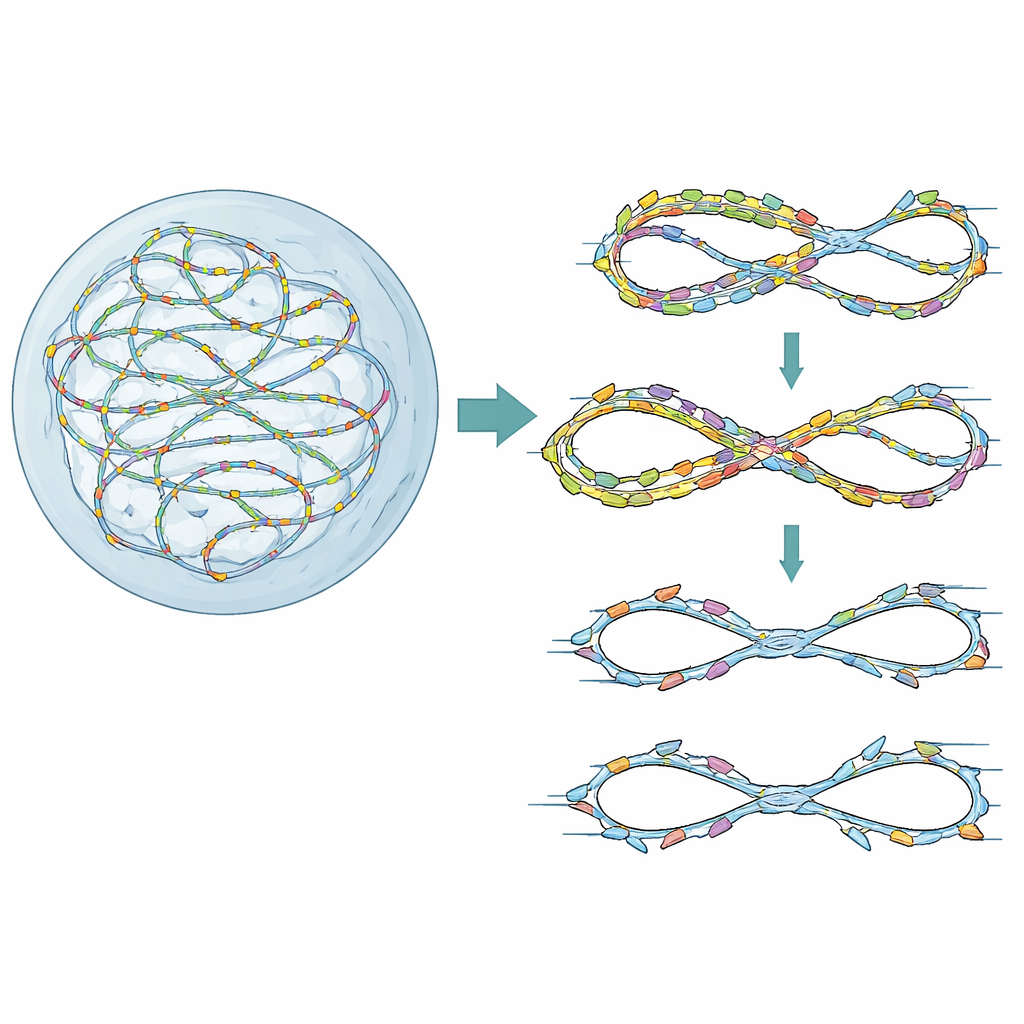
מעקות להעתקה נקייה פעם אחת
הכרומוזומים שלנו מוכפלים מתוך אלפי נקודות התחלה, או "מקורות", שמורשות ואז מופעלות בסדר ובתזמון קפדני. חלבון קטן בשם Geminin מסייע בדרך כלל להבטיח שכל מקור יופעל רק פעם אחת במחזור התא. כאשר Geminin אובד או מוחלש, כמה מקורות עלולים להיפעיל שוב על DNA שכבר הועתק — מצב שנקרא שכפול-מחדש. תאים סרטניים, שנוטים לייצר עודף גורמי רישוי, רגישים במיוחד לבעיה זו. המחברים השתמשו תחילה בסקר גנטי בר-תכולה גבוהה בתאים אנושיים שמוכוונים לשכפול-מחדש ברמה נמוכה על ידי דלדול Geminin. הם בדקו אילו גנים לתיקון DNA ולנקודות בקרה הופכים לקריטיים במצב הלחוץ הזה וגילו ש‑FANCD2, המוכר בעיקר מתיקון קישורי DNA באנמיה של Fanconi, מתגלה כמגן מרכזי על הישרדות התא ושלמות הגנום.
מגיב ראשון במכונות העתקה מעומסות
הצוות אז עקב אחרי היכן ומתי FANCD2 מופיע בתאים העוברים שכפול-מחדש. זמן קצר אחרי הסרת Geminin, FANCD2 מצטבר במהירות על הכרומטין ומייצר מוקדי גרעין מוארים, הרבה לפני שניתן לזהות שבירת DNA נרחבת. בעזרת תיוג של DNA חדש יחד עם מבחני קרבה הם הראו ש‑FANCD2 נרתם ישירות למכונות ההעתקה הפעילות, במיוחד בתאים שבהם ה‑DNA כבר מועתק פעם שנייה. בתאים מסונכרנים ששוחררו למחזור החלוקה הבא צצה אוכלוסייה מובחנת המראה דפוס DNA של שכפול-יתר מפוזר. תאים אלה הציגו אותות חזקים של FANCD2 ו‑RPA, המציינים מתח שכפול מתמשך, והוחזקו בגבול לפני מיטוזה על ידי נקודת בקרה פעילה, מה שמרמז ש‑FANCD2 הוא חלק מתגובה מוקדמת שמייצבת מזלי שכפול לחוצים במקום להגיב רק ל‑DNA שבור.
עיכוב זנבות פרועים ופערים נסתרים
כדי לבדוק כיצד FANCD2 מעצב את ההעתקה, החוקרים שילבו אובדן Geminin עם דלדול FANCD2. באופן מפתיע, הסרת FANCD2 לא הגבירה את השבר שנראה בשיעור התאים עם גנומים שהועתקו מחדש באופן ברור. במקום זאת, ניסויי סיבים של DNA חד‑מולקולריים חשפו שמזלגות ההעתקה נסעו מרחק גדול יותר והפכו לא סימטריים יותר — סימן להתקדמות בלתי שווה ולא יציבה. מזלגות מהירים אלה השאירו מאחוריהם יותר פערים חד‑גדיליים ב‑DNA החדש, שנראו כמוקדי RPA ו־BrdU אינטנסיביים ואוששו על ידי הרגישות של המסלולים המתויגים לאנזים החותך אזורים חד‑גדיליים. תאים חסרי Geminin וגם FANCD2 הראו זינוק בשבירות כרומוזומים, רסיסים, גופים גרעיניים ומיקרו‑גרעינים — כולם סימני היכר של חוסר יציבות גנומי חמור. חסימת PARP, גורם שעוזר בדרך כלל לנהל פערים כאלה, חיקה והחריפה את הליקויים האלה, ומדגישה שיצירת פערים בלתי מבוקרת היא במרכז הנזק.
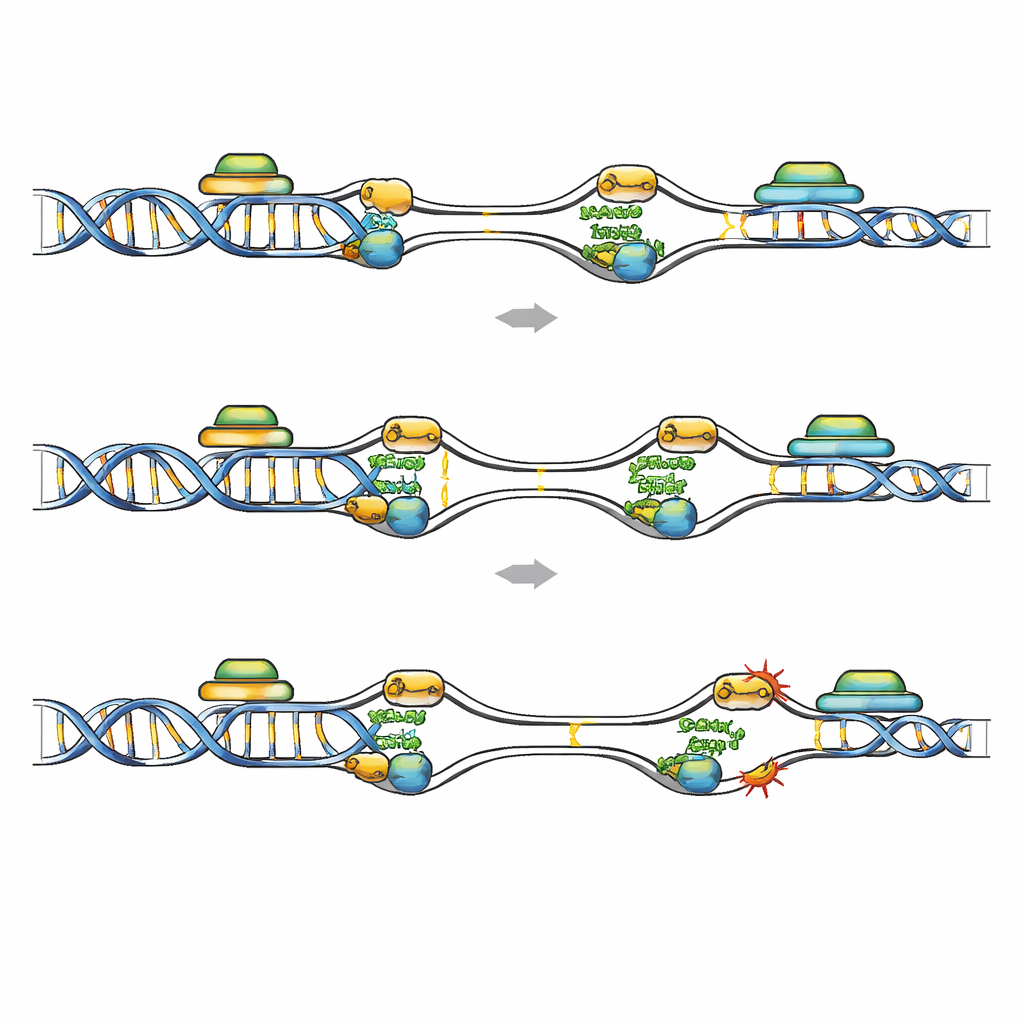
נקודות שבירות שבהן העתקה וקריאה מתנגשות
מיפוי מיטבי של קשירת FANCD2 ברחבי הגנום סיפק תמונה של האזורים שבהם שכפול-מחדש מסוכן במיוחד. בתאי לויקמיה עם דלדול Geminin, FANCD2 זז מאתרים שבירים שכיחים קלאסיים למקורות שכפול המופעלים מוקדם שמשולבים בתוך גנים קצרים, עשירים ב‑GC ובעלי שעתוק גבוה. אזורים אלה נושאים סימני שעתוק פעיל ורגישים ל‑R‑loops — היברידים של RNA מתהווה עם תבנית ה‑DNA שלהם — שעשויים לחסום שכפול. מאגרי נתונים ציבוריים הראו יותר נזקי DNA ואותות RNA–DNA מוגברים בגנים מועשרים ב‑FANCD2 לאחר אובדן Geminin, והאזורים הללו חפפו לאותם אתרי ‘‘נקודות שבירות מוקדמות''. כאשר השעתוק מדוכא באופן רחב באמצעות תרופה, או כאשר R‑loops מוסרים ספציפית על ידי ביטוי יתר של RNase H1, מספר מוקדי FANCD2, RPA ונזקי DNA בתאים חסרי Geminin ירד באופן ניכר. זה מצביע על כך שהתנגשויות בין מקורות שהופעלו שוב ליחידות שעתוק פעילות, המוחמרות על ידי R‑loops, יוצרות נקודות שבירות ש‑FANCD2 חייב להגן עליהן.
כוונון ההגנה דרך תגיות כימיות
FANCD2 מופעל חלקית על ידי הצמדת תג קטן הדומה לאוביקווויטין. על ידי דלדול FANCA, מרכיב מרכזי במכונות ההצמדה, ובשימוש בתאים שמבטאים מוטנט של FANCD2 העמיד לשינוי זה, המחברים הראו שהמונו‑אוביקוויטינציה משפרת את הישרדות התאים שעוברים שכפול-מחדש אך אינה הכרחית לחלוטין. גם FANCD2 שאינו מתויג העניק הגנה חלקית, תואמת לתפקידים מובחנים גם בחישה וגם ביציבות מזלי שכפול לחוצים. התמונה הכוללת היא ש‑FANCD2 מסייע להאט ולארגן את ההעתקה במקורות פגיעים מוקדמים ומגביל כמה גדולים וכמה רבים יהיו הפערים החד‑גדיליים.
מדוע זה חשוב לטיפול בסרטן
עבור לא מומחים, המסר המרכזי הוא שאין כל טעויות השכפול קטסטרופליות מיד. שכפול-מחדש קל, כפי שמתרחש בחלק מהגידולים, יכול להיות נסבל אם מערכות הגנה כמו FANCD2 שומרות על שכפול DNA מתפרץ ומונעות מהפערים השבריריים להפוך לכרומוזומים שבורים. כאשר המגן הזה מוסר או מוצף, אותן שגיאות רישוי ברמה נמוכה מחריפות במהירות לפיצוץ גנומי. מאחר שאובדן Geminin ופגמים ברישוי השכפול נפוצים בתאים סרטניים, ורבים מהגידולים כבר נושאים חסרונות ברשת Fanconi/BRCA, הפגיעויות שנחשפו כאן מציעות אסטרטגיות טיפוליות: שילוב מעכבים שמדחפים תאים סרטניים לכיוון שכפול-מחדש עם תרופות שמחריפות את הצבירה של הפערים, כגון מעכבי PARP, עשוי לדחוף תאים ממאירים מעבר לסף הסבילות שלהם תוך פגיעה מועטה בתאים נורמליים עם מערכות הגנה שלמות.
ציטוט: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
מילות מפתח: מתח בשכפול ה–DNA, FANCD2, Geminin, שכפול-מחדש, חוסר יציבות גנומית