Clear Sky Science · he
שחרור דראצמיזציה אנזימטית של אלנים מבניים מגוונים על ידי פוטואנזימים בתכנון
למה חשוב לשלב ולשדך מולקולות
תרופות רבות פועלות רק כאשר האטומים שלהן מסודרים באופן תלת‑ממדי מאוד ספציפי, בדומה לאופן שבו יד שמאל מתאימה לכפפה שמאלית אך לא לימנית. כימאים מצליחים לעתים קרובות ליצור מולקולות "אוחזות‑יד" כאלה, אך קשה להשיג זאת בצורה נקייה כאשר אבני הבניין מורכבות. מאמר זה מתמודד עם האתגר עבור כיתה מסובכת של מבנים מפותלים המכונים אלנים, באמצעות אנזימים מתוכננים המופעלים באור. העבודה מראה כיצד ניתן לשלב ביולוגיה ופוטוכמיה כדי לסנן את "היד" המולקולרית הרצויה מתוך תערובת מבולגנת, מה שמבטיח נתיבים מהירים ונקיים יותר לתרופות ולחומרים בעתיד.
אבני בניין מעוקלות עם החזר גדול
אלנים הם שרשורים ליניאריים של שלושה אטומי פחמן עם שני קשרים כפולים סמוכים, אך הסידור הפשוט הזה מעוות את המרחב באופן שמעניק למולקולה כיוון‑יד (handedness). עיוותים צירים אלה מופיעים במוצרי טבע, בחומרי הגנה על גידולים ובקטליזטורים מתקדמים. לצערנו, שיטות מסורתיות להכנת אלנים כירליים נוטות להיות מאוד מותאמות: קטליזטור שעובד מצוין עבור אלן אחד לעתים נכשל עבור אלן אחר שגם הוא משתנה במעט במבנה. גם קטליזטורים כימיים המונעים באור שפותחו לאחרונה נאבקים בבעיה זו. כתוצאה מכך, כימאים נדרשים לעתים קרובות לעצב מחדש קטליזטורים מאפס כאשר הם רוצים לחקור אלנים חדשים, מה שמאט את הגילוי ומגביר בזבוז.
להשאיל את הבחירה של הטבע ולהוסיף אור
אנזימים במערכות חיות מצטיינים בזיהוי והמרת צורות ספציפיות בדיוק מרשים, אך הם התפתחו למטרות טבעיות, לא לאלנים מלאכותיים. המחברים הציבו לעצמם ליצור "פוטואנזים" שמשלב את הסלקטיביות של אנזים עם היכולת ללכוד אור כמקור אנרגיה. הם התחילו ממבנה חלבוני בשם CTB10 ושינו אותו גנטית כדי לשאת חומצת אמינו לא‑טבעית המתנהגת כמו אנטנה זעירה ללכידת אור. כאשר אבני הבניין המיוחדות הללו סופגות אור אולטרה‑סגול, הן יכולות להעביר אנרגיה לאלן הסמוך, לעורר אותו באופן זמני ולאפשר לתפירתו להיטלטל. על‑ידי חזרה של התהליך פעמים רבות, האנזים יכול באופן סלקטיבי להסיר יד אחת מתערובת 50:50 ולהשאיר בעיקר את השנייה. 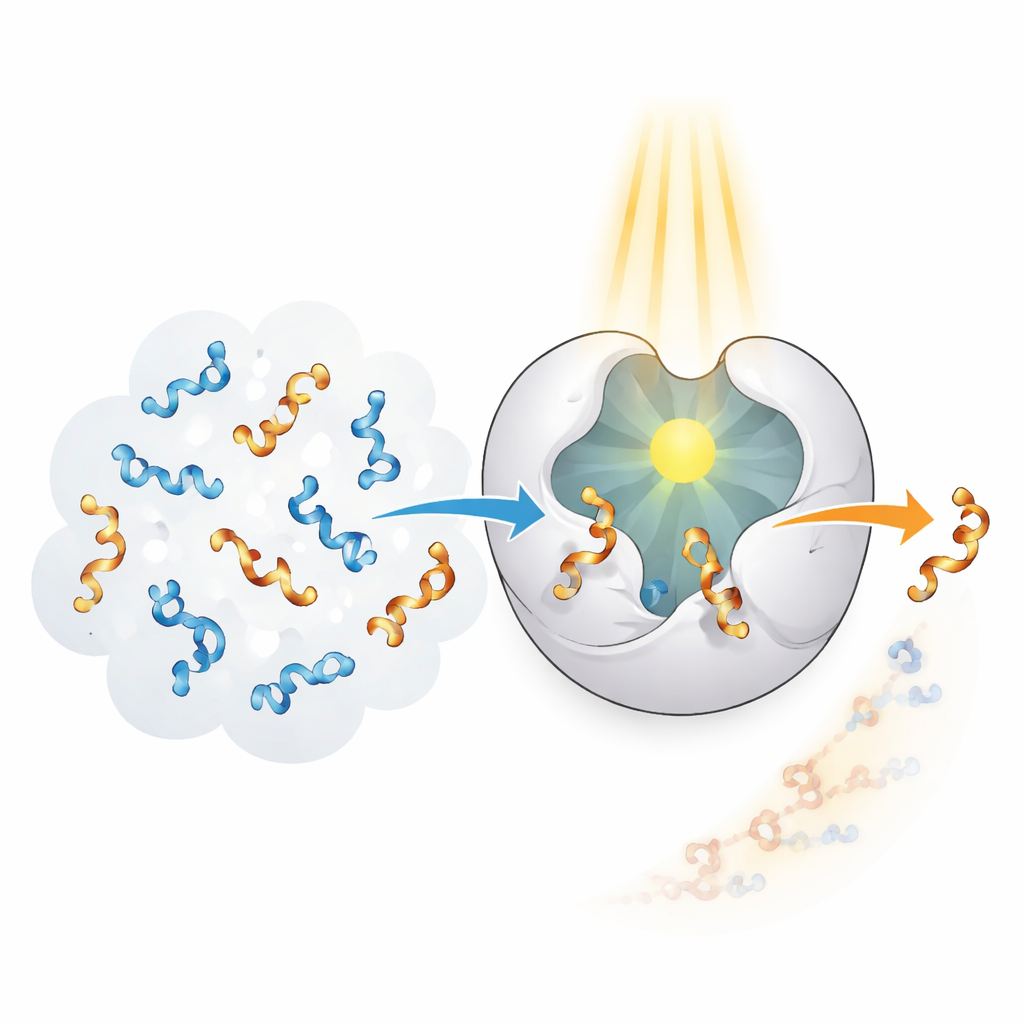
חיזוק כיסים צמודים לאורחים שונים
לעצב מערכת כזו אינו פשוט כמו להאיר חלבון באור. הצוות השתמש במודלינג ממוחשב, מוטציות אסטרטגיות וצילומי קריסטלוגרפיה של קרני‑X כדי לסלסל מספר וריאנטים של הפוטואנזים, לכל אחד כיס פנימי מעט שונה. כיסים אלה מחזיקים את האלן במצב מוגדר ליד אנטנת האור ומייצבים חלקים מרכזיים של המולקולה באמצעות קשרי מימן ואינטראקציות אריזה עדינות. צעד אחר צעד, החוקרים שיפרו הן את עוצמת הקשירה והן את ההתאמה בין האנזים לאלן, שהן קריטיות להעברה יעילה של אנרגיה. הווריאנטים הסופיים הראו ביצועים מרשימים, הממירים חומצות קרבוקסיל של אלנים, אסטרים ואמידים לתוצרים יד‑אחת בטוהר גבוה מאוד, לעתים מעל 99% של כיוון אחד, והכל תחת אוויר ללא צורך בתנאים עדינים.
צפייה במנגנון ברזולוציה אטומית
כדי להבין מדוע הפוטואנזימים החדשים מעדיפים יד אחת על פני השנייה, המחברים גיבשו זוגות אנזים–סובסטרט ובחנו אותם ברזולוציה אטומית. הם מצאו שהיד המועדפת של האלן יושבת קרוב יותר לקבוצת קליטת האור ויכולה לאמץ מספר צורות מעט שונות, כולן תואמות להעברה יעילה של אנרגיה. היד הלא‑מועדפת או נקשרת בחולשה או יושבת רחוק יותר, מה שמקטין מאוד את הסבירות שתעורר. ניסויים נוספים עם חומרים התחלתיים טהורים ימניים ושמאליים אישרו את ההטיה הזו: האנזים ממיר במהירות את היד המועדפת לאינטרמדיאט ריאקטיבי, אשר לאחר מכן מרפה בתמיסה בחזרה לתערובת שבה היד הנגדית מצטברת. בתמצית, החלבון מתנהג כמו פתח מולקולרי סיבובי, שמעורר לצורך ולאוכל יד אחת שוב ושוב בעוד הוא מאפשר לאחרת להצטבר. 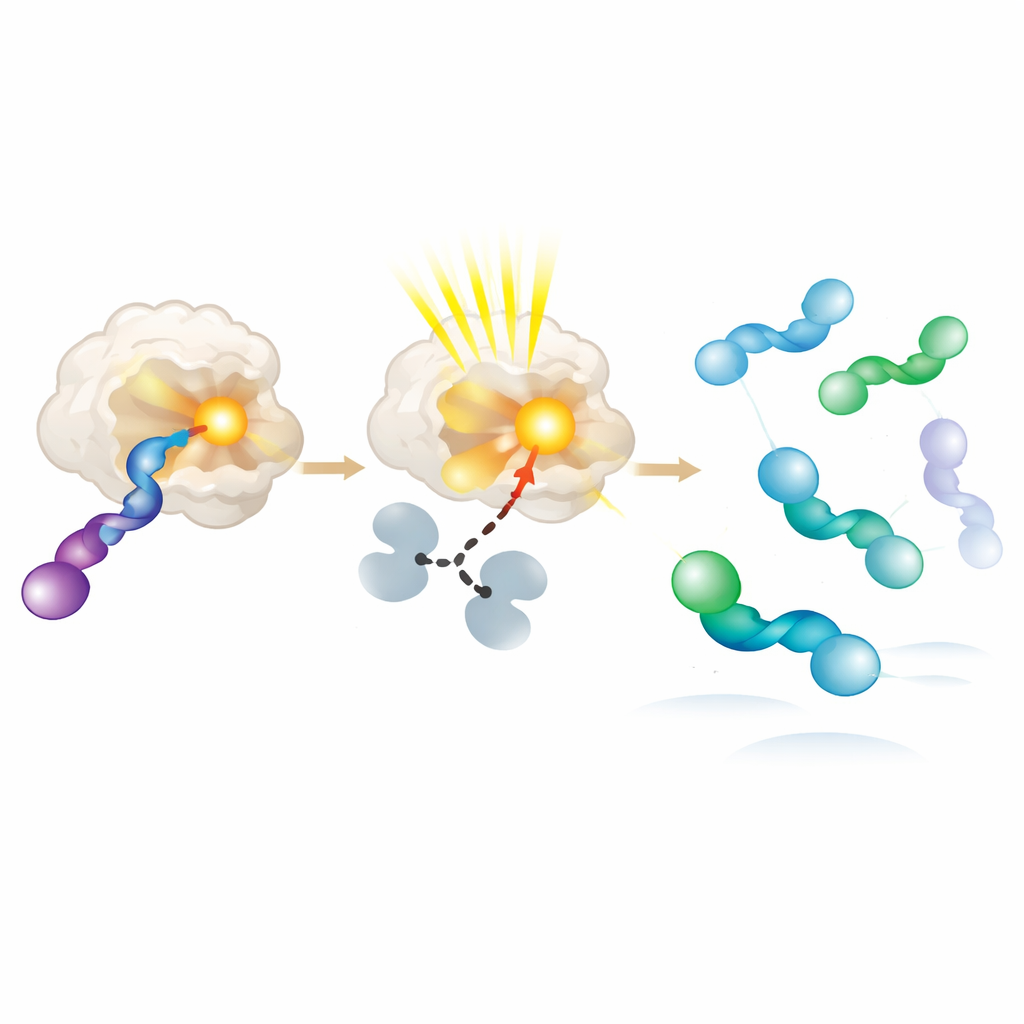
מה משמעות הדבר לכימיה של המחר
עבור לא‑מומחים, המסר המרכזי הוא שהצוות יצר מנוע חלבוני תכנתי המשתמש באור כדי למיין ולשדרג מולקולות מפותלות עם רבגוניות חסרת תקדים. במקום לעצב קטליזטור כימי חדש לכל מטרה, חוקרים יכולים כעת להתחיל מפלטפורמת הפוטואנזים הזו ולכוון את הכיס הפנימי שלה לקבלת מגוון אלנים. גישה זו מצמצמת את הפער בין השליטה העדינה של הטבע לבין הצורך של התעשייה הכימית בשיטות רחבות ועמידות. בטווח הארוך, אנזימים מופעלי‑אור כאלה עשויים לסייע לכימאים להכין אבני בניין מורכבות, בעלות יד‑אחת, לתרופות ולחומרים ביעילות רבה יותר, עם פחות שלבים ופחות בזבוז.
ציטוט: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
מילות מפתח: פוטואנזים, דראצמיזציה, אלן כירלי, ביокатליזה, העברת אנרגיית שלישייה