Clear Sky Science · he
FCHo2, לא טלין, מפעיל מאגד פנימי לאינטגרין ɑvβ5 בהידבקות מעוקלת
איך תאים חשים את צורת הסביבה שלהם
גופנו בנוי מתאים שבאופן קבוע אוחזים בסביבתם, מושכים ודוחפים כדי לנוע, להתחלק או להישאר במקום. המאמר הזה מראה שהתאים לא רק חשים כמה קשיחה הסביבה — הם גם קוראים את צורתה. באמצעות גילוי מערכת הצמדה מיוחדת שמופעלת רק באזורים שבהם ממברנת התא מעוקלת בחוזקה, המחברים מראים שהתאים משתמשים ב"אחיזות" פנימיות שונות לסביבות שטוחות מול סביבות סיביות, עם השלכות חשובות על אופן היווצרות הרקמות ועל התפשטות סרטן.
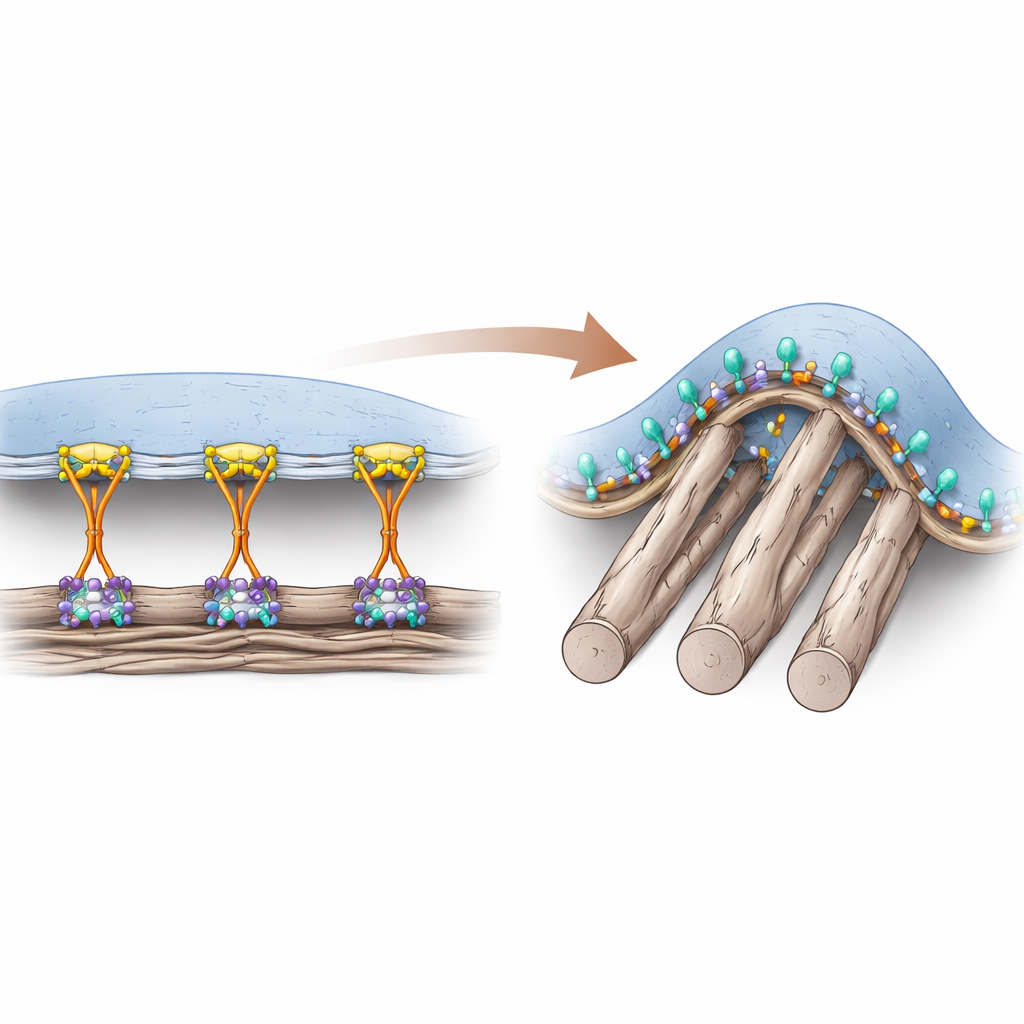
שתי דרכים שבהן תאים אוחזים
תאים מתחברים לחומר העשיר בחלבונים שמסביבם באמצעות קולטנים על פני השטח הנקראים אינטגרינים. במשך שנים סברו חוקרים שחלבון מסייע בשם טלין הוא חיוני להפעיל את האינטגרינים "מבפנים" ולהאפשר הצמדה חזקה באתרים עוגניים קלאסיים הידועים כהדבקות מוקדיות (focal adhesions). הדבקות אלה נוצרות בעיקר על משטחים שטוחים וקשים ומעבירות כוחות משיכה גדולים דרך שלד התא. עם זאת, ברקמות חיות רבים מהסיבים שמסביב הם רכים וצילינדריים, ויוצרים נקודות מגע מעוקלות שלא תומכות בקלות במבנים שנושאים כוחות כבדים אלה. המחברים מצאו בעבר סוג אחר של מבנה הצמדה, הנקרא "הדבקה מעוקלת", שמופיע בדיוק במקום שבו הממברנה מתעקלת סביב סיבים דקים ותלוי באינטגרין ספציפי, αvβ5.
אחיזות מעוקלות משתמשות בעוזר שונה
במחקר החדש הצוות מראה שטלין, אף שהוא עדיין נוכח, אינו המפעיל המרכזי של אינטגרין αvβ5 בהדבקות מעוקלות. במקום זאת, חלבון החוש עיקום בשם FCHo2 לוקח על עצמו תפקיד זה. באמצעות סרגלים ועמודים בננו-ממדים שתוכננו במדויק כדי לכופף ממברנות תאים באופן מבוקר, הם ראו ש-αvβ5 מתאשכול חזק באזורים מעוקלים, אך רק כאשר FCHo2 יכול להיקשר לרצף קצר מאוד — מוטיף HDRRE — שבפנים התא על זנב ה-β5. כאשר מוטיף זה מופרע, האינטגרין עדיין פועל בהדבקות מוקדיות אך לא יכול עוד ליצור הדבקות מעוקלות. השתקת FCHo2 משאירה את ההדבקות המוקדיות הקלאסיות ברובן שלמות אך מחסלת את ההדבקות המעוקלות, בעוד שהסרת טלין מרסה משמעותית את ההדבקות המוקדיות אך משאירה את ההדבקות המעוקלות ברובן בלתי מושפעות.
מתג חומצת אמינו בודדת כבודד צורה
חידה אחת הייתה מדוע אינטגרין קרוב מבנית, αvβ3, אינו יכול ליצור הדבקות מעוקלות למרות שהזנב הפנימי שלו דומה מאוד לזה של β5. על ידי החלפת מתחמים בין שני האינטגרינים והכנסת מוטציות נקודתיות, המחברים זיהו מיקום מכריע אחד קרוב לאתר הקשירה של טלין: לרוב אינטגריני ה-β יש טריפטופן (W), אך ל-β5 באופן ייחודי יש טירוזין (Y766). כאשר הטירוזין של β5 הוחלף לטריפטופן, האינטגרין איבד את יכולתו להשתתף בהדבקות מעוקלות והתנהג יותר כמו β3, המעדיף רק הדבקות מוקדיות. שינוי הפוך — הכנסת טירוזין לשחלוף β3-דמוי — השיב את הרגישות לעיקום. ניסויים נוספים עם וריאנטים המדמים מצבי זרחון או אי-זרחון של טירוזין זה מצביעים על כך ששינוי כימי שלו יכול להטות את האינטגרין לעבר הדבקות שטוחות בעומס גבוה או לעבר הדבקות מעוקלות בעומס נמוך.
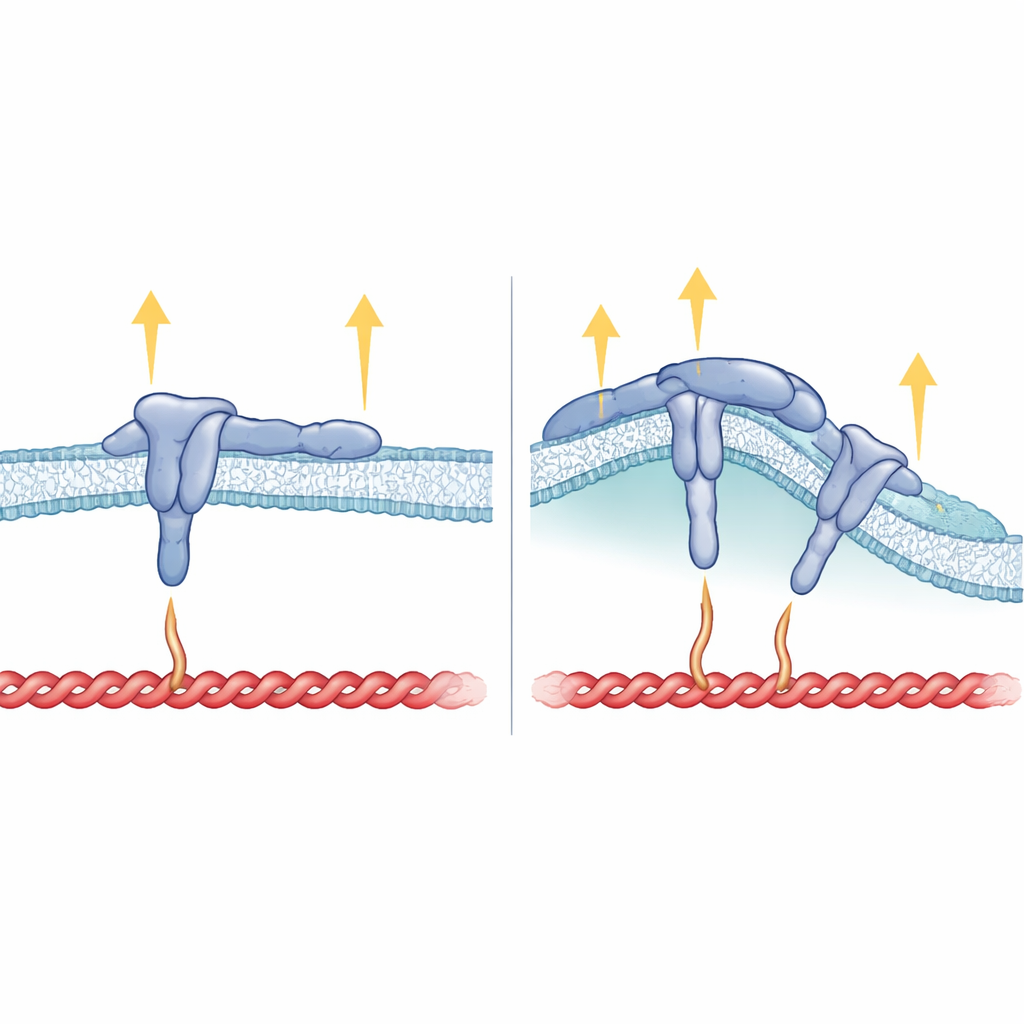
איך צורת הממברנה, מבנה האינטגרין וכוח משתלבים
מעבר לזנב הפנימי, גם החלק של β5 החוצה בממברנה הוכח כקריטי. כאשר החוקרים החליפו את מקטע הטרנסממברנלי של β5 בזה של β3, האינטגרין שהתמגן עדיין יכל ליצור הדבקות מוקדיות אך כבר לא העדיף את האתרים המעוקלים ולא עקב אחרי FCHo2. זאת מרמזת שעל האופן שבו האינטגרין משובץ בממברנה יש חשיבות בהטיית מוטיף ה-HDRRE כך ש-FCHo2 יוכל להיתפס באזורים מעוקלים וייצב את αvβ5 הקשור לליגנד במצב פעיל. בהדבקות מעוקלות, נראה שטלין נוגע רק לחלק רחוק יותר של זנב האינטגרין ואינו נושא מתיחה גבוהה, מה שמסביר מדוע רכיבים שתלויים בכוח כמו vinculin, tensin ו-kindlin נעדרים שם ברובם. לעומת זאת, בהדבקות מוקדיות, טלין אוחז גם באתרי קירבה וגם באתרי מרחק על הזנב והממברנה, ותומך בכוחות משיכה חזקים אך חוסם את גישת FCHo2 לאותו אזור.
מה זה אומר להתנהגות התא
לצופה שאינו מומחה, המסר של עבודה זו הוא שהתאים נושאים שתי "מצבי אחיזה" נפרדים להיצמדות לסביבתם. באזורים שטוחים וקשים הם משתמשים בהדבקות מוקדיות מונעות טלין שנבנו למשיכה חזקה. במבנים רכים, סיביים ומעוקלים הם עוברים להדבקות מעוקלות מונעות FCHo2 שמייצבות את אינטגרין αvβ5 בכוחות נמוכים הרבה יותר. שינוי זעיר בסדרת האינטגרין — והאם אתר זה עבר שינוי כימי — עוזר להכריע איזה מצב ישמש. המערכת הכפולה הזו מאפשרת לתאים לפרש גם קשיחות וגם צורה בסביבות תלת-ממדיות, תוך השפעה על הדרך שבה הם נודדים, מארגנים רקמות, ואפשרית גם על האופן שבו הם חודרים במהלך מחלה.
ציטוט: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
מילות מפתח: אינטגרינים, היצמדות תאים, עיקום ממברנה, FCHo2, שלד תאי