Clear Sky Science · he
התרחבות קלונלית של תאי T ציטוטוקסיים CD8⁺ בקשר ל‑ARIA בעקבות טיפול בליקנמב
מדוע זה חשוב לאנשים עם אלצהיימר
ליקנמב הוא אחד התרופות הראשונות שיכולות לנקות עמילואיד מהמוח ולהאט במידה מתונה את איבוד הזיכרון במחלת האלצהיימר. עם זאת, בחלק מהמטופלים בטיפול זה מתפתחת נפיחות מוחית או דימומים זעירים במוח, שינויים הנראים ב‑MRI ומסווגים תחת המונח חריגויות הדמיה הקשורות לעמילואיד (ARIA). המחקר שואל שאלה קריטית עבור מטופלים ובני משפחותיהם: מה קורה במערכת החיסון כאשר מופיעה ARIA, והאם בדיקת דם פשוטה יום אחד תוכל לעזור לחזות מי בסיכון הגבוה ביותר?
ההבטחה והסיכון של טיפול חדש באלצהיימר
ליקנמב הוא נוגדן הניתן בעירוי המסתפק בקבצים של חלבון בשם עמילואיד‑בטא, סימן היכר של מחלת האלצהיימר. על ידי סיוע לגוף לנקות עמילואיד, הוא עשוי להאט במידה מתונה את התדרדרות הקוגניציה. אולם תועלת זו מלווה בסיכון בטיחותי: חלק מהאנשים מפתחים ARIA, שיכולה לכלול אזורים של נפיחות מוחית או דימומים נקודתיים. תופעות לוואי אלה מחייבות מעקב תכוף ב‑MRI ועלולות להגביל מי יזכה לקבל את התרופה. לא כולם חשופים באותה מידה—נשאים של וריאנט גנטי בשם APOE4 בסיכון גבוה יותר—אך הגנטיקה לבדה אינה מסבירה מדוע ARIA מתרחשת, במיוחד מוקדם לאחר תחילת הטיפול. מאחר שליקנמב מועבר דרך מחזור הדם, החוקרים הניחו כי מעקב צמוד אחר תאי החיסון בדם עשוי לחשוף סימני אזהרה מוקדמים או אפילו מנגנונים המקשרים בין הטיפול לפגיעה בכלי דם במוח. 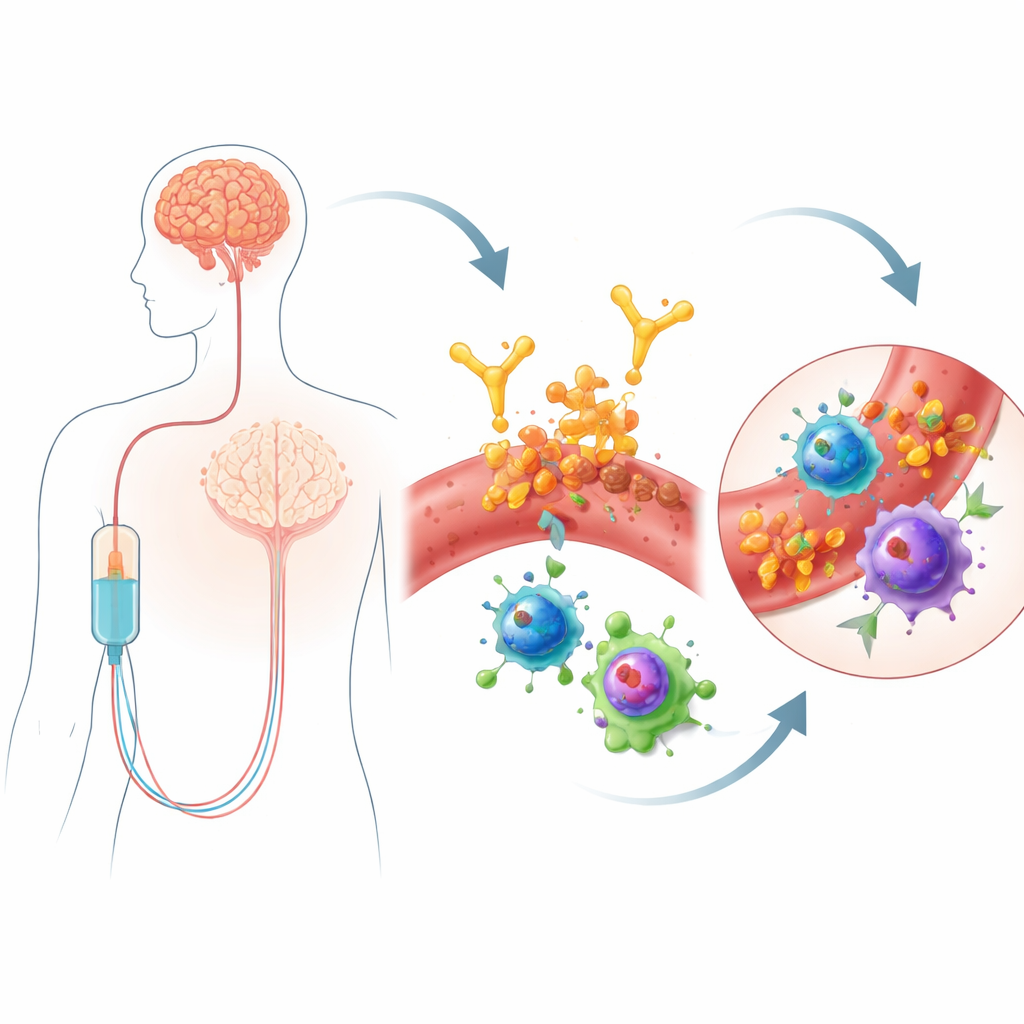
מעקב אחר תאי חיסון בחולים שאובחנו או לא אובחנו עם ARIA
החוקרים בחנו שישה אנשים עם אלצהיימר שהשתמשו בליקנמב במרפאת זיכרון אזורית. אצל שלושה מהם התפתחה צורות שונות של ARIA, ושלושה מתאימים (גיל, מין, גנוטיפ APOE ומספר עירויים דומים) לא פיתחו זאת. דמויות דם נלקחו מיד לפני העירויים, והצוות השתמש בגישה "מולטי‑אומית" מעמיקה: רצף RNA בתא יחיד כדי לקרוא אילו גנים דולקים באלפי תאי חיסון בודדים, תגי אנטי‑גוף כדי להגדיר סוגי תאים, רצף של קולטני תאי T כדי לעקוב אחרי קלונות, ומטבולומיקה ממוקדת כדי למדוד מאות מולקולות קטנות המעורבות במטבוליזם התאי. כך יכלו לשאול לא רק אילו סוגי תאים נוכחים, אלא עד כמה הם פעילים, איזה דלק הם משתמשים בו, והאם משפחות מסוימות של תאי T מתרחבות כתשובה לגירוי כלשהו.
התרחבות של תאי T קטלניים ממוכנים היטב
בהחולים שפיתחו ARIA צפה דפוס ברור. בהשוואה לקבוצת הבקרה, היתה להם חלקיות גבוהה יותר של תאי T מסוג CD8 "רוצחים" ופחות תאי T מסייעים מסוג CD4. בתוך מאגר ה‑CD8 בלטו שתי תת‑קבוצות: תאי זיכרון אפקטוריים וצורה דיפרנציאלית סופית הידועה כ־TEMRA. תאי TEMRA אלה דומים לחיילים ותיקים—מומחים מאוד להתקפה, עם מנגנון חזק להריגת תאים ממוקדים. בחולים החיוביים ל‑ARIA, תאי TEMRA היו רבים יותר, הראו הרחבה קלונלית גדולה יותר (כלומר משפחות תאי T מסוימות התכווצו), ונשאו תוכניות גנטיות הקשורות לציטוטוקסיות, להגירה דרך כלי דם ולסימנים של גירוי כרוני. מצבים דומים של תאי T נצפו בזקנה, בזיהומים כרוניים, ברביעיית מערכת העצבים (MS), ובנוזל השדרתי של אנשים עם אלצהיימר, שם הם יכולים להצטבר קרוב לכלי דם ולמשטח המוח.
שינוי מטבולי ותקשורת רוחבית עם תאי חיסון אחרים
הצוות גם מצא כי תאי ה‑CD8 האפקטוריים האלה שינו את המטבוליזם שלהם. במקום להסתמך בעיקר על ייצור אנרגיה יעיל במיטוכונדריה, הם הוסטו לכיוון גליקוליזה, דרך מהירה אך פחות יעילה לייצור אנרגיה התומכת בפעילות עוצמתית קצרת‑טווח. מדידות מטבוליטים בתאי דם תמכו בממצא: רמות החומצה הלקטית והפירובט עלו, בעוד רכיבים מרכזיים של מעגל חומצת החלב (מעגל חומצת הטריקרבוקסילית) הופחתו—דפוס טיפוסי של תאים חיסוניים דלקתיים. המונוציטים, סוג נוסף של תאי דם לבנים, הראו שינויים משלימים. בחולים החיוביים ל‑ARIA, מונוציטים הפעילו גנים להצגת אנטיגנים, להיצמדות לתאים אחרים ולהפקת כימוקינים—אותות כימיים שמושכים תאי T. מודלים חישוביים של זוגות ליגנד‑קולטן הציעו כי המונוציטים שולחים אותות חיזוק והכוונה חזקים יותר לתאי אפקטור CD8, ויוצרים סביבה המעודדת את תאי הרוצחים הללו לעסוק בדפנות כלי הדם.
קודי כתובת שמכוונים תאי T לכלי דם במוח
מאחר שהמחקר דגם רק דם, החוקרים פנו לסט נתונים עצמאי של תא יחיד ממרקמות מוח של מטופלים שטופלו בליקנמב כדי לבדוק האם אותן תוכניות תאי T מקושרות לנישות וסקולריות במוח. כאשר הם הקרינו את תת‑הקבוצות של CD8 על מפת המוח הזו, תאי TEMRA ותאי הזיכרון האפקטוריים מהחולים החיוביים ל‑ARIA הראו "קודי כתובת" תמלוליים—שילובים של מולקולות הידבקות וקולטני כימוקינים—שתאמו תאי אנדותל (תאי כלי דם) במוח החולה. החתימות הללו מרמזות שהתאי רוצחים המורחבים אינם רק חמושים וממונעים מטבולית, אלא גם מוכנים להגיע ולהתקשר עם כלי דם מוחיים במתח באתרים של ניקוי עמילואיד. 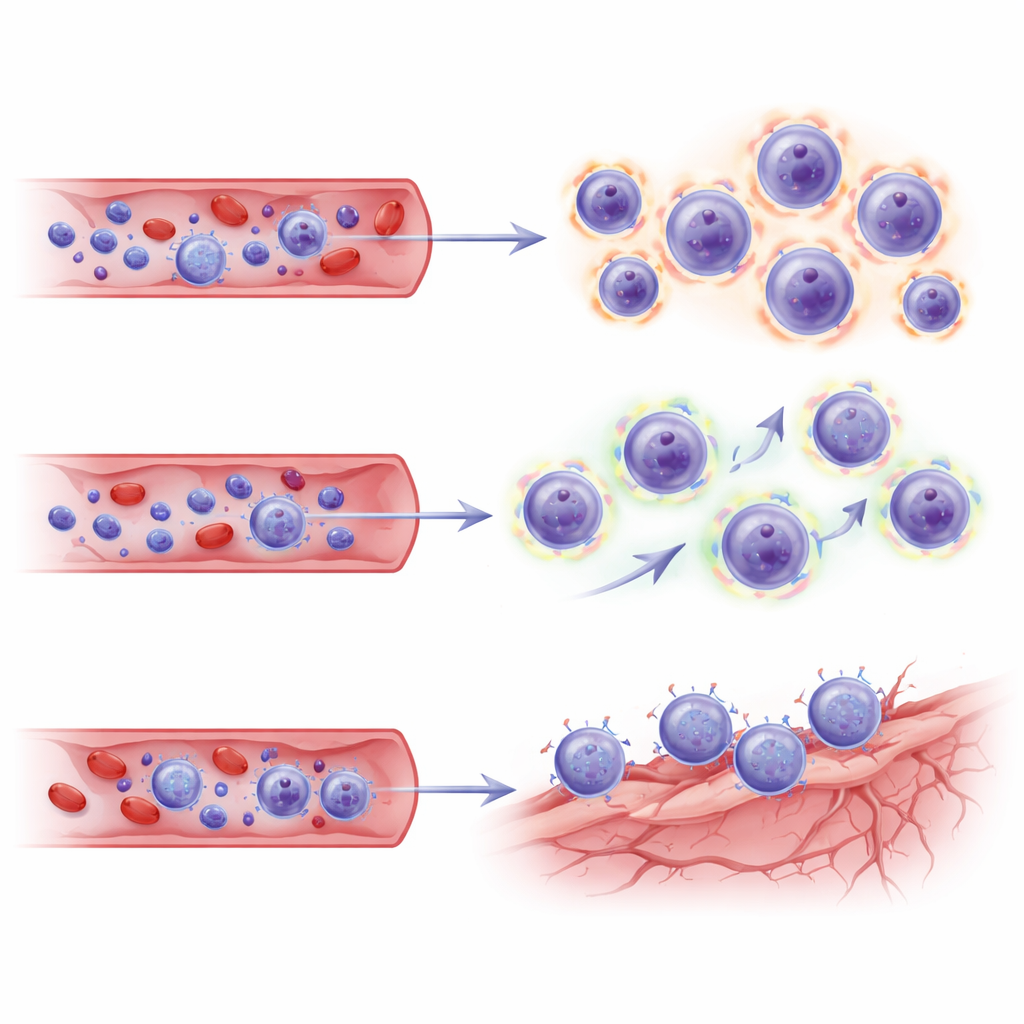
מה זה עשוי להצביע עבור מטופלים וטיפול עתידי
במבט כולל, המחקר הקטן אך המפורט הזה מצייר את ARIA כיותר מתופעת לוואי פסיבית של הסרת עמילואיד. במקום זאת, נראה שהיא מקושרת לתגובה חיסונית מתואמת בדם: הרחבה והפעלה מטבולית של קלונות ספציפיים של תאי רוצח CD8, איתות מחוזק מהמונוציטים ותכונות מולקולריות המעדיפות אינטראקציה עם כלי דם במוח. העבודה אינה מוכיחה שהתאים האלה גורמים ל‑ARIA—השינויים החיסוניים עשויים להיות תגובה לפגיעה כלי דם במקום להיות המקור—אבל היא מספקת השערות שניתן לבדוק ותוכנית לאבן דרך לביומרקרים מבוססי דם. בעתיד, מדידת השפע ומצב המטבוליזם של תאי CD8 TEMRA, יחד עם מולקולות איתות מרכזיות, עשויה לעזור לזהות מטופלים בסיכון הגבוה ביותר ל‑ARIA, לכוון לוחות זמנים למעקב או אפילו לעודד אסטרטגיות ממוקדות כדי לדכא זמנית את התגובה החיסונית הזו תוך שמירה על היתרונות של טיפולים המנקים עמילואיד.
ציטוט: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
מילות מפתח: מחלת האלצהיימר, ליקנמב, תאי חיסון, כלי דם במוח, תופעות לוואי של טיפול