Clear Sky Science · he
פפטיד קריפטי נוירוטוקסי הנובע מספלייסינג קריפטי של PKN1 התלוי ב‑TDP-43
איומים נסתרי בתוך תאי המוח
מחלות מוח רבות, כולל טרשת איזוטורפית נוירון מוטורי (ALS) ומחלת אלצהיימר, מאופיינות בצבירים של חלבון בשם TDP-43. מדענים יודעים שכאשר חלבון זה מפסיק לתפקד כראוי, תאי העצב מאבדים מסרים חיוניים ולבסוף מתים. המחקר הזה חושף תפנית מפתיעה נוספת: כישלון ב‑TDP-43 יכול גם לגרום לתאים המוחיים לייצר מיני‑חלבון רעיל שלא היה ידוע קודם, שממנו נגרם נזק למעגלי זיכרון. הבנת השחקן הנסתר הזה עשויה לפתוח דרכים חדשות לאבחון וטיפול בדמנציות הרסניות.
איך קורא הכתיב התאי שומר על סדר ב‑RNA
בתוך הנוירונים, TDP-43 פועל כעורך כתיב ל‑RNA, ההודעות התיווך שבין DNA לחלבונים. הוא נקשר לרצפים קצרים ספציפיים ומונע הכנסת "חלקים נוספים" מזדמנים לאותן הודעות. כאשר TDP-43 אובד או מוסב ממקומו, כפי שקורה ב‑ALS ובמקרים רבים של אלצהיימר, חלקים נוספים אלה — הנקראים אקסונים קריפטיים — עלולים להיכנס ל‑RNA. עד כה רוב האקסונים הקריפטיים הידועים גרמו פשוט לאובדן חלבון תקין בכך שהפכו את ההודעה ללא יציבה והובילו להשמדה מהירה שלה. לא היה ברור האם אירועים כאלה גם יכולים לייצר חלבונים חדשים ופוגעניים.
ספלייסינג קריפטי יוצר שבר רעיל
החוקרים התרכזו בגן בשם PKN1, שעוזר לשמר את השלד הפנימי וזרימת האיתות בנוירונים. בעזרת מודלים תאייים שבהם הוקטן TDP-43, הם גילו אקסון קריפטי שלא זוהה קודם, שכינו אותו PKN1‑5a1, שהוכנס בין שני מקטעים רגילים של RNA של PKN1. הכנסת זו הציגה אות עצירה מוקדמת, וגרמה ליצירת RNA מקוצר. באופן בולט, חלק מההודעה הפגומה הזו ניצלה את מערכת בקרת האיכות של התא ויתורגם לקטע יציב של חלבון PKN1 המכיל רק את 207 חומצות האמינו הראשונות שלו. הקבוצה קראה לתוצר המקוצר הזה PKN207. הם הראו ש־TDP-43 בדרך כלל מונע את הטעות הזו על‑ידי קשירה לכמה אזורים עשירים ב‑UG שמקיפים את האקסון הקריפטי; כאשר קשירה זו אובדת, האקסון נכנס בספלייסינג ו‑PKN207 מיוצר.
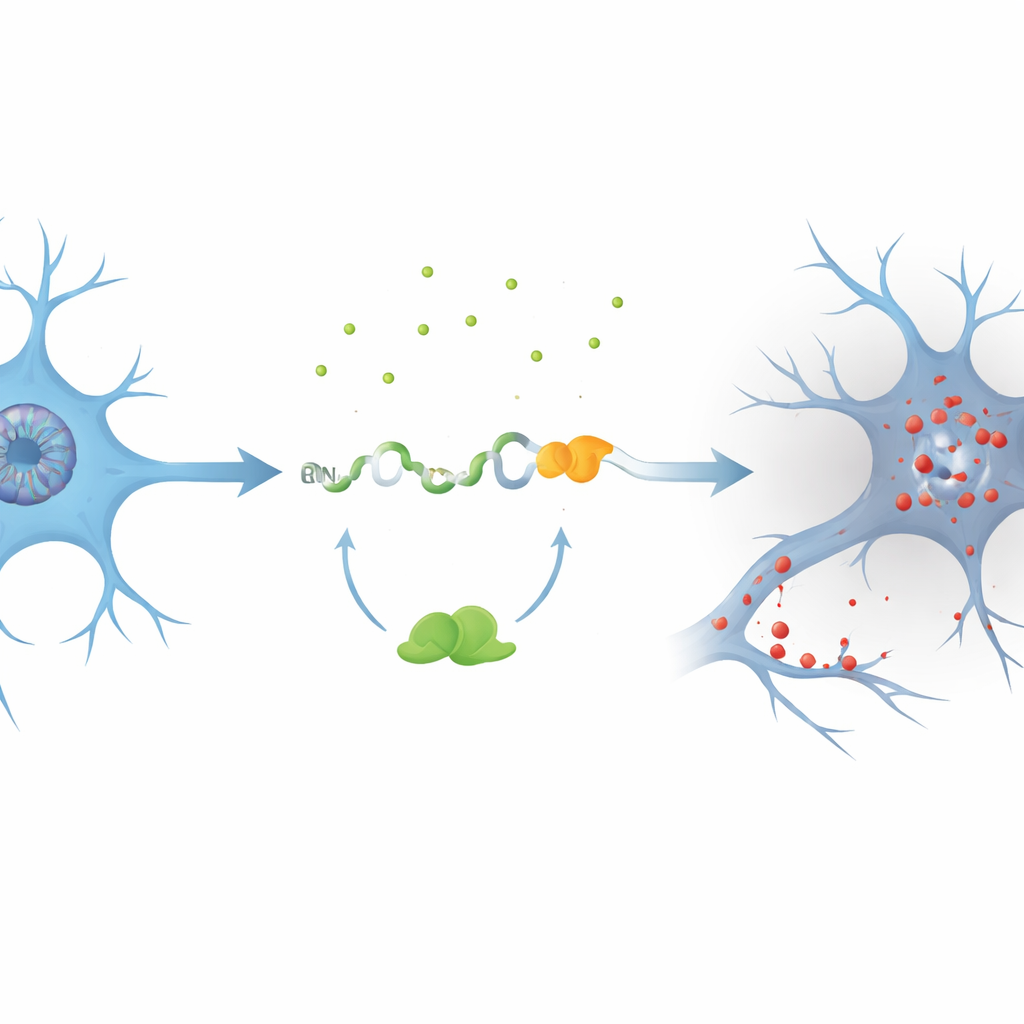
ראיות מתוך מוחי חולים ומאגרי נתונים גדולים
כדי לבחון האם האירוע הזה מתרחש במחלה אנושית, החוקרים כרו נתוני רצף RNA ממאות דגימות מוח וחוט שדרה של חולי ALS. הם מצאו הפעלה נרחבת של האקסון הקריפטי PKN1‑5a1 באזורים הידועים כנגועים בפאתולוגיה של TDP-43, כגון הקורטקס המוטורי וחוט השדרה, אך לא במח העצם שנשמר יחסית (הצרבלום). לאחר מכן הם פיתחו נוגדנים מאוד ספציפיים שמזהים רק את הזנב הייחודי של PKN207, ולא את חלבון PKN1 באורך מלא. ברקמה היפוקמפלית של חולי אלצהיימר שהציגו גם TDP-43 לא תקין ופוספורילציוני, נוגדנים אלה זיהו רצועה מובחנת המתאימה ל‑PKN207, בעוד שרצועה כזו נעדרה במוחות הבקרה. מאגרי נתוני אלצהיימר נוספים איששו שהאקסון הקריפטי מופעל אפילו בשלבי מחלה מוקדמים, מה שמרמז שהשגיאה המולקולרית הזו עלולה להתחיל זמן רב לפני שהתסמינים נהיים בולטים.
מיני‑חלבון בעל השפעה גדולה על הזיכרון
גילוי PKN207 במוח האדם החולה העלה את השאלה המרכזית: האם הוא מזיק? כדי לבדוק זאת, הקבוצה השתמשה בנגיפים לשם הבאת הביטוי של PKN1 רגיל או של PKN207 באופן ספציפי להיפוקמפוס — אזור מוחי קריטי לזיכרון — במכרסמים צעירים. חודשים לאחר מכן, שתי קבוצות העכברים הראו ליקויי למידה במבוך המים של מוריס, כשהם שוחים זמן ארוך יותר כדי למצוא משטח מוסתר. בנוזל השדרה שלהם נמצאו רמות גבוהות יותר של חלבון מבני, neurofilament light chain, סמן לנזק אקסונלי. בנוירונים בתרבית, הגברת PKN207 גרמה לפגיעה בתאים, כפי שנמדד בדליפת אנזים שמציינת נזק ממברנלי. פרופיל חלבוני מפורט של ההיפוקמפוס חשף שינויים רחבים במסלולים הקשורים לעוצמת הסינפסות (חיזוק לטווח ארוך) ולמחלות ניווניות ידועות, עם שיבוש חזק במיוחד במולקולות התומכות באיתות יעיל ובשלד הסיבי של העצבים.
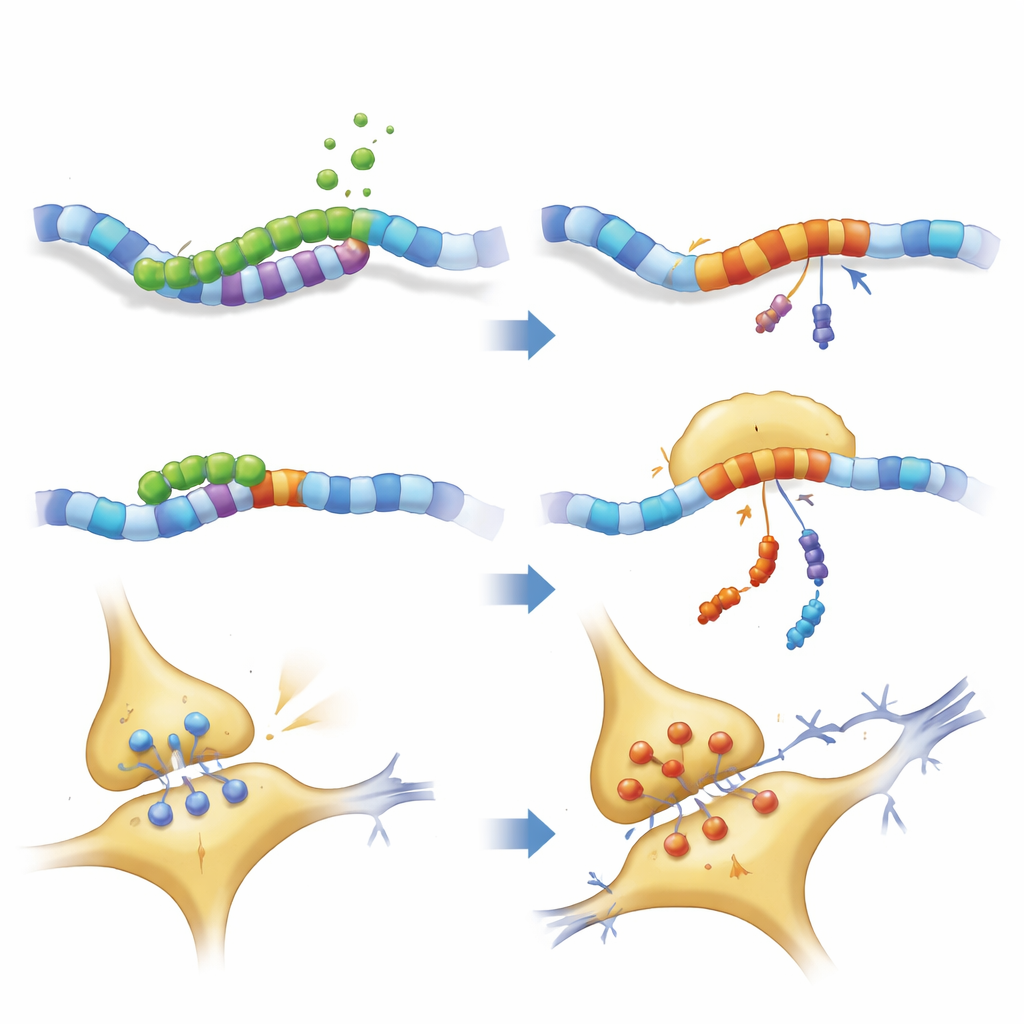
איך השבר ממוטט את חיבורי המוח
בחינה מדוקדקת של מבנה הנוירון הראתה שגם PKN1 במלואו וגם PKN207 הפריעו לרשת הנוירופילמנטים שמקנה לאקסונים את צורתם ועוזרת בהובלת מטען. חלבוני תנועה ושלד מרכזיים הופחתו, בעוד שחלק מרכיבי הנוירופילמנט הצטברו, מרמזים על צווארי בקבוק ותיתכן אגירה. הקלטות חשמליות מפרוסות היפוקמפליות איששו כי בעכברים שמביעים PKN207 יש חיזוק לטווח ארוך מוחלש — התהליך שבו סינפסות מתחזקות לאחר פעילות חוזרת ושהוא יסוד תאי מקובל ללמידה וזיכרון. אף על פי ש‑PKN207 חסר את תחום האנזים של PKN1, נוכחותו הספיקה לחקות ולפעמים לחרוג מהשפעות ההפרעה של החלבון המלא, מה שמעיד שהאזור ה‑N‑טרמינלי המשותף יכול בפני עצמו להפר את ההומאוסטזיס הנוירונלי.
מדוע גילוי זה חשוב למחלות מוח
עבודה זו מוסיפה שכבה חדשה להבנת ההפרעות הקשורות ל‑TDP-43. במקום רק לגרום לאובדן RNAs חיוניים, כישלון של TDP-43 יכול גם ליצור מיקרו‑חלבון יציב ורעיל שמתנגש בסינפסות ובקוגניציה. האקסון הקריפטי PKN1‑5a1 ומוצרו הפפטידי PKN207 בולטים כעת כסמנים פוטנציאליים של תפקוד מוקדם של TDP-43 וכמטרות מועמדות לטיפולים המתמקדים בתיקון הספלייסינג או בחסימת השבר המזיק. באופן רחב יותר, המחקר מציע כי אקסונים חבויים אחרים עלולים אף הם להוליד פפטידים שמניעים מחלה, ומכוון חוקרים לנוף עשיר — וגילויו הוזנח עד כה — של אשמים מולקולריים בניורודגנרציה.
ציטוט: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
מילות מפתח: TDP-43, ספלייסינג קריפטי, PKN1, נוירודגנרציה, אלצהיימר ו‑ALS