Clear Sky Science · he
שימוש אבולוציוני מחדש במעכב תיולאז מטבולי מאפשר ביוסינתזה של אנטיביוטיקה
איך מיקרובים יומיומיים ממציאים מחדש את הכימיה שלהם
הרבה מהאנטיביוטיקות והתרופות שעליהן אנו מסתמכים מיוצרות בשקט על ידי חיידקים. הכימאים הזעירים האלה משתמשים באנזימים — מכונות מולקולריות — כדי לבנות תרכובות הגנתיות מורכבות. המאמר חושף כיצד אנזים מרכזי מטבולי, שבעבר שימש למשימות תחזוקה תאיות בסיסיות, עבר כיוון אבולוציוני בחיידקי הפה כדי לייצר אנטיביוטיקה עוצמתית. הבנת המהפך הזה לא רק מגלה כיצד הטבע ממציא כימיה חדשה, אלא גם מספקת רמזים לתכנון תרופות וביокатליזטורים דורות הבאים.
ממתאבוליזם בסיסי לנשק כימי
כל התאים החיים תלויים בקבוצת אנזימים שמורות המנהלות את המטבוליזם המרכזי שלהם, כמו פירוק שומנים ובניית מולקולות חיוניות. אחת מהקבוצות הללו, שנקראת על-משפחת התיולאז, בדרך כלל מסייעת בטיפול במולקולות קטנות עשירות אנרגיה כמו אצטיל-CoA ותומכת בדרכים חיוניות ליצירת ליפידים ורכיבים תאיים אחרים. החוקרים גילו שבכמה מינים של Streptococcus בחלל הפה, קומפלקס תיולאז תלת-חלקי — המורכב מחלבונים הקרובים ל-HMGS, ACAT וחלבון מסייע שלישי — נטש את תפקידו המטבולי הקדמוני. במקום זאת, קומפלקס זה משלים כיום את הביוסינתזה של אנטיביוטיקה בשם reutericyclin A, שעוזרת לחיידקים אלה להתחרות בסביבת הפה הצפופה.
סוג חדש של תגובת אנזים על שלד אנטיביוטי
על ידי שחזור קומפלקס ה-Streptococcus במעבדה והזנתו בפרקורסור כימי מסונתז של reutericyclin A, החוקרים הראו שהקומפלקס מבצע תגובת חיבור פחמן–פחמן בלתי שגרתית הידועה כאצילציה מסוג Friedel–Crafts על פחמן. במקום לקשר קבוצת אצטיל לחמצן, כפי שעושים אנזימים רבים, הוא מציב קבוצה זו ישירות על אטום פחמן של טבעת pyrrolidine-2,4-dione — חלק מרכזי במבנה של reutericyclin. הקומפלקס מקבל גם תורמים טבעיים של אצטיל כמו אצטיל-CoA וגם מספר תורמים מלאכותיים, ואפילו יכול להריץ את התגובה בהיפוך, לשבור את הקשר שיצר. הגמישות הזו מרחיבה את הרפרטואר המוכר של אצילטרנספראזות ביולוגיות ומרמזת כיצד ניתן להתאים אנזימים כאלה לבניית מוצרים כימיים מגוונים.
שימוש מחודש במבנה חלבוני משומר
באמצעות מיקרוסקופיה הקריואלקטרונית ברזולוציה גבוהה, הצוות פתר את המבנה התלת־ממדי של קומפלקס ה-Streptococcus, שכונה SmaATase. למרות פונקצייתו החדשה, SmaATase שומר על דמיון ארכיטקטוני בולט לקומפלקס דומה בארכאיה המעורב במעבר המבלנואט לייצור ליפידים איזופרנואידים. שניהם הרכבים מולטימריים גדולים בנויים מחזרות של מודולים ומציגים חלל משותף שבו הקו-פקטור CoA יכול להיקשר ולהעבור בין אתרי הפעולה. עם זאת, שאריות קטליטיות מפתח הדרושות לתגובה המטבולית המקורית חסרות או הושמוּנו בגרסה החיידקית. בדיקות ביוכימיות מאשרות ש-SmaATase כבר אינה יכולה לייצר את המוצר הקדמוני HMG-CoA ובמקום זאת משתמשת באצטיל-CoA כתרומה בלבד לתת־המולקולות הקטנות החדשות שלה.
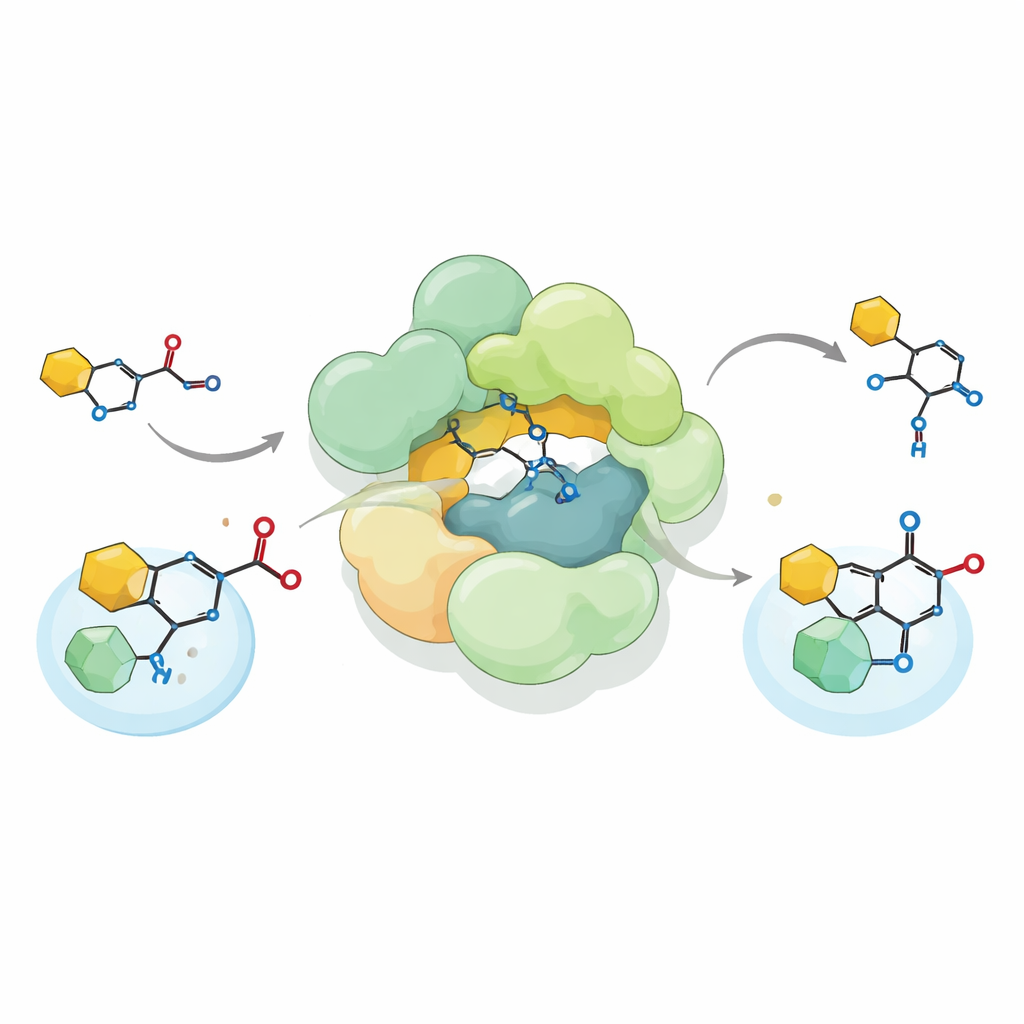
שביל אבולוציוני ממטבוליזם לאנטיביוטיקה
כדי להבין כיצד שימוש מחודש כזה התפתח, המחברים השוו רצפים ופעילויות של קומפלקסים קרובים ברחבי חיידקים וארכאיה רבים. הם זיהו למעלה מאלף אשכולות גנים המכילים את אותו טריו של סוגי האנזים. חלקם עדיין תומכים בכימיה התיולאזית הקלאסית; אחרים, כמו אלה ב-Pseudomonas, מזינים אנטיביוטיקות קטנות שונות. קומפלקס ייצוגי מ-Pseudomonas fluorescens נראה יושב בחלקו בדרך האבולוציונית הזו: הדומיין הדומה ל-HMGS בו מושבת, אך היחידה הדומה ל-ACAT עדיין מבצעת תגובה יותר קונבנציונלית על תת־מוצרים קושרי CoA. ב-SmaATase ובמקבילו של Pseudomonas שמייצר את התרכובת המגינה על יבולים DAPG, שינויים נוספים סביב אתר הפעולה כיוו את האנזימים לזהות מקבלים לא סטנדרטיים כגון טבעות ארומטיות או ליבות טטרמידיות.
מדוע קבוצת אצטיל זעירה עושה הבדל גדול
בסופו של דבר, התשואה הביולוגית של השינוי המולקולרי הזה ברורה. כשהצוות בדק את האנטיביוטיקות המסויידות reutericyclin A ו-DAPG מול פנל של חיידקים גרם-חיוביים, המולקולות הללו הראו פעילות קטילה חזקה, בעוד שמקדמיהם הלא מסויידים היו חלשים בהרבה או כמעט לא פעילים. קבוצת האצטיל הקטנה הזו, הממוקמת בדיוק במקום הנכון על ידי קומפלקס האנזימים הממועד מחדש, הופכת שלד צנוע לנשק עוצמתי, מה שמאפשר ל-Streptococcus בחלל הפה או ל-Pseudomonas סביב שורשי צמחים להתחרות ביתרון על פני שכנים. עבודה זו ממחישה כיצד האבולוציה יכולה למחזר מסגרות חלבוניות קיימות באמצעות מוטציות מינימליות אך אסטרטגיות, ולהפוך מכונה מטבולית שגרתית לכלי מיוחד להגנה כימית — ומספקת תבנית למהנדסים השואפים לעצב קטליזטורים חדשים ליצירת קשרי פחמן–פחמן לגילוי תרופות וביולוגיה סינתטית.
ציטוט: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
מילות מפתח: אבולוציית אנזימים, ביוסינתזה של מוצרי טבע, כימיה של אנטיביוטיקה, שימוש מחודש מטבולי, אצילציה מסוג פרידל–קראפטס