Clear Sky Science · he
מודל מבוסס iPSC אנושי של פיברוזיס ריאתי חושף שעיכוב p300/CBP מדכא את מצב התא המעברי האפטולרי
מדוע ריאות מסוידות חשובות לכולנו
פיברוזיס ריאתי אידיופתי (IPF) היא מחלה בלתי פוסקת שבה הריאות הופכות לאט לרקמת צלקת, מה שהופך כל נשימה לקשה יותר. התרופות הקיימות יכולות להאט את התהליך בלבד ולעתים גורמות לתופעות לוואי מטרידות. מחקר זה משתמש בכלי גנטיקה ותאי גזע מתקדמים כדי לשחזר ריאות מסוידות במעבדה, ושואל שאלה פשוטה אך חיונית: האם ניתן למצוא מתג שמסרב תאים ריאתיים פגועים ממצב מזיק וחוזר אותם לכיוון ריפוי?
חלון מעבדתי אל ריאה מסוידת
כדי לבדוק IPF, החוקרים בנו ריאות מיניאטוריות מתאי גזע פלוריפוטנטיים שהושרו (iPSCs) של אדם. ה‑iPSC הללו הוכוונו להפוך לתאי אלוואולר — התאים שמצפים את שלפוחיות האוויר הזעירות שבהן החמצן נכנס לדם — וגדלו יחד עם פיברובלסטים ריאתיים, תאי רקמת החיבור היוצרים את הצלקת. מובלים בתוך ג׳ל רך, "אורגנואידים אלוואולריים" אלה התנהגו בדומה לרקמת ריאה אמיתית. כשנחשפו לסרטן הכימותרפי בליאומיצין, מגרה מוכר של פגיעה ריאתית, הג׳לים התקצרו כאשר הפיברובלסטים משכו אותם, מחקים את כיווץ הרקמה הנראה בפיברוזיס.
באמצעות מערכת זו, הצוות סקר ספרייה של 264 מולקולות קטנות ומדד באופן אוטומטי כמה כל תרופה מנעה כיווץ הג׳ל, עם כלי ניתוח תמונה מבוסס למידה עמוקה שסיפק קריאות אובייקטיביות. רבות מהחומרות לא הראו השפעה, אך משפחה אחת בלטה בבירור: מעכבים של החלבונים p300 ו‑CBP, המסייעים לשלוט באריזת ה‑DNA ובאילו גנים הופעלים. כל שמונת תרכובות המיועדות ל‑p300/CBP בספרייה הפחיתו כיווץ במינונים נמוכים, מה שמדגיש את המסלול הזה כיד תקווה לטיפול בפיברוזיס. 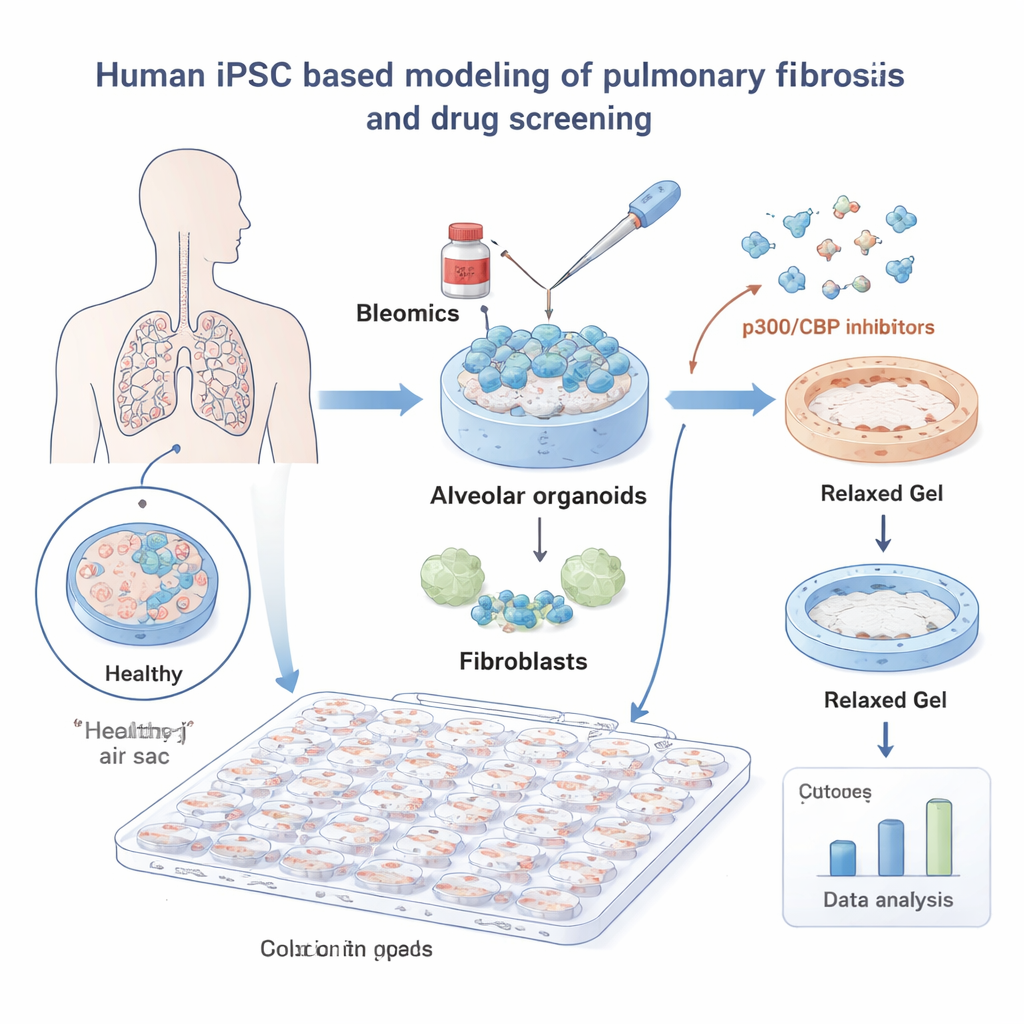
המטרידים: תאים ריאתיים במצב מעבר
עבודות אחרונות חשפו סוג תא "בין־בינוני" בעייתי בריאות חולות, הנקרא מצב התא המעברי האלוואולרי. בדרך כלל, תאי תמיכה הידועים כ‑AT2 מתמיינים לתאי AT1 דקים במיוחד שמכסים את שלפוחיות האוויר ומאפשרים חילוף גזים. ב‑IPF, עם זאת, תאי AT2 לעתים רבים נתקעים במצב המעברי הזה, מבטאים גנים הקשורים ללחץ ולתיקון בעוד שאינם משלימים את המעבר לתאי AT1 תפקודיים. תאים מעברים אלה מצטברים באזורים פיברוטיים ומתקשרים בעוצמה עם הפיברובלסטים, אך לא היה ברור האם הם רק תוצאה נלווית של הנזק או גורמים פעילים של הצלקת.
על ידי רצף RNA ופרופילינג של כרומטין פתוח באורגנואידים שלהם, המחברים הראו שהתאים המעברים שעולים במודל שלהם התאימו במדויק לאלה שנמצאו בריאות של חולים עם IPF. תאים מחוללים אלה הציגו חתימות גנטיות של לחץ, דלקת ושיקום מטריצה, והם הפעילו בחוזקה פיברובלסטים ריאתיים מבוגרים שנמצאו איתם במגע. באופן מכריע, כאשר p300/CBP נחסם, הסמנים של המצב המעברי ירדו, זהות ה‑AT2 נשמרה טוב יותר, והפעלת הפיברובלסטים נחלשה. במילים אחרות, התרופות לא הרעילו תאים באופן כללי; במקום זאת, הן מנעו באופן סלקטיבי מתאי AT2 להיתפס במצב המעבר המזיק הזה.
פיענוח מתגי המולקולרים
כדי להבין כיצד p300/CBP מעצב את החלטת הגורל הזו, הצוות בחן סימנים כימיים על היסטונים — חלבונים המסייעים באריזת ה‑DNA. סימן מסוים, אצטילציה של H3K27, מונח לעתים קרובות על‑ידי p300/CBP באזורים משופרים ופרומוטרים פעילים. בתאים המעברים, אזורים סמוכים לגנים של תגובת לחץ ופרו‑פיברוטיים נשאו אצטילציה חזקה ב‑H3K27 והיו מועשרים לאתרי קשירה של גורמי שעתוק כגון AP‑1 ו‑HNF1B. כאשר תאים טופלו במעכבי p300/CBP, סימני האצטיל הללו פחתו באתרים אלה וביטוים של גנים רבים פרו‑פיברוטיים ירד. חסימת AP‑1 ישירות, או הפחתת AP‑1 ו‑HNF1B בעזרת RNAi, גם כן צמצמה את התוכנית המעברית וכיווץ האורגנואידים, וקשרה את הטריו—p300/CBP, AP‑1 ו‑HNF1B—למנוע שמניע את ההתארגנות הפיברוטית.
מעבר למאגר, המחקר בדק מעכב אחד, CBP30, בעכברים עם פגיעה ריאתית שנגרמה על‑ידי בליאומיצין. בעלי החיים שקיבלו CBP30 הראו פחות תאים אפיתליאליים במצב מעבר, פחות הפעלה של מיופיברובלסטים היוצרים צלקת ובהפחתה בביטוי סמני פיברוזיס. אימות זה בין מודלים אנושיים מבוססי תאי גזע לבין מודל חיה מחזק את הטענה ש‑p300/CBP אינו רק ארטיפקט מעבדתי אלא רגולטור אמיתי של היווצרות צלקת בריאה. 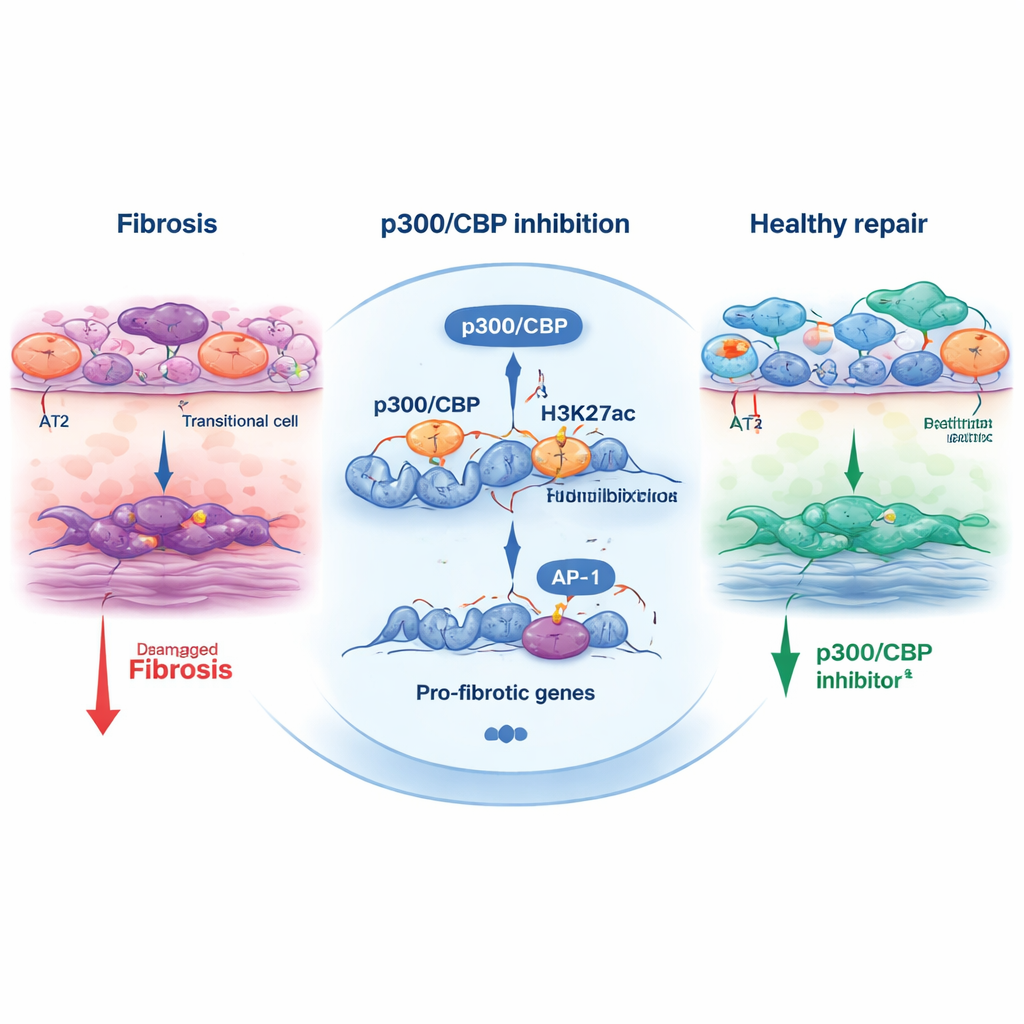
מה משמעות הדבר לטיפולים עתידיים
ללא‑מומחים, המסקנה המרכזית היא שהמחברים בנו מודל אנושי מציאותי של ריאות פיברוטיות והשתמשו בו כדי להאיר יעד תרופתי חדש. עבודתם מרמזת כי צלקת ריאתית מונעת בחלקה על‑ידי מצב תאי מעבר הפיך, מופעל לחץ, שמטעה את הרקמה הסובבת. על‑ידי השתקת p300/CBP, ייתכן שניתן לשכך מצב זה, לשמור על תאי האלוואולה במסלול התפתחותי בריא ולהפחית את האותות שדוחפים את הפיברובלסטים לעבודה מופרזת. בעוד שמעכבי p300/CBP צריכים עדיין לעבור אופטימיזציה לבטיחות וניסויים קליניים, המחקר הזה מצביע על טיפולים המתייחסים לשורש התקשורת התאית השגויה ב‑IPF במקום רק להאט את השלכותיה.
ציטוט: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
מילות מפתח: פיברוזיס ריאתי אידיופתי, אורגנואידים אלוואולריים, מעכבים של p300/CBP, תאי אפיתל מעבריים, תאי גזע ריאתיים