Clear Sky Science · he
מנגנון ננו-מבוסס-DNA החושב על איתות פורינרגי ומניע מתג חיסוני להחלטת דלקת
הנמכת מערכת האיתות של הגוף
כאשר הרקמות שלנו ניזוקות, תאים משחררים התפרצות של "אותות אזעקה" כימיים שמזמינים תאי חיסון להילחם בזיהום ולנקות שברי רקמה. תגובה זו חיונית, אך אם האזעקה פועמת חזק מדי או למשך זמן רב מדי, היא עלולה להניע דלקת מזיקה בריאות, בכליות ובאיברים אחרים. המחקר הזה מתאר מכשיר זעיר, ניתן לתכנות ובנוי מ-DNA, שיכול לחוש כשהאות חזק מדי ולבהיל אותו בעדינות, ועוזר למערכת החיסון לעבור ממצב התקפה למצב ריפוי.
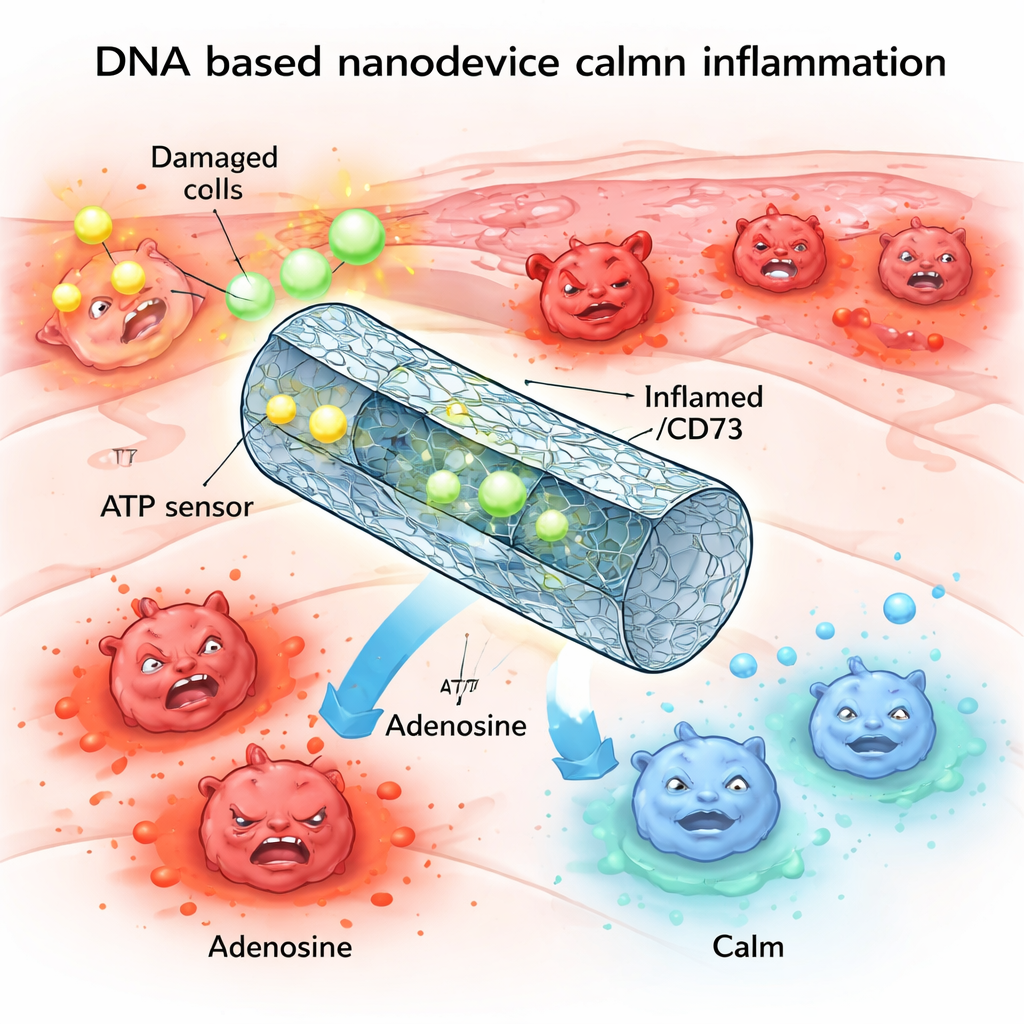
אות כימי שיכול להחריף יתר על המידה
אחד המולקולות המרכזיות של מערכת האזעקה בגוף הוא ATP, הידועה בעיקר כ"מטבע האנרגיה" בתוך התאים. בעת פציעה או מתח, כמויות גדולות של ATP דולפות מתאים פגועים אל המרחב החוץ-תאי. שם, ה-ATP החוץ-תאי פועל כאות מצוקה, נקשר לקולטנים על תאי החיסון ודוחף אותם למצב דלקתי חמור. בתנאים בריאים, אנזימים על פני התאים מפרקים במהירות ATP עודף לאדנוזין, מולקולה קרובה שמנחמת ובעלת השפעה נוגדת דלקת. אך במחלות דלקתיות כרוניות או חמורות רבות, מכונת פירוק זו פגומה, מה שמשאיר רמות ATP גבוהות, אדנוזין נמוך ורקמות תקועות במחזור של נזק.
בנייה של צינור DNA חכם
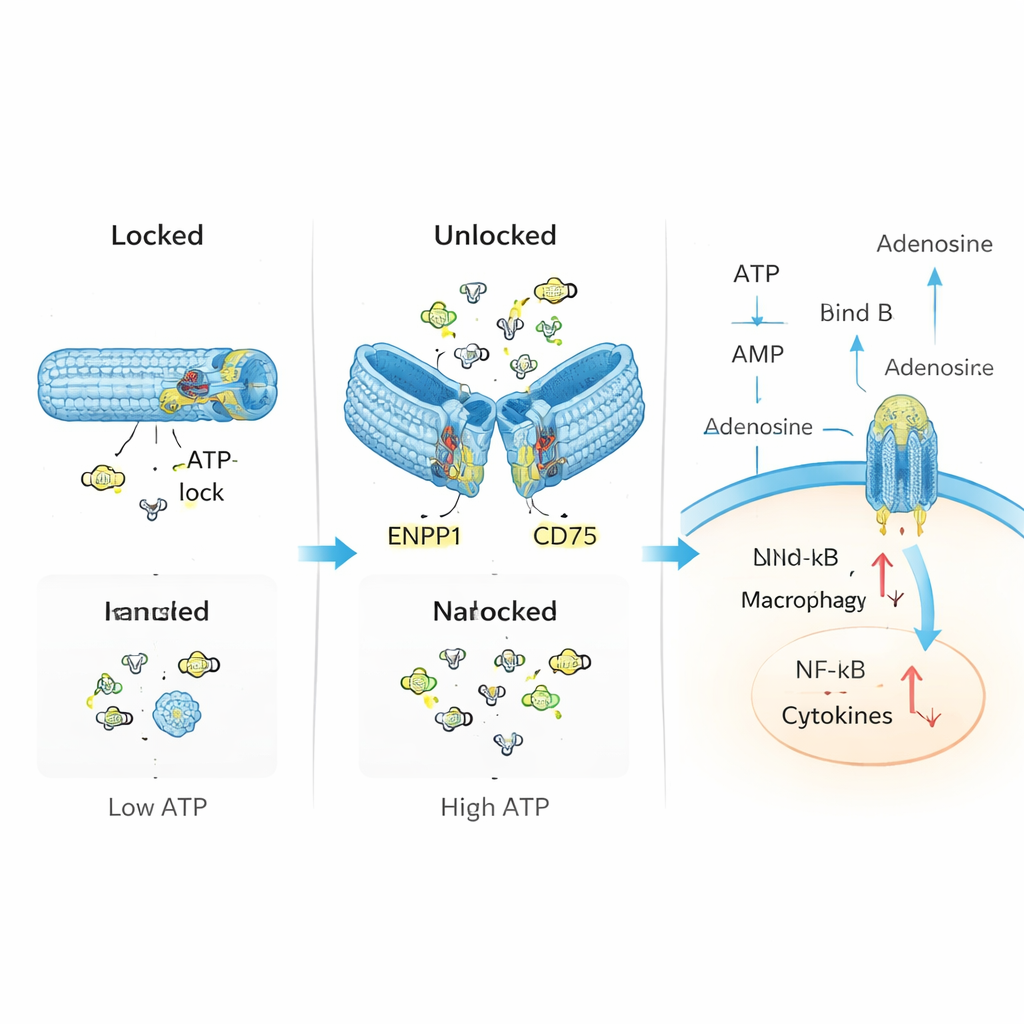
החוקרים שאפו לחקות ולתקן מערכת בקרה טבעית זו באמצעות ננוטכנולוגיית DNA. הם בנו צינור חלול מ-DNA, מקופל בדומה לאוריגמי, וציודו בשני רכיבים עיקריים: "חיישנים" שמזהים ATP, ואנזימים ההופכים ATP לאדנוזין. במצב מנוחה ונעילה, הצינור מוחזק סגור על-ידי מקטעי DNA קצרים המשמשים גם כחיישני ATP. כאשר רמות ה-ATP עולות מעל סף מסוים אופייני לרקמות פגועות, ה-ATP נקשר למקטעים אלה, גורם לצינור להיפתח ולחשוף את האנזימים ENPP1 ו-CD73 שבפנים. אלו לאחר מכן מפרקים את ה-ATP העודף ומייצרים אדנוזין, ומשנים בעדינות את האיזון הכימי המקומי מאיתות סכנה לאיתות פתרון.
הוכחת פעולת המתג
בניסויים מבוקרים במעבדה, הצוות אישר שהצינור ה-DNA נשאר סגור ברמות ATP נמוכות אך נפתח באמינות כאשר ה-ATP נעשה בשפע, בדומה לוולב חירום. לאחר ניעולו, המכשיר ממיר בעקביות ATP לתוצרים ביניים ולבסוף לאדנוזין, מבלי לפגוע משמעותית בפעילות האנזימים. בתאי חיסון החשופים ל-ATP גבוה, הננו-מכשיר הקטין תוצרים רעילים במיטוכונדריה, הפחית פעילות של מסלולי דלקת כגון NF-κB והאינפלמזום NLRP3, וחיזק איתותים הקשורים לפעולות המרגיעות של אדנוזין. במילים אחרות, המכשיר עשה יותר ממחיקת ATP; הוא שינה בפועל את התנהגות התאים ממצב דלקתי לרגולטורי.
נסיעה אל אתרי הפציעה
עיצוב מתג חכם הוא דבר אחד; להביא אותו למקום הנכון בגוף הוא דבר אחר. כדי לפתור את בעיית ההעברה הזו, החוקרים חיברו את צינורות ה-DNA שלהם למשטח מונוציטים נעים בדם, סוג של תאי דם לבנים שנוטים באופן טבעי להגיע לרקמות דלקתיות. באמצעות עוגן DNA מקושר כולסטרול, הם "חנו" כמויות גדולות של ננו-מכשירים על ממברנת כל תא, שם המכשירים נשארו בעיקר על פני השטח במקום להיספג לתוך התא. במודלים עכבריים של פציעה חדה בריאה ובכליה, מונוציטים אלה ובעלי הדקורציה הצטברו באיברים הפגועים באופן יעיל בהרבה מאשר מכשירים צפים חופשיים, והננו-מכשירים עדיין הגיבו באופן ספציפי ל-ATP גבוה ברקמות הפגועות.
סיוע לרקמות להחלים
בעכברים עם פציעות ריאה או כליה שנגרמו בכימיקלים, טיפול במכשיר ה-DNA הפחית נזק רקמתי, הצטברות תאי חיסון ומולקולות שליח דלקתיות. הגרסה הנשאת על-ידי מונוציטים עבדה הכי טוב, והציעה הגנה חזקה יותר מאשר המכשיר החופשי או האנזימים לבדם. אנליזות גנטיות ומטבוליות מעמיקות יותר של רקמת הריאה הראו שהגישה לא רק דכאה גנים דלקתיים אלא גם סייעה לשחזר מטבוליזם אנרגטי מופרע בתאים. מה שחשוב, המכשירים הראו רמות רעילות נמוכות ולא עוררו תגובות חיסוניות מזיקות בבעלי חיים בריאים.
מדוע זה חשוב לטיפולים עתידיים
עבור הקורא שאינו מומחה, המסר המרכזי הוא שעבודה זו מדגימה "תרמוסטט" מולקולרי ניתן-תכנות לדלקת. בנוי מ-DNA ואנזימים טבעיים, הננו-מכשיר חווה מתי אות הסכנה חזק מדי וממירה אותו אוטומטית לאות מרגיע, מסייע לתאי החיסון להירגע ולרקמות להתחדש. למרות שעדיין מדובר בשלבים ניסיוניים מוקדמים, האסטרטגיה הזו מציעה כיתת טיפולים חדשה שאינה חוסמת פשוט מסלולי חיסון בכל המקומות, אלא מאזנת מקומית את האיתותים הכימיים באתרים פגועים, ומאפשרת שליטה מדויקת על דלקת מזיקה במחלות רבות.
ציטוט: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
מילות מפתח: מכשיר ננו מבוסס DNA, ATP חוץ-תאי, דלקת, איתות אדנוזין, ננו-רפואה