Clear Sky Science · he
סידור אנטי-מקביל של פילי Csu מניע הרכבה תלת־ממדית של ביופילם ב‑Acinetobacter baumannii
כיצד חיידקי בית חולים בונים ערים ממוגנות
כמה מן החיידקים הבעייתיים בבתי חולים שורדים טיפול באנטיביוטיקה על ידי התגנבות לקהילות ריריות תלת־ממדיות בשם ביופילם. המחקר הזה שואל שאלה פשוטה אך חשובה: איך חיידקים בודדים משזרים עצמם למבנים חסונים ומרובדים כאלה? בעזרת הגדלה במיקרוסקופים אלקטרוניים מתקדמים, החוקרים חשפו "וולקרו" מיקרוסקופי העשוי סיבים שיערתיים שמאפשר לפתוגן המסוכן Acinetobacter baumannii לתפור את עצמו לצברי הגנה תלת־ממדיים. הבנת השלד החבוי הזה עשויה לפתוח דרכים לפרק ביופילמים ולשפר את יעילות התרופות הקיימות.
שיערות זעירות שמאחזות את החיידקים זה לזה
A. baumannii, גורם עיקרי לזיהומים בבתי חולים שקשה לטפל בהם, מצופה בשערות דקיקות על פני השטח הנקראות פילי Csu. עבודות קודמות הראו שפילי אלה חיוניים ליצירת ביופילמים קשיחים בצורת גוגמה, אך עד כה לא היה ברור איך הם מארגנים תאים למבנה תלת־ממדי. באמצעות כמה שיטות של מיקרוסקופיה אלקטרונית, המחברים אישרו תחילה שבתרבית נוזלית הפילי לרוב בולטים בנפרד מכל חיידק, כמו זיזים על פרגולה. בקולוניות צפופות שגדלו על משטחים, התמונה משתנה באופן דרמטי: פילי רבים עוטפים זה את זה בצפיפות, ויוצרים רצועות רחבות ושטוחות המחברות בין תאים שכנים, ויוצרות רשת עדינה לכאורה אך נרחבת בשלושה ממדים. 
סולמות שטוחים המבוססים על סיבים מזוגגים
כדי להבין כיצד רצועות אלה נוצרות, הצוות זיקה פילי Csu וטיפל בהתנהגותם לבד. במשך ימים עד שבועות, סיבים יחידים החלו להתחבר בזוגות ואז להתמזג לסופרסטאקים מרובי־סיבים, ולבסוף ליצור רשת ג'ל‑דומה שהעתיקה במדויק את המבנים שצפו בביופילם אמיתי. מיקרוסקופיה קריו־אלקטרונית ברזולוציה גבוהה חשפה את התכנון הבסיסי. כל פילוס אינו צינור חלק אלא מוט זיגזאגי. כאשר שני מוטות שוכבים זה לצד זה בכיוונים מנוגדים, הם נוגעים בנקודות פינה חוזרות, ויוצרים צמתי לטרל יציבים. זוגות אנטי־מקבילים רבים יכולים להתמקם זה אחר זה לאגד דק בדמוי יריעת־סרט—בע Essentially סולם או סרט מיקרוסקופי בעובי של סיב יחיד אך ברוחב של סיבים רבים.
תוכנית מוטמעת לצמיחה תלת־ממדית
המבנים המפורטים מראים כי היכולת להיצמד זה לזה מוטמעת בגיאומטריה של הפילי עצמם. דפוס הזיגזג חוזר על עצמו על מרחק קצר מאוד, ויוצר נקודות מגע רבות לאורך כל סיב. כתוצאה מכך, ברגע ששני פילי נפגשים בכיוון המתאים, שרשרת צמתים יכולה להיווצר כמו רוכסן ולהאריך במהירות את היריעה. חשובה העובדה שמיקום המוטות מבטיח שמגעים בדרך כלל ייתכנו בין פילי מתאים מתאים מתאים מתאיים מתאימים from different cells ולא מאותו תא, מה שמעודד קישור תא־לתא. הערימות נשארות גמישות וממתיחות, כך שהביופילם הצומח יכול לספוג מאמץ פיזי בלי להישבר. החוקרים ראו שבמהלך חלוקת התא, תאי הבת לעיתים קרובות מסתיימים כשהפילי שלהם ממוקמים פנים אל פנים, מצב שמעודד יצירת ערימות בדיוק במקום הנחוץ לקשירת התאים לאשכול תלת־ממדי. 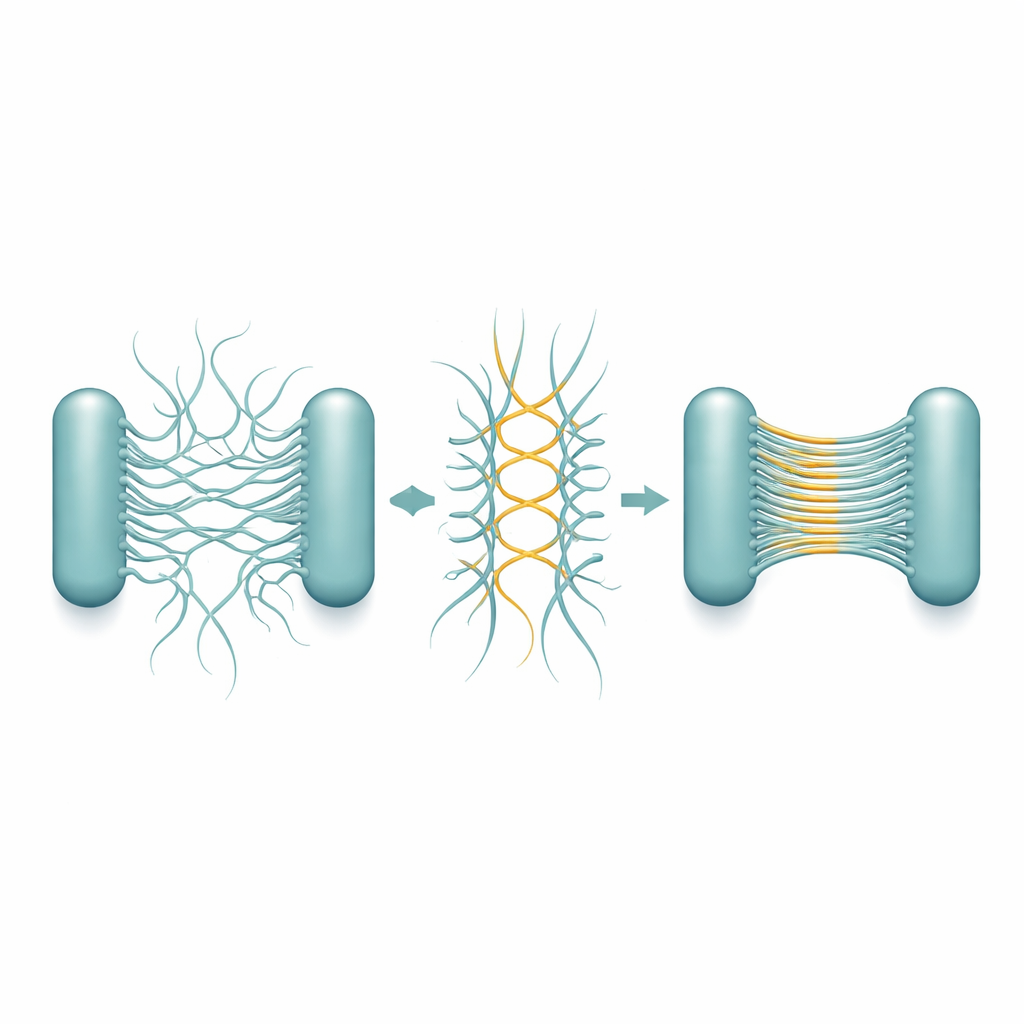
דבק, חומר מילוי ושלד ראשוני
המחקר בחן גם כיצד מרכיבים אחרים בביופילם תורמים למבנה. פולימר סוכרי בשם PNAG ו‑DNA רופף מתאים שנוצרו מתאים שבורים ידועים להצטבר בביופילם בוגר. מיקרוסקופיה הראתה חומרים אלה ממלאים את הפערים הצרים בין החיידקים ועוטפים את ערימות הפילי, בדומה לבטון שנשפך סביב זיון פלדה. עם זאת, כאשר הצוות הסיר את ה‑PNAG וה‑DNA, החיידקים עדיין יצרו רפסודות מאורגנות שמוחזקות בעזרת ערימות פילי Csu בלבד. זה מראה שהפילי בונים את השלד הראשוני, בעוד שהחומר המקיף מאוחר יותר צמתי ומייצב את המבנה.
נקודות תורפה חדשות במצודות החיידקים
במילים פשוטות, עבודה זו מסבירה כיצד A. baumannii משתמש בשיערות פני השטח שלו כדי לשזור את עצמו לצברים קשיחים ורב‑שכבתיים שקשה לתרופות ולתאי מערכת החיסון לחדור דרכם. הפילי פועלים תחילה כעוגנים שמתחברים למשטחים ואחר כך כרצועות גמישות המתערמות ליריעות שטוחות, הקושרות תאים שכנים בכל הכיוונים. פולימרים סוכרים ו‑DNA ממלאים את הפערים והופכים את רשת הרצועות למבצר איתן. על ידי זיהוי האופן המדויק שבו הפילי נדבקים זה לזה, המחקר מדגיש מטרה טיפולית חדשה: תרופות או מולקולות המשבשות את מגעי הפילי־על־פילי עשויות להחליש מבנים של ביופילם מבפנים ולהקל על סילוק זיהומים כרוניים של חיידקים.
ציטוט: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
מילות מפתח: ביופילם, Acinetobacter baumannii, פילי, עמידות לאנטיביוטיקה, מיקרוסקופיה קריו־אלקטרונית