Clear Sky Science · he
תגובות cGAS-IFN-I על ידי חילוץ DNA גרעיני מתאים גוססות באמצעות נוקלאוציטוזה
כיצד מערכת החיסון שלנו קוראת DNA מהמתים
כשתאים שלנו מתים במהלך זיהומים, סרטן או בלאי יום‑יומי, נשאריהם חייבים להיות מנוקים מבלי לעורר דלקת מוגזמת. מאמר זה חושף דרך מפתיעה שבה תאי חיסון יכולים למעשה לחפור לתוך גרעיני תאים גוססים, לשלוף משם את ה‑DNA ולהשתמש בו כאות סכנה. הבנת מערכת הניקוי‑והאזהרה החבויה הזו עשויה לשנות את התפיסה שלנו לגבי תרופות אנטי‑ויראליות, מחלות אוטואימוניות, טיפול בסרטן ותופעות לוואי של תרופות.
אזעקת DNA חבויה בתוך תאי החיסון
בתאים שלנו יש חיישן הנקרא cGAS שמזהה DNA במיקום הלא נכון — צף בציטוזול במקום להיות מוגן בגרעין או במיטוכונדריה. כשה‑cGAS נחשף ל‑DNA כזה, הוא מפעיל תוכנית אזעקה חזקה שמייצרת אינטרפרונים מסוג I, חלבונים מרכזיים בהגנה אנטי‑ויראלית ובבקרת החיסון. מדענים ידעו שוירוסים יכולים להכניס את החומר הגנטי שלהם לתאים ולגרום להפעלת הנתיב הזה, ושהיסטיונים של DNA עצמנו עלולים לדלוף ולגרום למחלות אוטואימוניות. אך נשארה חידה בסיסית: כיצד כמויות גדולות של DNA עצמאי, במיוחד מותאים גוססים, מגיעות ל‑cGAS מבלי להיהרס ב"קיבות" תאיות הנקראות ליזוזומים?
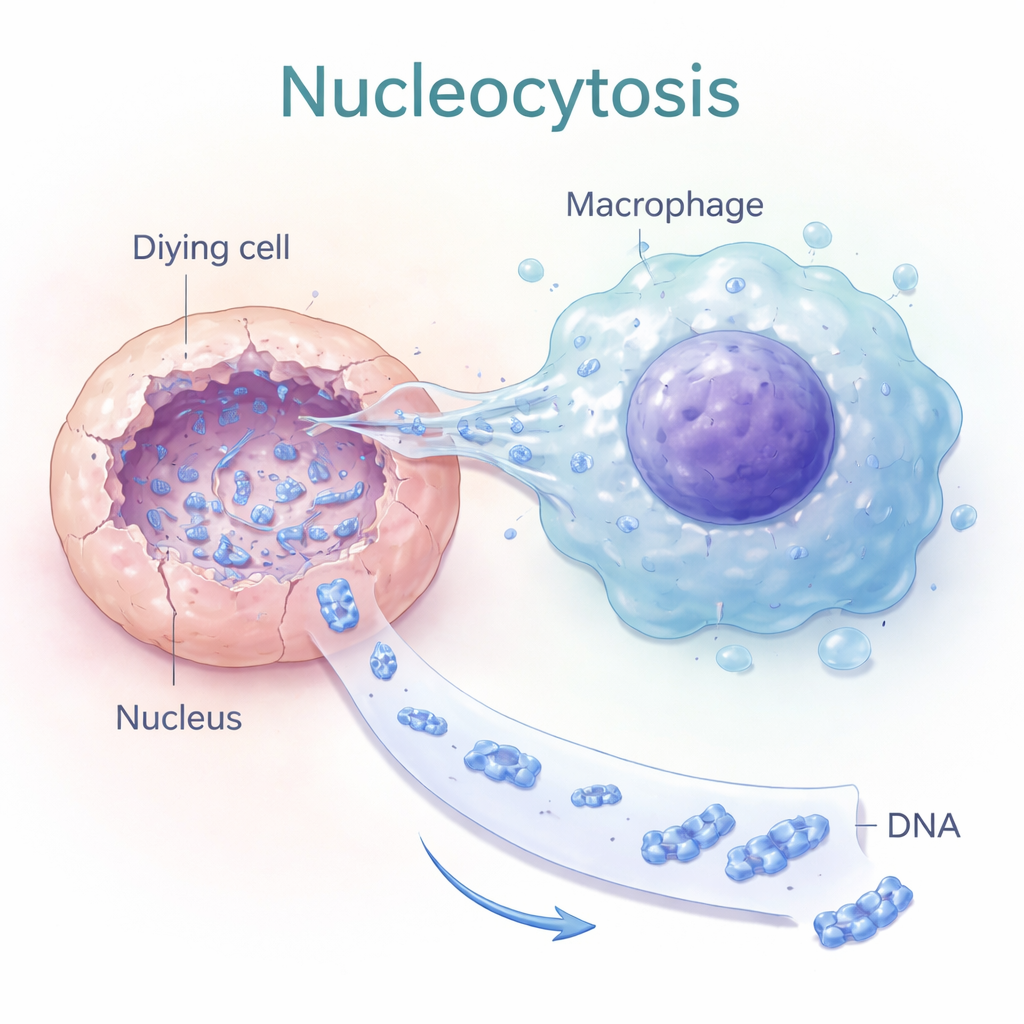
נוקלאוציטוזה: חפירה לתוך גרעיני תאים גוססים
המחברים גילו תהליך שהם מכנים "נוקלאוציטוזה", שבו מקרופאגים מסוימים — תאי חיסון שבדרך כלל בולעים פסולת — עושים משהו ממוקד הרבה יותר. במקום לבלוע תא מת שלם, הם מאריכים בליטות דקות בדמות אצבעות שנכנסות ישירות לגרעין התא המת. הדמייה של תאים חיים הראתה ירידה בעוצמת ה‑DNA בתוך גרעין התא המת ועלייה בעוצמת ה‑DNA בתוך המקרופאג המחובר, מה שמעיד על חילוץ פעיל של DNA גרעיני. העברה זו הייתה תלויה בשלד התאי (אקטין) ובמולקולות איתות ששולטות בצורת התא, מה שמרמז שנוקלאוציטוזה היא התנהגות מכנית מכוונת, לא דליפה פאסיבית.
מתי תרופות אנטי‑ויראליות מדליקות את אזעקת ה‑DNA
במהלך מגפת COVID‑19 נבדקו תרופות כמו הידרוקסיכולורוקווין ברוחב, אך הפעולות המדויקות שלהן בגוף נשארו עמומות. החוקרים מצאו שהידרוקסיכולורוקווין וכמה תרופות קשורות הידרופוביות‑קטיוניות יכולות להפעיל בחוזקה את ציר cGAS–STING–אינטרפרון — אך רק בתת‑אוכלוסייה של מקרופאגים. תרופות אלה מופרעות את הליזוזומים על‑ידי העלאת ה‑pH שלהם וחסימת אנזים בשם PPT1, שמסייע לפרק תגים שומניים על חלבונים. ההשפעה המצטברת דוחפת חלק מהתאים לצורת מוות מיוחדת שבה חלבון בשם קלרטיקולין מצטבר בגרעין. מקרופאגים נוטים להאריך בליטות לכיוון גרעינים עשירים בקלרטיקולין, לחלץ DNA באמצעות נוקלאוציטוזה, ולהפעיל ייצור אינטרפרון עז בעד כמה תאים — מספיק כדי ליצור אות אנטי‑ויראלי מקומי חזק מבלי להציף את כל הגוף.
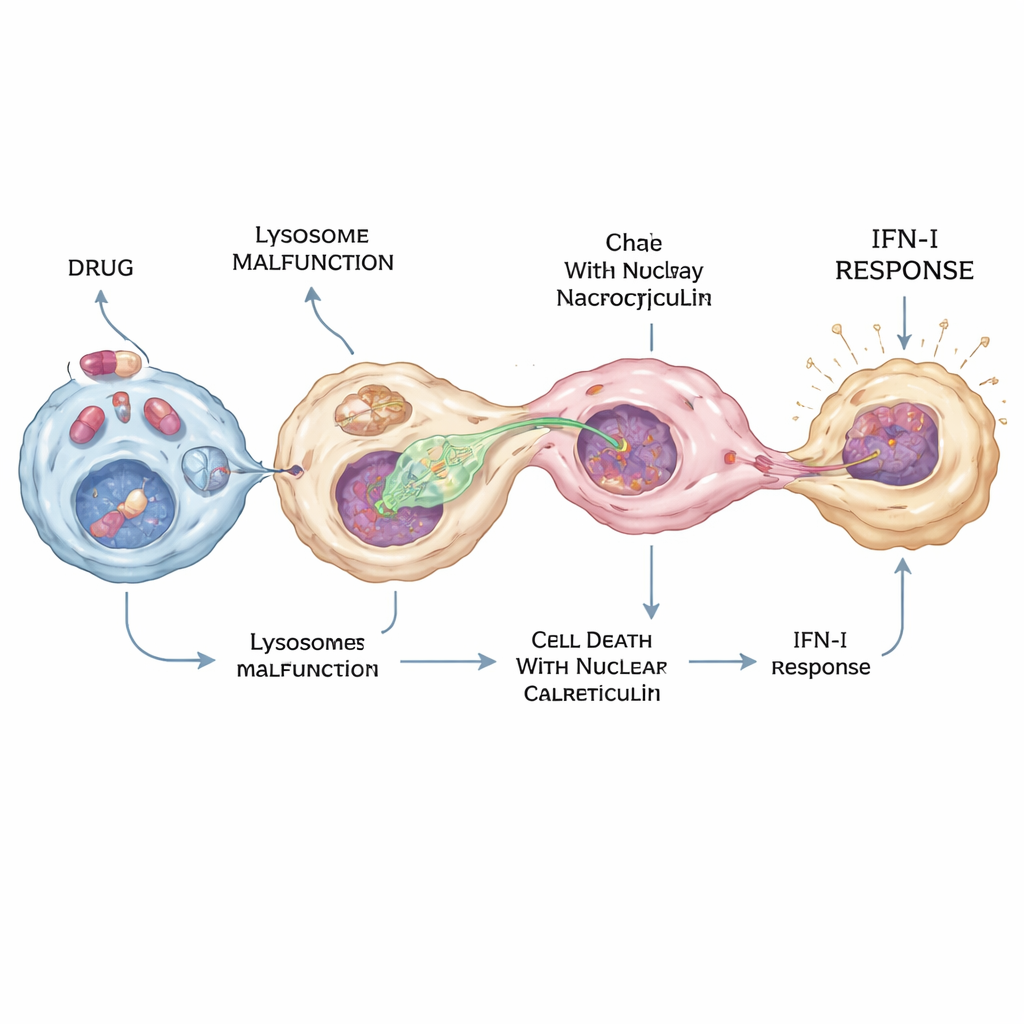
מההגנה מקומית למחלה ולתופעות לוואי
בעבודה על תרביות תאים ועל ריאות עכברים הראו החוקרים שמקרופאגים שטופלו בתרופות יכולים להצית תגובת אינטרפרון תלויה ב‑STING שנשארת ברובה מקומית — למשל בריאה — ולא הופכת לסיסטמית. זה מסביר מדוע תרופות כמו הידרוקסיכולורוקווין עשויות להראות יתרונות אנטי‑ויראליים או אנטי‑גידוליים ברקמות מסוימות, אך גם מדוע הן עלולות לגרום לתופעות לוואי ממוקדות באיברים כמו עין או לב בשימוש לטווח ארוך. אותו תהליך נוקלאוציטוטי עלול לתרום באופן סביר גם למחלות אוטואימוניות או דלקתיות כאשר תאים מתים ולחץ ליזוזומלי מצטלבים, כי הוא מספק נתיב ישיר ל‑DNA עצמי להפעיל את אזעקת ה‑cGAS.
מדוע זה חשוב לטיפולים עתידיים
ללא‑מומחה, המסר המרכזי הוא שתאי חיסון אינם רק בולעים באופן פאסיבי תאים מתים; הם יכולים לחפור באופן פעיל בגרעינים כדי לחלץ DNA ולהשתמש בו כאות לזימון עזרה. מסלול הנוקלאוציטוזה הזה מסביר כיצד ה‑DNA שלנו יכול להפעיל בצורה בטוחה הגנות אנטי‑ויראליות חזקות באופן ממוקד ומקומי, ובו‑בזמן מדגיש כיצד תרופות שמפריעות לליזוזומים או ל‑PPT1 עלולות בטעות להדליק את המתג הזה. על ידי למידת התאמה של נוקלאוציטוזה — בין אם בהדגשה לשיפור תרופות אנטי‑ויראליות וטיפולים בסרטן ובין אם במניעת אותות DNA עצמיים לא רצויים במחלות אוטואימוניות — החוקרים מקווים לרתום את המנגנון שגווע זה לטיפולים בטוחים ומדויקים יותר.
ציטוט: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
מילות מפתח: נוקלאוציטוזה, cGAS-STING, הידרוקסיכולורוקווין, אינטרפרון מסוג I, מקרופאגים