Clear Sky Science · he
הכנה לעומת הפצה: השפעות חיסוניות מובחנות של רדיופרמצבטיקה פולטי־אלפא לעומת פולטי‑בטא כשהיא משולבת בחסימת נקודות בדיקה חיסוניות בעכברים
להפוך את הקרינה לבן ברית חיסוני
רופאי סרטן מנסים יותר ויותר לגייס את המערכת החיסונית להילחם בגידולים, אך רבים מהסרטנים עדיין מתעלמים או מתנגדים לתרופות אלה. המחקר הזה שואל שאלה עכשווית: האם סוגים שונים של קרינה ממוקדת יכולים לשמש לא רק להקטנת גידולים באופן ישיר, אלא גם כאמצעי לאימון המערכת החיסונית לשיפור הביצועים — והאם בחירת התרופה הרדיואקטיבית משנה את אופי אותו אימון?
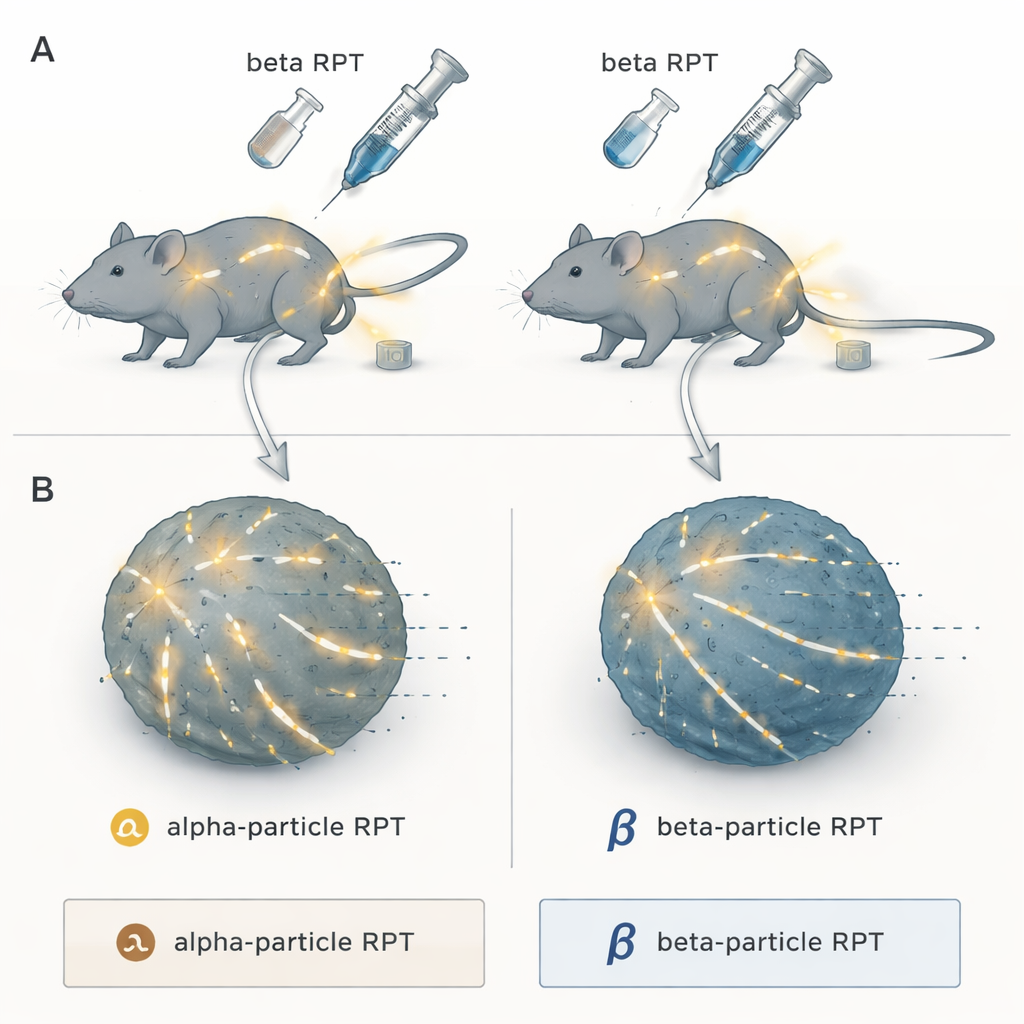
שני טעמים של קרינה מדויקת
החוקרים התמקדו בטיפולי רדיופרמצבטיקה, גישה של "חפש‑והרוס" שבה מטען רדיואקטיבי מקובע למולקולה שנוטה באופן טבעי להגיע לגידולים. לאחר הזרקה הוא מסתובב בגוף ומעביר קרינה לשיירי סרטן היכן שהם מסתתרים — דבר שקשה להשיג באמצעות קרינת חוץ‑גוף רגילה במחלות מפושטות. הצוות השווה שתי קטגוריות עיקריות: פולטות חלקיקי אלפא, שמשחררות תנודות אנרגיה צפופות מאוד על מרחק קצר מאוד, ופולטות חלקיקי בטא, שמשדרות קרינה בעלת צפיפות אנרגטית נמוכה יותר שנעה למרחק גדול יותר ברקמה. כל אלה הוצמדו לאותו תרכובת מחפשת‑גידול, NM600, כך שהבדל היה בסוג הקרינה — לא במכוונות.
שילוב קרינה עם חוסמי נקודות בדיקה חיסוניות
לבדם, תרופות חוסמות‑נקודות כגון אנטי‑PD‑L1 ואנטי‑CTLA4 יכולות להרים את הבלמים מעל תאי החיסון, אך הן עובדות היטב כשגידול כבר גלוי למערכת החיסון. בדגמי עכברים של מלנומה, סרטן הערמונית וסרטן המעי הגס, המדענים נתנו מנה מבוקרת ונמוכה של קרינה מ‑NM600 מבוסס אלפא או בטא, עם או בלי שילוב של חוסמי נקודות בדיקה. הם גם שינו את מועד מתן התרופות החיסוניות — לפני, מיד לאחר או זמן רב אחרי הטיפול הרדיואקטיבי — כדי לבדוק כיצד הטיימינג השפיע על תוצאות כמו גדילת הגידול, הישרדות וזיכרון חיסוני לטווח ארוך.
מתי קרינת בטא זוהרת: חיזוק תגובה קיימת
בדגם של סרטן המעי הגס שהיה "חם חיסונית" וכבר הגיב לאימונותרפיה, התוצאות הטובות ביותר ניכרו עם NM600 פולטת בטא, במיוחד כאשר התרופות החיסוניות הושקו מוקדם או בנקודת זמן בינונית. הגידולים התקצרו יותר, העכברים חיו זמן רב יותר ובעלי חיים שהחלימו דחו לעתים קרובות את אותו סוג סרטן כשחזר הוחדר שוב חודשים לאחר מכן. פרופיל חיסוני מפורט הראה שטיפול מבוסס בטא בשילוב חסימת נקודות בדיקה לא ייצר כל כך תגובה חדשה אלא כּוֹפל תגובה שכבר הייתה קיימת: תאי T קטלניים ספציפיים להתא סרטני התרחבו, הפכו פעילים יותר והפיקו יותר אותות התקפה. בקיצור, פליטות בטא היו מצוינות בהפצת תגובה חיסונית שוטפת וחיזוקה.
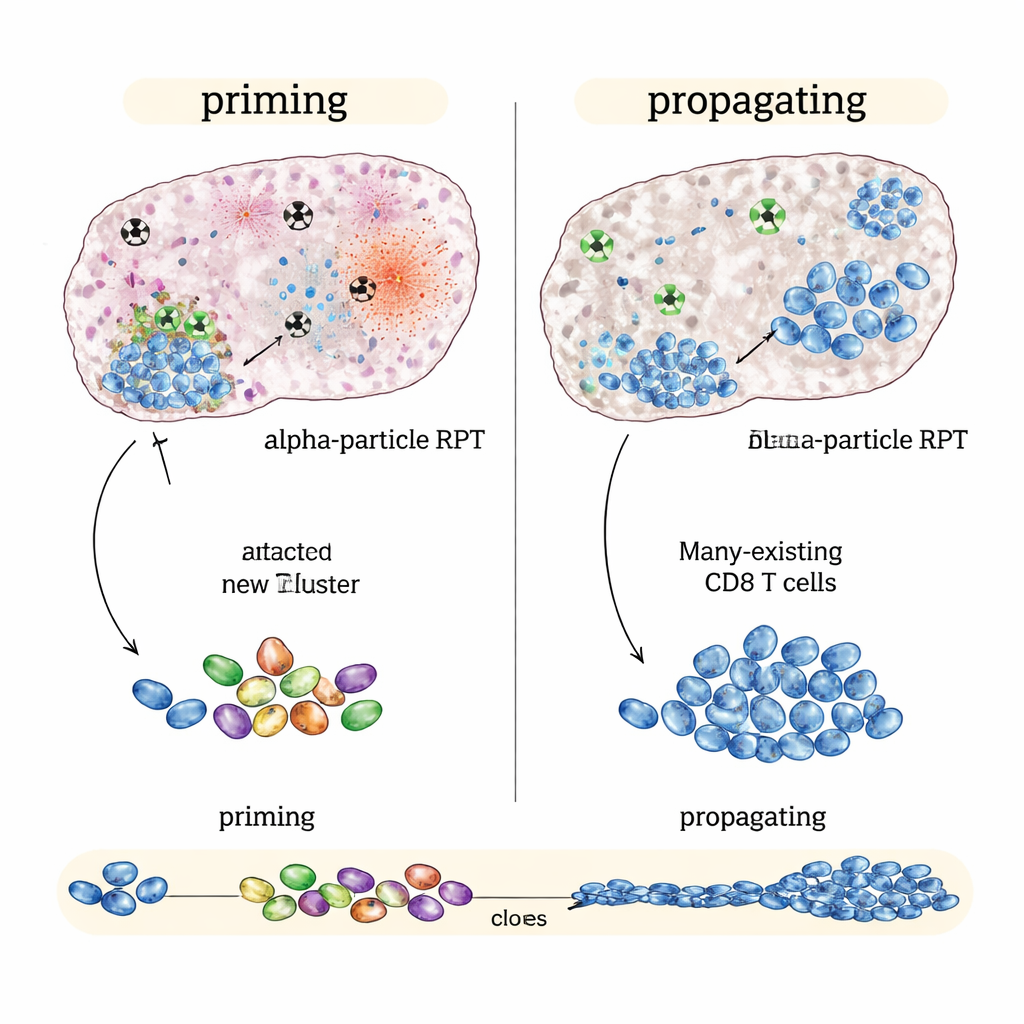
מתי קרינת אלפא זוהרת: הצתת התקפה חיסונית חדשה
בניגוד לכך, בגידולים "קרים חיסונית" כגון דגם של מלנומה וסרטן ערמונית שהגיבו חלש לחוסמי נקודות לבד, הגרסה הפולטת אלפא הופיעה טובה יותר מאשר פולטות בטא באותה מינון ממוצע לגידול. טיפול מבוסס אלפא בשילוב תרופות חיסוניות האט יותר את גדילת הגידול ושיפר עוד יותר את ההישרדות. ניתוחים גנטיים ברמת תא יחיד הציעו הסבר: קרינת אלפא גרמה לנזק מקומי עז שנראה כמיוצר אותות אזעקה חזקים בתוך הגידול תוך פגיעה פחותה במבנים חיסוניים סמוכים. דפוס זה נקשר לתגובות T‑cell רחבות ומגוונות יותר ועדויות ליצירה של תאי T קטלניים חדשים שמכירים את הגידול וקושרים לזיכרון ארוך‑טווח — עדות להכנה חיסונית ולא רק להעצמה.
מדוע סוג וטיימינג של קרינה חשובים
בכל הדגמים, מתן מוקדם או בנקודת זמן בינונית של חוסמי נקודות בדיקה — בערך כאשר האותות המסכנים שנגרמים על‑ידי הקרינה בשיאם — היכו בעקביות את הטיפול המתעכב. העבודה מציעה כלל אצבע פרקטי: בסרטנים שכבר גלויים למערכת החיסון, רדיופרמצבטיקה מבוססת בטא במינון נמוך עשויה להתאים במיוחד כחבר לתרופות נקודות בדיקה כי היא מפיצה ומחזקת חיסוניות קיימת. בסרטנים עמידים יותר לחיסון, פולטות אלפא בעלות השפעה גבוהה עשויות להתאים יותר להכנה של תגובות T‑cell חדשות ולהפיכת גידול "קר" ל"חם". עבור מטופלים, המשמעות היא שלא כל התרופות הרדיואקטיביות ניתנות להחלפה; התאמת האיזוטופ ולוח הזמנים לאישיות החיסונית של הגידול יכולה להפוך קומבינציית רדיו‑אימונו‑תרפיה ליעילה ועמידה יותר.
ציטוט: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
מילות מפתח: טיפולי רדיופרמצבטיקה, אלפא לעומת בטא קרינה, חוסמי נקודות בדיקה חיסוניות, אימונותרפיה של סרטן, מיקרו‑סביבת הגידול