Clear Sky Science · he
המפה התפקודית של ריצוף חלופי בהחלטת ייחוס תאי דם
איך עריכות זעירות בגנים מעצבות את הדם שלנו
כל שנייה הגוף שלך מייצר מיליוני תאי דם חדשים. מאחורי הפלא השקט הזה פועל מנגנון מולקולרי של עריכה שיכול לחתוך ולהדביק קטעים של מסרי גנטי בדרכים שונות, וליצור גרסאות מעט שונות של אותו חלבון. המחקר הזה חוקר כיצד תהליך העריכה הזה, הנקרא ריצוף חלופי, מסייע להטות תאים אבות בלתי בוגרים לכיוון הפיכה לתאי דם אדומים, תאי דם לבנים או סוגי תאים אחרים – ומה קורה כאשר חתיכה בודדת שנערכה חסרה.
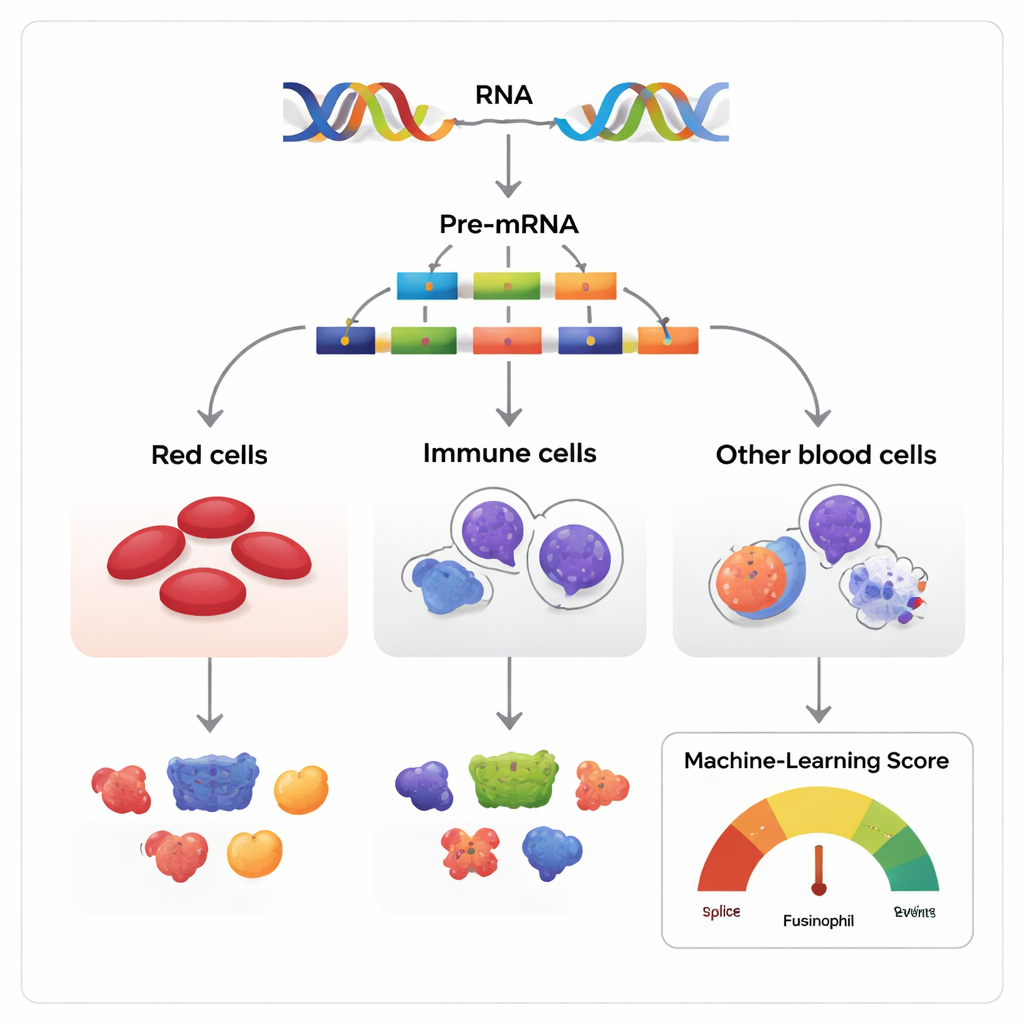
גרסאות רבות מאותו תסריט גנטי
לעתים גנים מתוארים כתכניות, אך במציאות הם יותר כמו תסריטים שניתן לסדר מחדש. בעת קריאה של גן, העתק ה-RNA ההתחלתי מכיל מקטעים שנקראים אקסונים שניתן לשמור או לדלג עליהם לפני שהמסר הסופי מתורגם לחלבון. המחברים בחנו תהליך זה, הידוע כדילוג אקסון, רקמות יוצרות דם בבני אדם, בעכברים ובכמה עופות חולייתיים אחרים. הם הרכיבו יותר מ-270 מערכי נתוני RNA שעוקבים יחד אחר תאי גזע ותאי־אב של הדם כשהם בוגרים לשלוש משפחות עיקריות: תאים אריתרואידים מייצרי תאי דם אדומים, תאים מיואידים לוחמי זיהום, ותאים לימפואידים מייצרי נוגדנים.
דירוג אילו שינויים בריצוף באמת חשובים
מכיוון שרוב הגנים עם כמה אקסונים ניתנים לריצוף בדרכים רבות, האתגר המרכזי הוא להבחין בין וריאציות חסרות מזיק לאלה שבאמת משפיעות על גורל התא. החוקרים בנו מודל למידת-מכונה, שנקרא ניקוד פונקציונלי של ריצוף חלופי (FAScore), כדי להתמודד עם הבעיה. עבור כל אירוע דילוג אקסון, המודל בוחן 19 פרטים, כגון כמה השימוש באקסון משתנה במהלך התפתחות התא, עד כמה ה-DNA הסובב שמור בין מינים, האם הוא משנה מתחמי חלבון מוכרים, והאם הוא מכיל אתרי מודיפיקציה כימית של החלבון. האלגוריתם, שאומן בגישה חיובי–לא מסומן ובמיין-יער אקראי, מפיק ניקוד בין 0 ל-1 המציין עד כמה סביר שאירוע ריצוף נתון יש לו השפעה פונקציונלית.
איתור מתאמים שימוריים ובעלי ספציפיות לקו התפתחות
בהפעלת FAScore על עשרות אלפי אירועי דילוג אקסון, הצוות סיווג אותם לקבוצות סבירות פונקציונליות, לא פונקציונליות או לא ודאיות. אירועים שחזו שיהיו פונקציונליים נמצאו בתדירות גבוהה יותר באזורים בחלבון החשובים לאינטראקציות, ברצפים שמורים אבולוציונית ובמקטעים שמכילים תגיות כימיות כמו פוספורילציה או SUMOylation. רבים מהאירועים האלה היו פעילים רק בקווים מסוימים של הדם או במהלך יצירת דם עוברית, מה שמרמז שהם פועלים כמפסקים מכוונים היטב בחלונות התפתחותיים מסוימים. המחקר הראה גם כי חלק מהאירועים העתיקים ביותר — אלה משותפים לחולייתיים במשך מאות מיליוני שנים — נוטים במיוחד להיות פונקציונליים, בדומה לאופן שבו גנים ישנים נושאים לעתים תפקידים ביולוגיים מרכזיים.
הוכחה ניסויית: כוונון תוצאות של תאי דם
כדי לבדוק את תחזיות המודל, בחרו המחברים מספר אקסונים בעלי ניקוד גבוה בגנים פעילים בקווים שונים של הדם ומחקו אותם בתאי גזע ותאי־אב של דם בעכבר באמצעות CRISPR. התוצאות התאימו לציפיות המודל: הסרת אקסונים מסוימים בגן KLF6 ובגן SSBP3 פגעה בהיווצרות מושבות מיואידיות בלי לפגוע בייצור תאים אדומים, בעוד שמחיקת אקסונים ב-EPB41L1 וב-TBC1D23 שינתה את היווצרות מושבות אריתרואידיות. במיוחד, דילוג על אקסון 15 של TBC1D23 הפחית את ייצור קדם-תאי דם אדומים בעכברים ובזברדגים, מה שהוביל לפחות תאי דם אדומים בסירקולציה ולרמות המוגלובין נמוכות יותר, תוך שמירה יחסית על תאי דם לבנים.
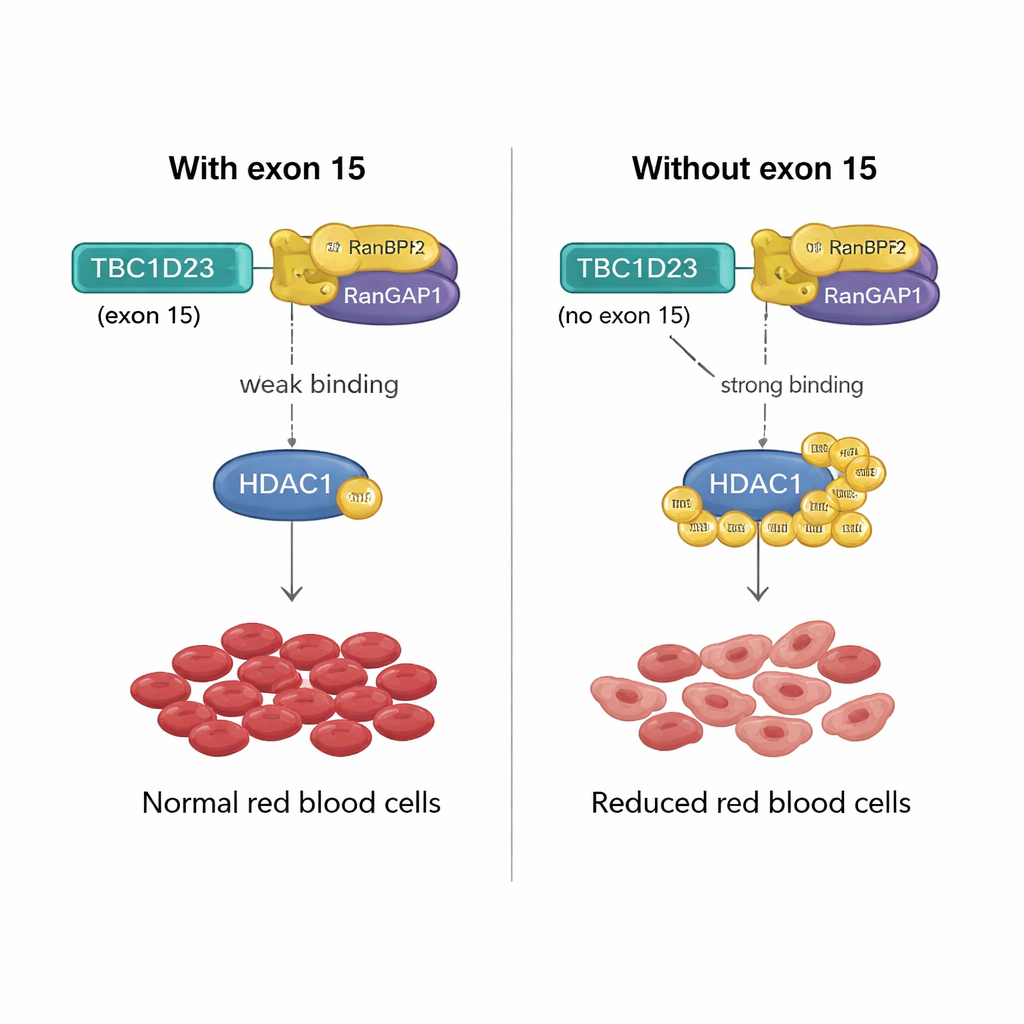
מנופי מולקולרי לייצור תאי דם אדומים
כיצד מקטע של 15 חומצות אמינו שמקודד על ידי אקסון 15 של TBC1D23 יכול לגרום להשפעה כזו? הצוות מצא שהכללת האקסון מחלישה את הקיבוע של TBC1D23 לזוג חלבונים בשם RANBP2/RANGAP1, שמפעלים בשיתוף כדי לקשור תגיות SUMO לחלבונים אחרים. ללא אקסון 15, TBC1D23 נקשר לזוג זה בחוזקה רבה יותר, ומגביר את SUMOylation של אנזים מרכזי, HDAC1. תגיות מחוזקות אלה משנות את הפעילות של גורמי שעתוק רבים — רגולטורים ראשיים של ביטוי גנים — ומערערות את תוכניות הגנים הנחוצות לבשלות תקינה של תאים אדומים. כאשר החוקרים הנדסו גרסה של HDAC1 שאינה יכולה לקבל תגיות SUMO בשתי עמדות קריטיות, היא החזירה את ייצור התאים האדומים בתאים החסרים את אקסון 15 של TBC1D23, ואישרה כי התיוג הכימי הזה הוא הצעד הקריטי.
מדוע זה חשוב לבריאות ולטיפולים עתידיים
ללא היכרות מקצועית, המסר של העבודה הזו הוא שלא כל שינויים גנטיים שווים: לעתים, ההבדל בין דם בריא לאנמיה נעוץ בשאלה האם מקטע זעיר של גן נשמר או מדולג בהודעה הסופית. בשילוב נתוני RNA בקנה מידה גדול עם מערכת ניקוד מתקדמת, המחקר מספק מפת דרכים לזיהוי אילו וריאנטים של ריצוף סביר שישפיעו על בחירת הגורל של תאי הגזע. גישה זו מעמיקה את הבנתנו לגבי אופן היווצרות תאי הדם במצב תקין ובמחלה, ומציעה אסטרטגיה כללית לאיתור אירועי ריצוף חשובים באיברים אחרים, שעשויה להנחות טיפולים גנטיים מדויקים בעתיד.
ציטוט: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
מילות מפתח: ריצוף חלופי, המטופואזה, למידת מכונה, תאי דם אדומים, ויסות גנים