Clear Sky Science · he
אספקת קואצרטים פפטידיים ליצירת מרכזי אינטראקציה יציבים בתאים
בניית “תחנות עבודה” חדשות בתוך תאים
התאים שלנו מלאים בתחנות עבודה זעירות שבהן מתבצעות משימות חשובות — כמו ייצור אנרגיה או תגובות ללחץ. עם הזמן, או במצבים של מחלה, תחנות העבודה הטבעיות הללו עלולות להיחלש. במחקר זה נחקרת דרך להוסיף "מרכזי אינטראקציה" חדשים לתאים חיים באמצעות טיפות פשוטות המיוצרות במעבדה מפפטידים קצרים. המרכזים הסינתטיים האלה יכולים ללכוד חלבונים ספציפיים, לרכז אותם ואף לסייע בהשמדתם, מה שמציע אסטרטגיות חדשות לטיפולים עתידיים והנדסת תאים.
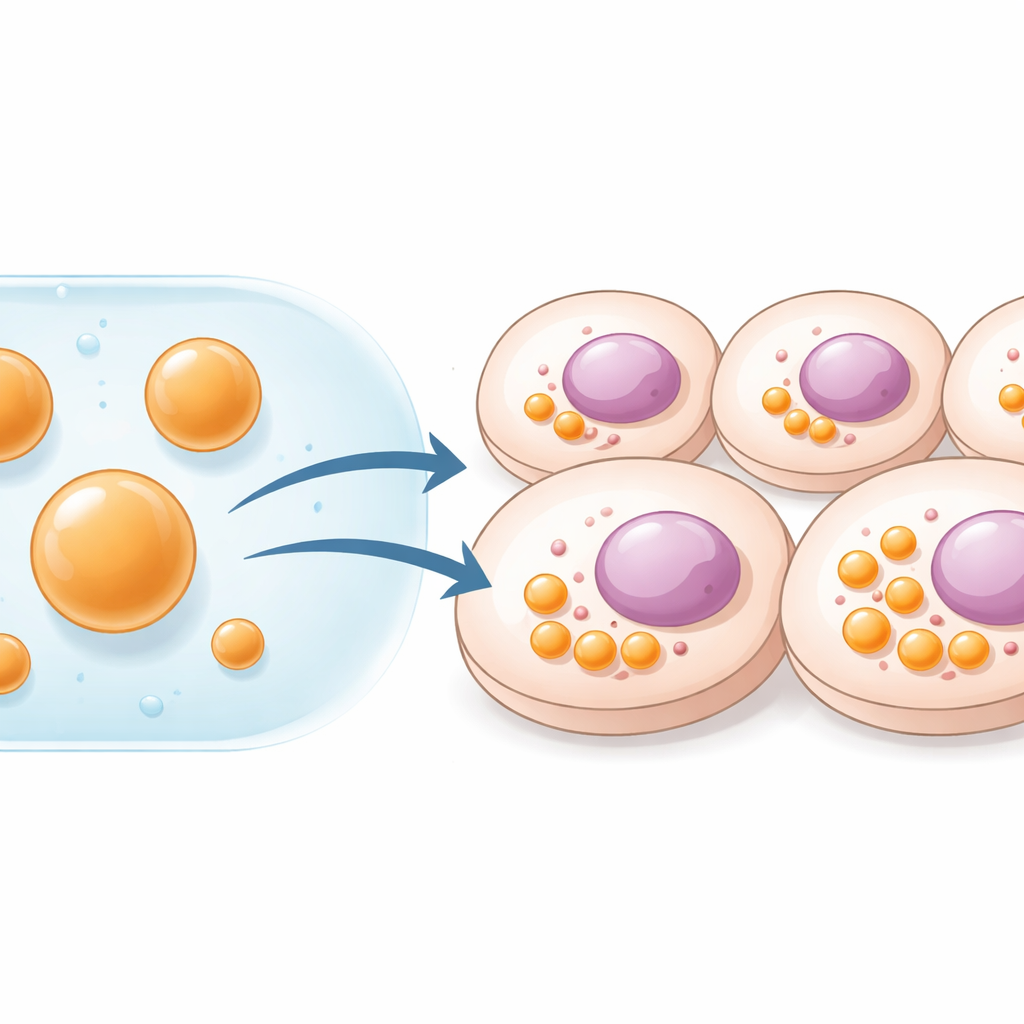
מדוע תאים זקוקים לתחנות עבודה מותאמות
תאים שומרים על סדר על‑ידי הפרדה של משימות שונות לתאים נפרדים. חלקם עטופים ממברנות, כמו מיטוכונדריה; אחרים הם מבנים רכים בדמות טיפות שנוצרות כאשר חלבונים ו‑RNA מסוימים מצטברים יחד. טיפות נוזליות אלו, או עיבויים (condensates), פועלות כמוקדי תגובה שמאיצים או מעכבים מסלולים ביוכימיים ספציפיים. מדענים כבר הנפיקו compartments כאלה על‑ידי אילוץ תאים לייצר חלבוני תבנית מיוחדים באמצעות הכנסת גנים. שיטה זו חזקה, אך דורשת מסירת DNA ומגבילה את כמות החומר שהתא יכול לייצר. מחברי המחקר ביקשו לעקוף את ה‑DNA ולבנות במקום זאת compartments מוכנים מחוץ לתא, ולאחר מכן למסור אותם ישירות כטיפות יציבות בקנה‑מידע מיקרוני.
טיפות פפטידיות היוצרות מרכזים יציבים
הצוות עבד עם פפטידים קצרים וחסרי סדר הידועים כ‑HBpep וגירסה רגישת רדוקס, HBpep‑SA. בתנאים מעט חומציים פפטידים אלה נשארים מומסים, אך כאשר ה‑pH מועבר לרמות קרובות לפיזיולוגיות — או כאשר הטמפרטורה יורדת — הם עוברי פאזות וטופחים לטיפות רכות בדמות ג׳ל בקוטר של כ‑1–5 מיקרומטר. על‑ידי כוונון ריכוז הפפטיד, החוקרים יכלו לשלוט גם בגודל הטיפות וגם במספרן. באמצעות טכניקות פלואורסצנטיות הראו שהמולקולות הפפטידיות בתוך הטיפות נעות לאט, מה שמעיד על מצב ג׳ל שחזק מספיק כדי לשרוד דילול וטיפול. כאשר נוספו לתרביות של תאי סרטן אנושיים, תאי מלנומא של עכבר ותאים חיסוניים ראשוניים אנושיים, הטיפות התקבלו ביעילות והצטברו בציטופלזמה. טיפות גדולות יותר, במיוחד, נשארו שלמות לפחות חמישה ימים, ופעלו למעשה כאברונים סינתטיים ארוכי‑שימושה בתוך תאים חיים.
טענה וכוונת המרכזים
כדי שהמרכזים יהיו שימושיים, הם חייבים לאחוז ולארגן חלבוני מטען. החוקרים שיפרו תחילה את הטענת המטען על‑ידי חיבור תג קצר נגזר HBpep לחלבון מודל, GFP. תג זה עודד את GFP להיקלט בחוזקה לתוך הטיפות ולרכז, באופן מעניין, בסמוך למשטחים שלהן, ויצר ארגון ליבה‑קליפה. לאחר מכן הם הטמיעו בנאבודיז — חלבונים קומפקטיים דמויי‑נוגדן הקושרים בחוזקה מטרות נבחרות — בתוך הטיפות. הבנאבודיז הקושר GFP איפשר למרכזים ללכוד באופן סלקטיבי GFP גם בצינורות מבחנה וגם בתוך תאים. מכיוון שג'ל הפפטיד צפוף יחסית, בתחילה רוב ה‑GFP שנתפס הצטבר על פני שטח הטיפה. אך כאשר המבנה הפנימי הוחרש חלקית, בין אם על‑ידי שינוי תנאי רדוקס או בעזרת יציאה מהאנדוזום, ה‑GFP החל לחדור גם לפנים. בתוך תאים, מוליכים כימיים שמקדמים בריחת אנדוזומים הגדילו במידה ניכרת את החלק של המרכזים שהצליחו לגייס את המטרות שלהם.
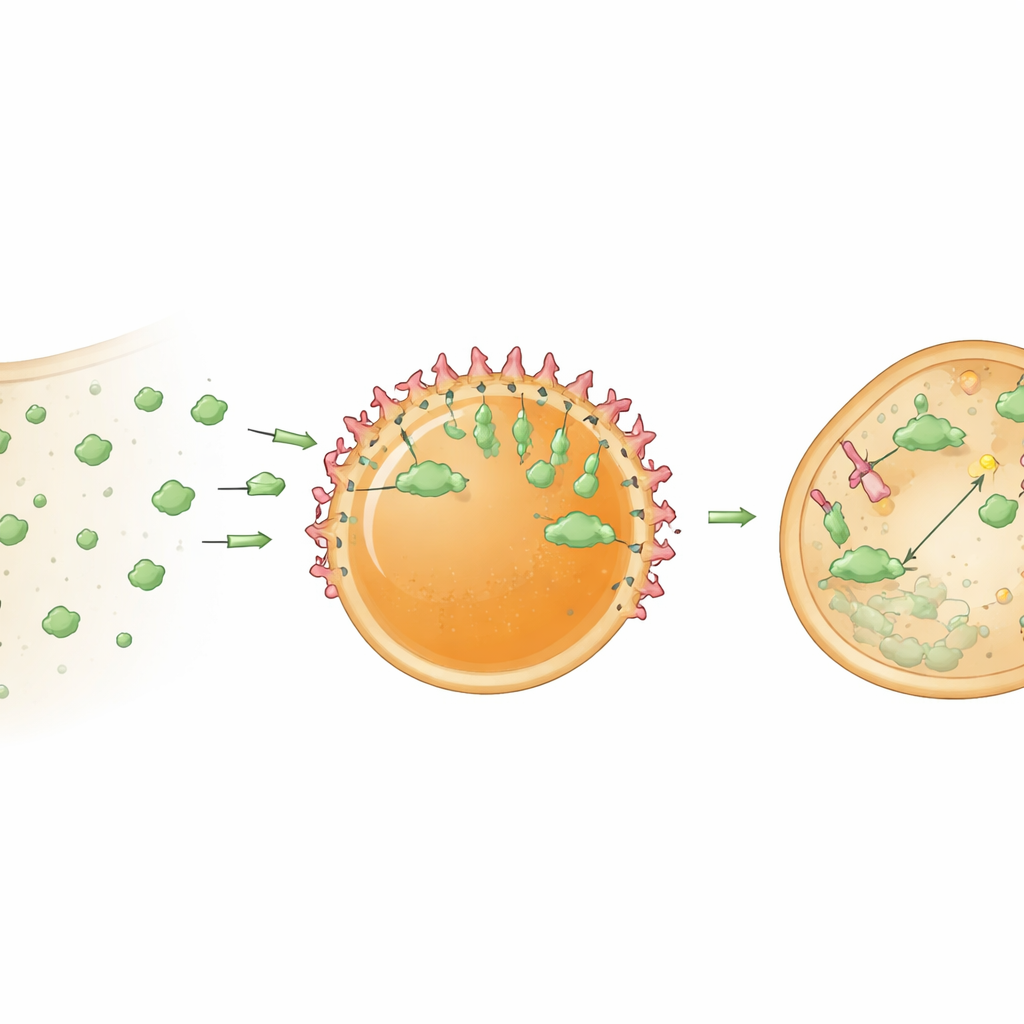
הפיכת המרכזים לטוחני חלבונים
המחברים שדרגו אז את המרכזים מלכידות פסיביות למרכזי עיבוד פעילים. הם טעינו את הטיפות ב‑bioPROTAC — חלבון מיזוג המשלב בנאבודיז קושר מטרה עם חלק ממתאם אנזימטי המסמן חלבונים להשמדה על‑ידי מערכת ההריסה של התא. כאשר טיפות ה"דגרדוזום" הללו נמסרו לתאים שמביעים GFP באופן יציב, רמות GFP בציטוזול ירדו בכ‑78 אחוז בתוך יום אחד. מרכזי ביקורת שכללו רק את הבנאבודיז לכדו את ה‑GFP אך לא הורידו באופן מהותי את רמתו הכוללת, מה שמאשר שהירידה החזקה נבעה מפירוק ממוקד ולא מלכידה בלבד. הממצאים מרמזים שאגירת bioPROTACs בתוך מיקרו‑סביבה מרוכזת הופכת אותם לעוצמתיים בהרבה מאשר כשהם מפוזרים בחופשיות בציטופלזמה.
מה זה עשוי לומר על טיפולים עתידיים
במילים פשוטות, עבודה זו מראה כי מדענים יכולים לייצר טיפות מבוססות פפטידים במבחנה, לארוז אותן בכלי חלבוני מותאם, ואז למסור אותן לתאים חיים שבהם הן מתנהגות כאברונים חדשים וארוכי‑חיים. מרכזים סינתטיים אלה יכולים למשוך באופן סלקטיבי חלבונים טבעיים וכשמצוידים במכונת פירוק, הם יכולים להסיר בח_ACTIVE mål נבחרים מתוך התא. מכיוון שהפלטפורמה הזו נמנעת משינוי גנטי בתא והיא מודולרית במה שהיא יכולה לשאת, היא פותחת נתיב לעבר טיפולים שישקמו או ישנו התנהגות תאית — כגון ניקוי חלבונים מזיקים או חיבור מחדש של איתות לקוי — על‑ידי התקנה פשוטה של "תחנות עבודה" תכנותיות חדשות בתוך תאים שלנו.
ציטוט: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
מילות מפתח: אברונים סינתטיים, קואצרטים פפטידיים, אספקה תוך‑תאית, פירוק חלבונים, הנדסת תאים