Clear Sky Science · he
NatA משתתפת במכלולים רב-גורמיים ביציאת המנהרה של הפוליפפטיד בריבוזום
איך תאים מכוונים בדיוק חלבונים חדשים ברגע שנולדים
כל שנייה, התאים שלך מייצרים אלפי חלבונים חדשים על מכונות זעירות שנקראות ריבוזומים. כאשר כל שרשרת חלבון מתגלה החוצה, יש לגזור אותה, לתייג אותה ולתקפל אותה כראוי, אחרת היא עלולה להתנהג בצורה שגויה ולתרום למחלה. המחקר הזה בוחן אחד ממערכות התיוג המרכזיות, השינוי שנקרא אצטילציה N-טרמינלית, ומראה כיצד קומפלקס אנזימתי מרכזי, NatA, פועל יחד עם מספר שותפים ממש במקום שבו חלבונים חדשים יוצאים מהריבוזום. הבנת הכוריאוגרפיה הזו מסבירה כיצד התאים שומרים על פעילות מפעלי החלבון שלהם בצורה חלקה.
התג הכימי הקטן שחשוב
רוב החלבונים מתחילים את חייהם עם אותו אבני בניין ראשונה, חומצת האמינו מתיונין. לעתים קרובות, המתיונין ההתחלתי מוסר ומוחלף בתג כימי קטן הנקרא קבוצת אצטיל. תג זה, הנוסף לקצה החלבון (הטרמינוס N), יכול להשפיע על משך חייו של החלבון, היעד שלו בתא ואופן פעולתו. שני סוגי אנזימים עיקריים ממוקמים ביציאת מנהרת הריבוזום כדי לבצע את המרה הראשונית הזו: מתיונין-אמינופפטידאזות (MAPs), שחותכות את המתיונין ההתחלתי, ואצטילטרנספרזות N-טרמינליות (NATs), שמוסיפות את תג האצטיל. בין ה-NATs, NatA הוא העבודה הסיזיפית בתאים אנושיים, עם פוטנציאל לשינוי כמעט 40% מכלל החלבונים. מאחר שרבים מהחלבונים מיוצרים בו זמנית, התא חייב לארגן את האנזימים האלה כך שהגזירה והתיוג יקרו במהירות ובסדר הנכון.
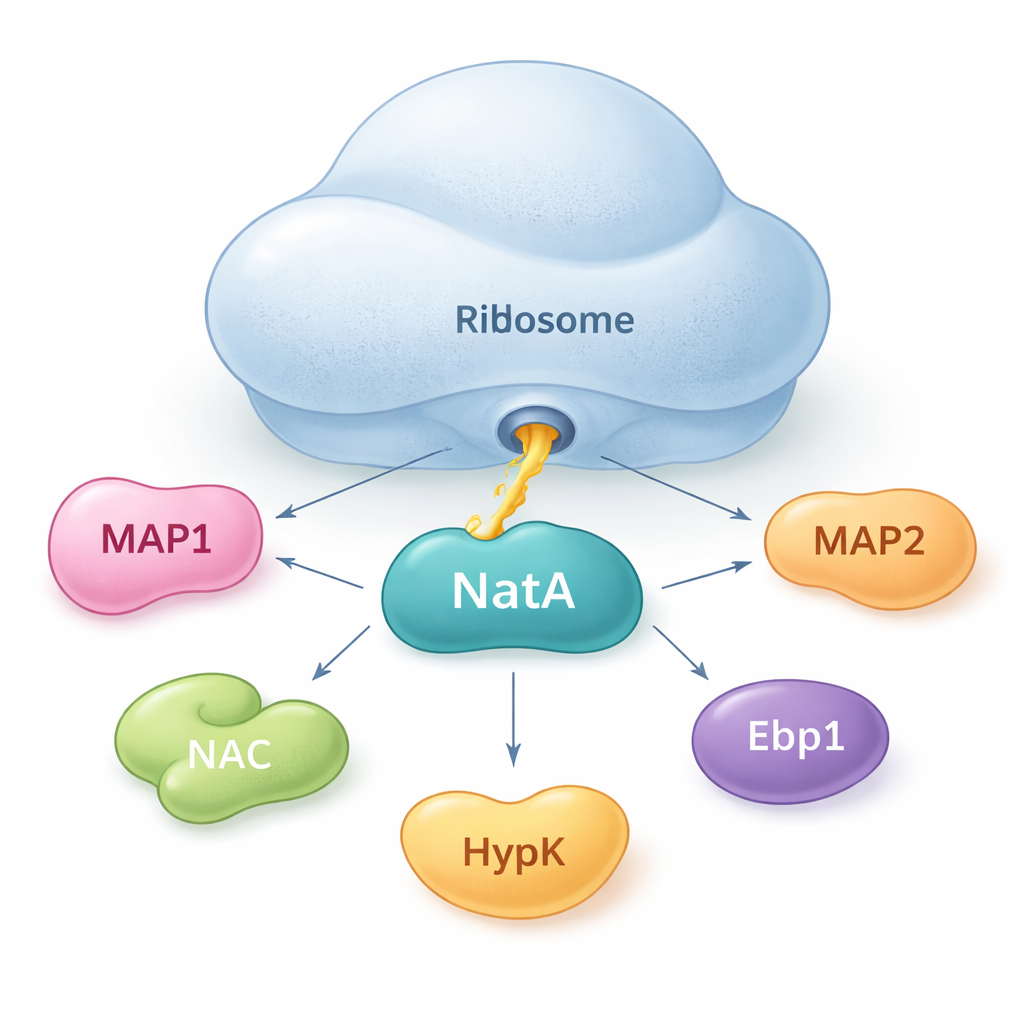
NatA כנקודת מפגש לעוזרי חלבון
המחברים מראים ש-NatA לא פועלת לבד. במקום זאת, הוא מתנהג כצומת שמאחד מספר חלבוני עזר, הן על הריבוזום והן מחוצה לו. באמצעות מדידות קשירה רגישות בתמיסה, הם מצאו ש-NatA יכול ליצור קומפלקסים הדוקים עם MAP1, קומפלקס המקושר לפוליפפטיד הנולד (NAC), החלבון המווסת HypK, ועוד אנזים אחד, Naa50, אפילו ללא נוכחות הריבוזום. NAC יכול לגשר בין NatA ל-MAP1, מה שמאפשר ששני שלבי החיתוך והתיוג יקושרו ב'התקנה' אחת. עם זאת, HypK, שבדרך כלל מרסן את פעילות NatA, יכול לחסום את קשירת NAC. ממצא זה מרמז שהתאים עשויים לעבור בין מצב פעיל יותר, מקושר ל-NAC, לבין מצב מרוסן, קשור ל-HypK, בהתאם לצורכיהם.
מקום עגינה נוסף ממש ביציאת המנהרה
באמצעות מיקרוסקופיה אלקטרונית בקירור (cryo-EM), טכניקה שמדמה מולקולות גדולות ברזולוציה כמעט אטומית, החוקרים גילו ש-NatA יכול להיקשר לריבוזום בשני מצבים מובחנים. אתר אחד, הידוע קודם לכן, נמצא מרחוק במעט מיציאת המנהרה. האתר החדש שנמצא, "פרוקסימלי", מציב את הליבה הקטליטית של NatA קרוב מאוד למקום שבו השרשרת הגדלה מתגלה החוצה, מקצר את המרחק שהשרשרת צריכה לעבור כדי לעבור את השינוי. מעניין ששני המיקומים יכולים להיות מאוכלסים בו-זמנית, כלומר שני קומפלקסי NatA יכולים לשבת על אותו ריבוזום. העתק המרוחק מתפקד כשלד ועוגן, בעוד ההעתק הפרוקסימלי ממוקם בצורה מיטבית לתייג חלבונים חדשים. שני מולקולות ה-NatA גם נוגעות אחת בשנייה, מה שמרמז ש-NatA יכול לתאם את הכפילוּת שלו לצוותי אנזימים רב-מרוכבים.
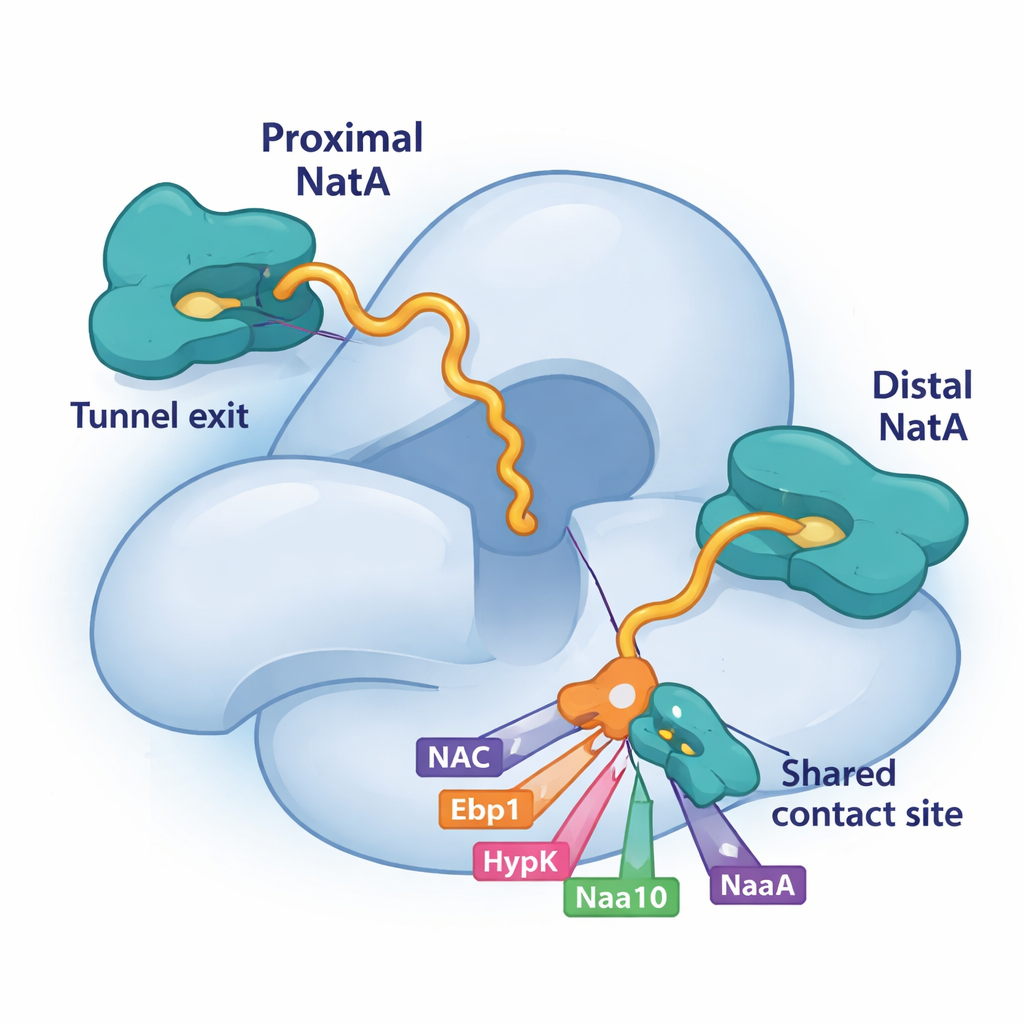
תחרות על משטח עגינה משותף ב-NatA
חתיכת מפתח בפאזל הזה היא חריץ קטן בתת-היחידה הגדולה של NatA, Naa15. המחקר מראה כי ארבעה גורמים מקושרי ריבוזום—NAC, HypK, Ebp1 ואפילו מקטע זנב של תת-היחידה הקטליטית של NatA, Naa10—משתמשים להילכד על ידי הלחמה קצרה של הליקס כדי להיצמד בדיוק לאותה פיסה על Naa15. מאחר שכולם מסתמכים על משטח עגינה משותף זה, הם חייבים להתחרות על הגישה. כאשר HypK תופס את האתר, הוא לא רק משתק את פעילות NatA אלא גם מונע מ-NatA להתמזג עם NAC או ליצור דימרים NatA–NatA. כאשר NAC, ה'פסאודו-אנזים' Ebp1, או Naa10 הפרוקסימלי נקשרים שם במקום, הם יכולים לשנות את מיקום NatA או את הקשרים שלו על הריבוזום. קשירה תחרותית זו מעניקה לתא דרך גמישה לבחור אילו שותפים יתאספו סביב NatA בכל רגע נתון.
פסאודו-אנזים כבורר תנועה
החלבון Ebp1 מרתיע במיוחד. הוא דומה לאחד מהאנזימים שמסירים מתיונין אך חסר פעילות קטליטית; הוא "פסאודו-אנזים." עבודות קודמות הראו ש-Ebp1 יכול לנחות על הריבוזום ליד יציאת המנהרה ולכבוש מקטע RNA ארוך. במחקר זה, המחברים מגלים שכאשר NatA מצטרף לריבוזום, Ebp1 משנה את מיקומו, משחרר את ה-RNA, ובמקום זאת משתמש בהליקס שלו כדי לתפוס את אותו אתר קשירה ב-Naa15 שבו משתמשים NAC ו-HypK. שינוי זה מרמז כי Ebp1 יכול לפעול כמעין מחליף מקומות או מארגן: הוא יכול לעצב את סביבה ה-RNA המקומית ואז למסור את הבקרה לאנזימים פעילים כמו MAPs ו-NatA, מבלי לבצע תגובות כימיות בעצמו.
מדוע שליטה מולקולרית זו חשובה
לא-מומחה, פרטי ההליקסים ואתרי הקשירה עשויים להשמע מופשטים, אך המסר פשוט: התאים מנהלים מערכת איכות-שלבים רב-מוקדית ומחויבת תיאום בדיוק במקום שבו חלבונים נוצרים. NatA יושב במרכז המערכת הזו, מסוגל לגייס או לשחרר שותפים שונים בהתאם לאלו שזוכים בגישה לפאץ' עגינה קריטי ולאיזה אתר ריבוזומלי NatA תופס. הרשת הגמישה הזו מסייעת להבטיח שהגזירה והאצטילציה יתקיימו בסדר ובזמן הנכון לאלפי חלבונים שונים. מאחר שמטענים בשינויי הקצה N-טרמינליים קשורים להפרעות בהתפתחות, לנוירודגנרציה ולסרטן, מיפוי האופן שבו NatA ושותפיו מורכבים נותן לחוקרים מפת דרכים ברורה יותר להבנת האופן שבו עיבוד חלבון מוקדם נשלט—ואיך ניתן לכוון אותו כאשר הוא משתבש.
ציטוט: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
מילות מפתח: בקרת איכות חלבון, אצטילציה קוטבית N-טרמינלית, יציאת מנהרת הריבוזום, מולקולת NatA, שינוי קו-תרגומי