Clear Sky Science · he
הבסיס המבני וההשלכות הפתולוגיות של קומפלקס הליבה הדימרי OS9-SEL1L-HRD1 של ERAD
צוות הניקיון התאי תחת המיקרוסקופ
בתוך כל אחד מתאי הגוף שלנו פועלת מפעלת פעילות המתורגמת הוראות גנטיות לחלבונים פעילים. כמו בכל מפעל, מתרחשים שיבושים. כאשר חלבונים מתקפלים באופן שגוי, הם עלולים לסתום את המערכת ולתרום למחלות. המחקר הזה מתמקד באחד מהמנגנונים המרכזיים של בקרת האיכות התאית — קומפלקס SEL1L‑HRD1 — ובוחן את המבנה התלת‑ממדי שלו ברזולוציה גבוהה כדי להראות כיצד שינויים גנטיים זעירים עלולים לשבש את המכשיר הזה ולהוביל למחלה בבני אדם.
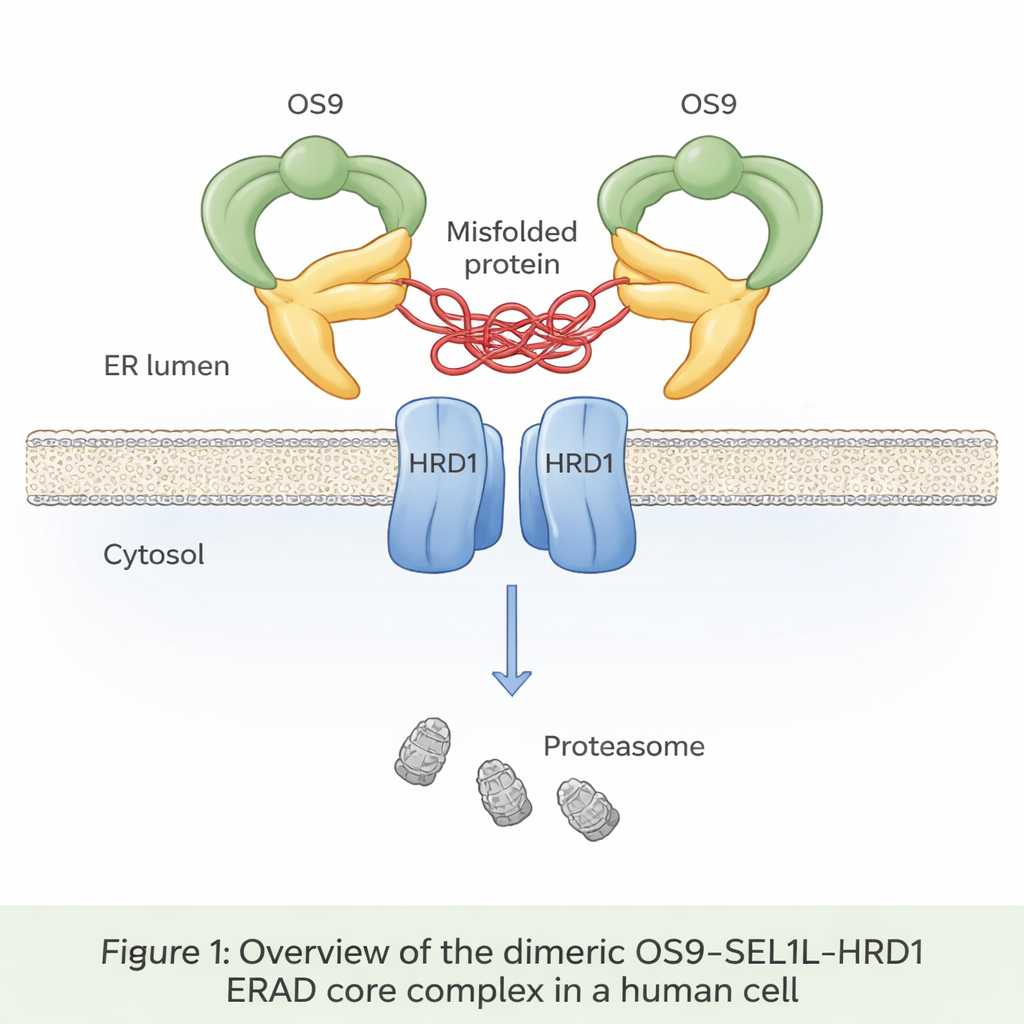
מסוע נסתר בתוך התא
עד שליש מכל החלבונים החדשים המיוצרים נכנסים למחלקה שנקראת הרשתית התוך‑תאית (ER), שם הם מתקפלים ונבדקים. חלבונים מקופלים שגוי מזוהים בדרך כלל, נמשכים חזרה מתוך ה‑ER ונהרסים בתהליך הידוע כ־ER‑associated degradation (ERAD). בליבת אחד הנתיבים העיקריים של ERAD יושבת שלישייה של חלבונים: OS9, SEL1L ו‑HRD1. OS9 משמש כחיישן לחלבונים פגומים שסומנו בסוכרים; SEL1L משמש כתומכת מסגרת; ו‑HRD1 מסמן חלבונים נידונים באמצעות דגלונים קטנים של יוביקוויטין שמסמנים אותם להרס על ידי יחידות המחזור של התא, הפרוטאזומים. עד כה אף אחד לא תיאר ברזולוציה אטומית כיצד שלושת המרכיבים האלה משתלבים בתאים אנושיים.
חשיפת צורת המכונה המרכזית
המחברים השתמשו במיקרוסקופיה אלקטרונית קרטוגרפיה בקריוגניקה (cryo‑EM), טכניקה המציגה מולקולות בהקפאה מהירה ברזולוציה קרובה לאטומית, כדי לדמות את קומפלקס OS9‑SEL1L‑HRD1 שעובד ותוחם מתאים אנושיים. הם גילו שהוא יוצר דימר — למעשה שתי עותקים זהים שמחוברים זה לזה — במקום להישאר כיחידות בודדות. בצד לומן ה‑ER (הפני הפנימיות של ה‑ER), שני מולקולות OS9 ושתי מולקולות SEL1L מרכיבות טבעת בצורת טפרי סרטן עם פתיחה מרכזית שנראית מותאמת לאחיזת חלבונים מקופלים שגוי. בתוך הממברנה עצמה, שתי מולקולות HRD1 מצמדות זו לזו כדי ליצור תעלה משותפת. סידור זה ממקם את ה"טפר" ישירות מעל פתח HRD1, ויוצר מסלול רציף לחלבונים מקופלים שגוי לנוע מלומן ה‑ER, דרך הממברנה, ולקראת הפירוק בציטוזול.
כיצד שינויים זערוריים משבשים מערכת גדולה
מכיוון שמוטציות ב‑SEL1L וב‑HRD1 נמצאו בחולים עם הפרעות קשות בהתפתחות נוירולוגית ומחלות נוספות, הצוות מיפה מספר וריאנטים המקושרים למחלות על גבי המבנה ובדק כיצד הם מתנהגים בתאים. שתי מוטציות ב‑SEL1L, G585D ו‑S658P, יושבות ממש בנקודות המגע עם OS9 ו‑HRD1, בהתאמה. בניסויים בתאים, G585D כמעט ביטלה את יכולת SEL1L להיקשר ל‑OS9, בעוד ש‑S658P החלישה משמעותית את אחיזתה ב‑HRD1; שילוב של שתי המוטציות למעשה שיבש את קומפלקס הליבה, אך השאיר שותפים אחרים ללא פגיעה. כתוצאה מכך התאים התקשו לסמן ולנקות קדם‑הורמון מקופל שגוי, מה שאיפשר לחלבונים פגומים להתממש ולצבור.
מוטציה מחלתית בתעלת הממברנה
המבנה גם מראה שהמקטע החוצה‑ממברנלי 3 של HRD1 הוא ממשק המפתח שבו שתי מולקולות HRD1 נפגשות ליצירת התעלה. החוקרים הנדסו "ידיות" ציסטאין במיקומים ספציפיים והשתמשו בקישור כימי להצמדה כדי לאשר שאזורים אלה באים במגע צמוד בתאים חיים, והוכיחו ש‑HRD1 באמת מדימריזציה בחיים. כאשר הם הפריעו לשריד יחיד שנשמר בחוזקה (T93) בממשק זה, הדימר התמוטט ופעילות ה‑ERAD קרסה, אף על פי שהקומפלקס עדיין הורכב עם OS9 ו‑SEL1L. לאחר מכן הם בחנו וריאנט חולה שהתגלה זה עתה, HRD1 A91D, שנמצא בילד עם בעיות לב וריאות. השינוי הזה, שגם הוא בממשק הדימר, צמצם את הדימריזציה של HRD1 בכ‑כמעט חצי ופגע קשות בהסרת חלבונים מקופלים שגוי, שוב מבלי לערער את הקשירה הכוללת של השותפים.
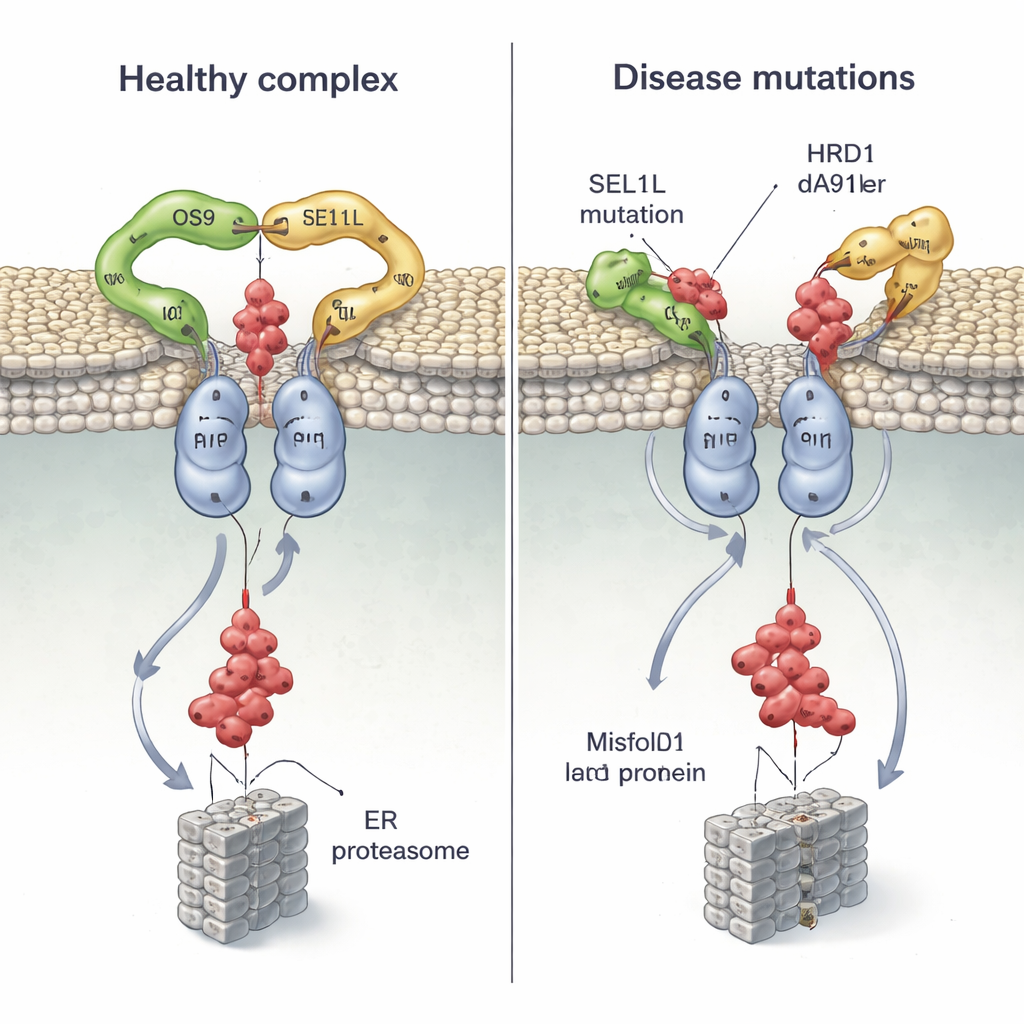
מבט חדש על בקרת איכות חלבונים ומחלות
על ידי שילוב ביולוגיה מבנית עם בדיקות על בסיס תאים, עבודה זו מראה כי קומפלקס OS9‑SEL1L‑HRD1 פועל כמכונה צמודה ודימרית: לוכד בצורת טפר המקושר לתעלה משותפת שמובילה חלבונים פגומים החוצה מה‑ER. מוטציות שמרשלות את אחיזת הטפר או שמייצבות בצורה לקויה את זוג‑HRD1 אינן רק משפרות או מורידות יעילות — הן יכולות למעשה לשתק את המערכת, לאפשר הצטברות של חלבונים פגומים ולתרום למחלות אנושיות. עבור הקוראים שאינם מומחים, המסר המרכזי הוא שלהחלפה של אות אחת ב‑DNA שלנו יכולה להיות השפעה מעוותת על צורתן של מכונות תאיות חיוניות, עם השלכות נרחבות על התפתחות המוח, חיסון ותפקוד האיברים.
ציטוט: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
מילות מפתח: בקרת איכות של חלבונים, רשתית תוך‑תאית (ER), ERAD, קומפלקס SEL1L-HRD1, קיפול חלבונים שגוי