Clear Sky Science · he
מיפוי מחיקות אקסונים בתא יחיד חושף אירועי ספלייסינג שעוצבים את ביטוי הגן ואת דינמיקת מצבי התא
איך עריכות זעירות ב‑RNA יכולות לשנות את התנהגות התא
התאים שלנו קוראים ומחברים בקביעות הוראות RNA כדי להחליט אילו חלבונים לייצר וכיצד להגיב ללחץ, לגדול או להתחלק. מחקר זה מראה ששינוי חתיכות מאוד קטנות של ההודעות האלו — מקטעים בודדים הנקראים אקסונים — יכול לעצב מחדש בעוצמה את פעילות הגנים ואפילו להזיז את האופן שבו תאים מתקדמים במחזור התא. העבודה מציגה כלי חזק שמאפשר למדענים לסרוק בו‑זמנית רבות מהבחירות הקטנות הללו ברמת התא היחיד, ופותח דרכים חדשות להבין מחלות ולגלות מטרות תרופתיות.
גיזור מילים נבחרות מתוך התסריט הגנטי
גנים כתובים כשרשראות ארוכות של DNA, אך התאים לא קוראים אותם ישר. במקום זאת, הם חותכים ומדביקים ביחד בלוקים קטנים יותר, שנקראים אקסונים, כדי להרכיב הודעת RNA. על‑ידי בחירה אילו אקסונים לשמר, תאים יכולים לייצר גרסאות חלבון שונות מאותו גן — בדומה לעריכת גרסאות שונות של סרט מחומר גלם משותף. מחלות רבות, כולל סרטן ואוטיזם, מקושרות לשיבושים בתהליך הזה, אך עבור רוב בחירות האקסון עדיין לא ברור מה תפקודן בפועל. המחברים שאפו לשנות זאת על‑ידי בניית מערכת בהיקף רחב שמסוגלת להסיר אקסונים ספציפיים מרבים מהגנים ולצפות, באלפי תאים בודדים בו‑זמנית, כיצד עריכות אלה משפיעות על הרשת הפנימית של התא.
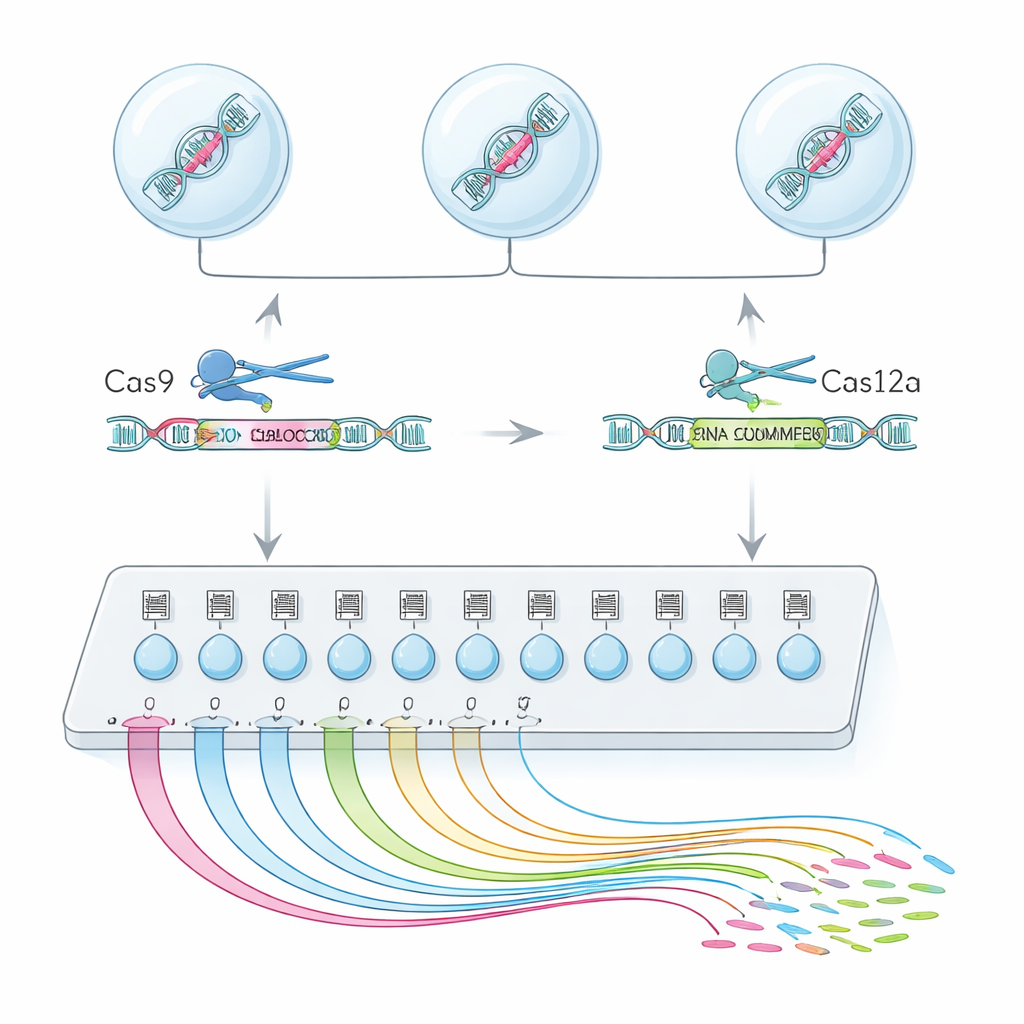
"מנוע חיפוש" בתא יחיד לפונקציית אקסונים
כדי להשיג זאת, הצוות שילב שני אנזימי עריכת גנום, Cas9 ו‑Cas12a, לפלטפורמה היברידית שנקראת CHyMErA. כל אנזים מונחה ל‑DNA על‑ידי "כתובות" RNA קצרות. על‑ידי כיוון שתי האנזימים לחתוך ממש לפני ואחרי אקסון נבחר, ניתן למחוק בצורה מדויקת את המקטע הזה תוך שמירה על שאר הגן. השיטה החדשה, scCHyMErA‑Seq, מקשרת את החיתוך המדויק הזה לטכנולוגיית ריצוף RNA בתא יחיד. ה‑RNA של כל תא נלכד בטיפה יחד עם ברקוד ועם ה‑guide RNAs שמציינים איזה אקסון הוסר. הריצוף חושף אז, בעשרות אלפי תאים, הן את העריכה שכל תא קיבל והן את דפוס ביטוי הגנים המפורט שהוא הפעיל או כבוה.
הנדסת הכלי כדי לראות את שתי להבי המספריים
אתגר מפתח היה גילוי אמין של ה‑guide של Cas12a לצד זה של Cas9 באותו ניסוי תא‑יחיד. העיצובים הראשוניים נכשלו ללכוד את ה‑guide של Cas12a או פגעו ביעילות העריכה. החוקרים פתרו זאת על‑ידי עיצוב מחדש זהיר של רצף המ_HANDLE של Cas12a כדי להסיר מקטעים שגורמים לעצירה מוקדמת של השעתוק, ובהוספת אלמנט RNA קטן שמייצב ושלב הגברה ממוקד. התאמות אלה שיפרו את היכולת לראות את שתי ה‑guides בכ־90% מהתאים, תוך שמירה על מחיקת אקסונים חזקה. בעדכון האופטימלי הזה, המחברים סרקו 224 אקסונים חלופיים ב‑161 גנים בתאים אנושיים, תוך פרופילינג של יותר מ‑200,000 תאי‑יחיד איכותיים.
חשיפת אקסונים ששולטים בתכניות גנים ובמחזורי התא
כשצוות המחקר השווה את פעילות הגנים בתאים שעברו עריכה לאלו שבקרה, כמעט חצי מהאקסונים שנבדקו גרמו לשינויים משמעותיים במאות גנים אחרים. אקסונים של גנים המעורבים בעיבוד RNA והשעתוק נטו להצטבר יחד, ולהניב טביעות אצבע ביטויית דומות ולחשוף מסלולים ביולוגיים משותפים, כמו בניית הריבוזום או דגרדציה של RNA. במקרים מסוימים, מחיקת אקסון יחיד הובילה להשפעה ברורה וניתנת לפרשנות: הסרת אקסון ב‑TAF5 או ב‑LSM11 הפרה עיבוד תקין של RNA היסטון והובילה להצטברות חריגה של הודעות היסטון עם פוליאדנילציה. מאגר הנתונים גם הדגיש עשרות אקסונים שאיבודם שינה את חלוקת התאים בשלבים שונים של מחזור התא, וקשר אירועי ספלייסינג מסוימים ישירות להחלטות על זמני עצירה, שכפול ה‑DNA או הכנה לחלוקה.
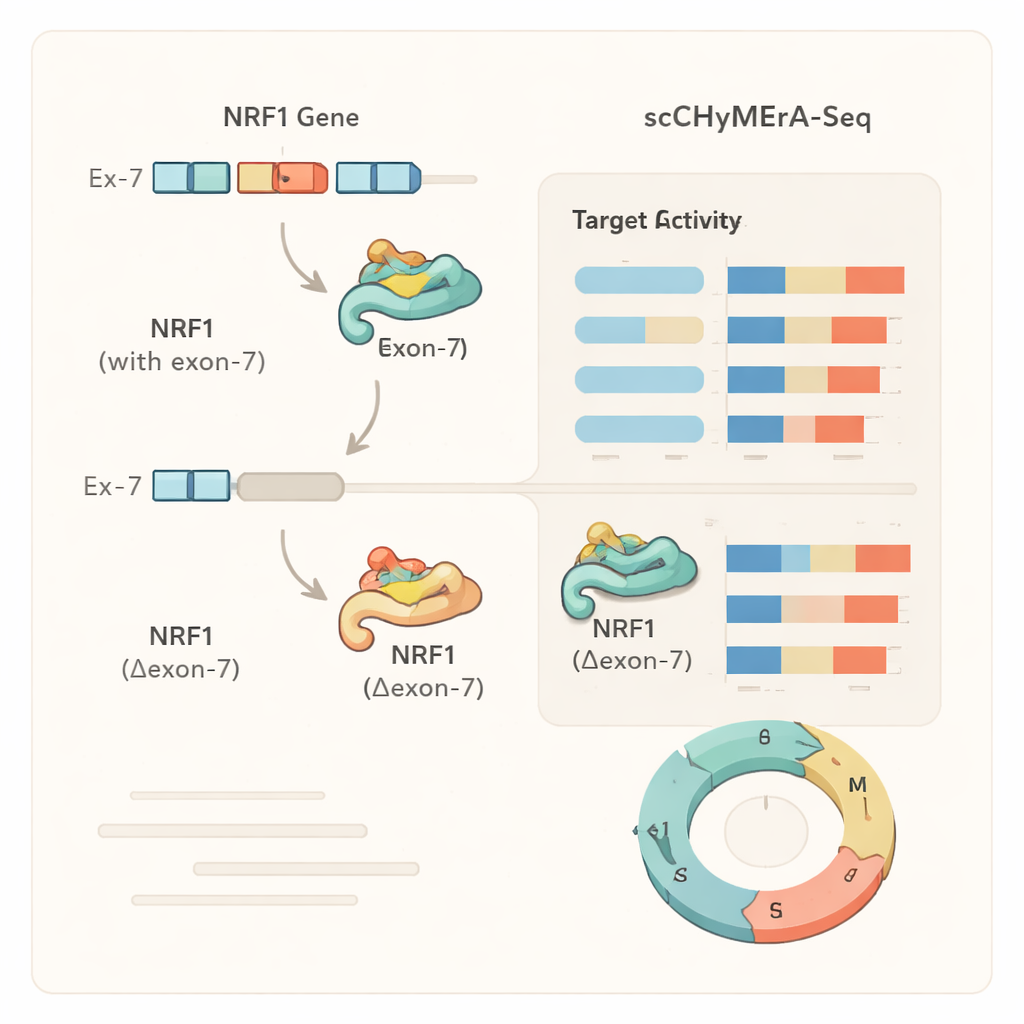
מקרה בוחן: אקסון אחד שמכוונן רגולטור ראשי
דוגמה בולטת הייתה האקסון 7 בגן NRF1, גורם שעתוק השולט ברבים מהגנים המעורבים בהפקת אנרגיה תאית. אקסון זה חופף חלקית לאזור קשירת ה‑DNA של NRF1. כאשר האקסון 7 נמחץ, מאות גנים הנמצאים תחת פיקוח NRF1 שינו את פעילותם, וניסויים מפורטים הראו שהחלבון המקוצר של NRF1 הראה יכולת קשר נמוכה בהרבה לפרומוטורים היעדיים שלו בגנום. המחברים גם זיהו רגולטור ספציפי של ספלייסינג, SRSF3, שמעודד הכללת אקסון זה, וחושף שרשרת מרכיבים מרגולציה של ספלייסינג, דרך בחירת אקסון ב‑NRF1, לשינויים נרחבים בתכניות הגנטיות והמטבוליזם של התא. ניתוחים דומים הראו שעבור חלק מהגנים, מחיקת אקסון חקה השתקה מלאה של הגן, בעוד שעבור אחרים היא יצרה שינוי עדין ותלוי‑מצב, מה שמרמז שאקסונים חלופיים יכולים למודולציה עדינה של התנהגות החלבון במקום פשוט לכבות או להפעיל אותו.
למה זה חשוב לבריאות ולטיפולים עתידיים
לא‑מומחה, המסר המרכזי הוא שהתאים מסתמכים על הכללה או דילוג על מקטעי RNA קצרים מאוד כדי לכוונן את אופן פעולת הגנים, וכי התאמות עדינות אלה יכולות לשנות תכונות מרכזיות כגון אופן חלוקת התאים או תגובה ללחץ. פלטפורמת scCHyMErA‑Seq פועלת כמו בדיקה במעבדה בקצב גבוה לבחירות הספלייסינג הללו, ומצביעה אילו אקסונים בעלי השפעה פונקציונלית אמיתית וכיצד הם מעצבים מצבי תא. מכיוון שרבים מסוגי סרטן והפרעות נוירולוגיות מעורבים באקסונים משובשים או בגורמי שעתוק משונים, השיטה הזו עשויה לסייע בפריוריטיזציה של אילו וריאנטים של ספלייס צריך למקד באמצעות תרופות עתידיות או טיפולי RNA, ולספק מפת דרכים להבנת כיצד עריכות קטנות בתסריט הגנטי מתורגמות לשינויים גדולים בהתנהגות התא.
ציטוט: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
מילות מפתח: ספלייסינג חליפי, ריצוף RNA בתא יחיד, סקרינג CRISPR, ויסות גנים, מחזור התא