Clear Sky Science · he
ננוזים המדמה גרנזיים B לשימושים ממוקדים בננוחליות נגד סרטן
להמציא מחדש את רוצחי הגוף נגד סרטן
למערכת החיסון שלנו יש תאים מיומנים שיכולים לאתר ולהרוג תאים סרטניים, אבל ברבים מהגידולים המוצקים הם מתקשים להיכנס, מתעייפים מהר או תוקפים מטרות שגויות. המאמר מתאר מערכת מלאכותית בקנה מידה ננוסקופי שמדמה אחד הנשקים החזקים של המערכת החיסונית ומספקת אותו ישירות לתוך תאי הגידול. העבודה חשובה כי היא מצביעה על טיפולים בסרטן שמתנהגים כמו תאים חיסוניים חיים, אך עשויים מחומרים יציבים ושמישים שניתן לשלוט בהם, במקום מתאים אנושיים פגיעים.
להפוך רצחנית טבעית לתכנית פעולה
תאי T ציטוטוקסיים, סוג של תאי דם לבנים, הורגים תאים מסוכנים באמצעות אנזים הנקרא גרנזים B. כשהם מזהים מטרה, הם יוצרים חורים קטנים בממברנה ומזריקים את הגרנזים B, שמפעיל תכניות התאבדות בתוך התא. אסטרטגיה זו היא הבסיס לטיפולים מודרניים כמו תאי CAR-T, שיכולים לרפא חלק מסוגי סרטן הדם. עם זאת, בגידולים מוצקים תאי CAR-T נכשלו לעתים קרובות מכיוון שאינם יכולים להגיע לכל אזורי הגידול, נהיים מותשים או פוגעים ברקמות בריאות בטעות. החוקרים שאלו האם אפשר לבנות מכשיר לא-חי בקנה מידה ננו שמחזור את הפונקציה המרכזית של גרנזים B — הדלקת מנגנון ההשמדה העצמית של התא — בלי להסתמך על תאי T חיים.
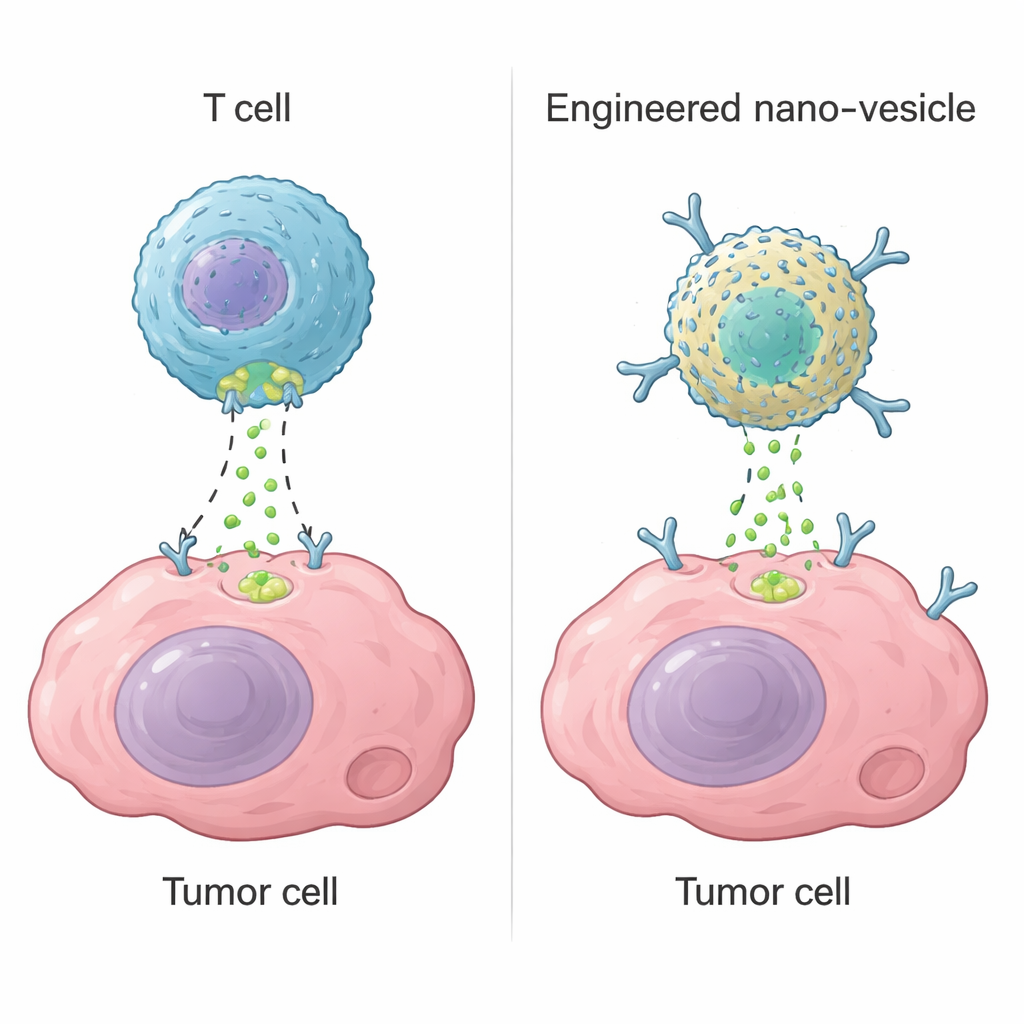
עיצוב אנזים מלאכותי זעיר
הצוות התחיל מפראיטין, חלבון טבעי שיוצר כלובים ננוסקופיים חלולים שקל לייצר בכמויות גדולות. על ידי קשירת יוני פלדיום לפראיטין אנושי הם יצרו "ננוזים" עם התנהגות דמויית אנזים. מחקרים מבניים מדוקדקים הראו ששני אטומי פלדיום מתמקמים בכיס ספציפי על משטח החלבון, מוחזקים במקום על ידי חומצות אמינו המכילות גופרית וחנקן ומולקולות מים. המרכז המתכתי הבינוארטני הזה פועל כאתר חיתוך מלאכותי שמזהה את אותו רצף קצר שמשתמש בו גרנזים B על יעד מרכזי הנקרא קסקפה-3. בניסויים במעבדה הננוזים גזר ביעילות את קסקפה-3 בעמדה הנכונה והפעילו אותו, בעוד שהתעלמו מחלבונים קרובים במשפחתם. האנזים המלאכותי היה מעט פחות יעיל מהגרנזים B הטבעי אך בולט ביציבות רבה יותר בטווח רחב של טמפרטורות וחומציות.
להבריח את הננוזים לתוך תאי הגידול
אנזימים כמו גרנזים B פועלים רק אם הם מגיעים אל פנים תאי הגידול. כדי להשיג זאת, החוקרים ארזו את הננוזים של פלדיום–פראיטין בתוך ננו-ווסיקולות שומניות — בועיות קטנות ורכות העשויות ממולקולות דמויות שומן. לאחר מכן הם ציפו את הווסיקולות בקטעי נוגדנים שמזהים את HER2, חלבון שמופק לעתים בתדירות גבוהה בתאי סרטן השד והשלפוחית. כשהבועיות המחופשות האלה פוגשות תאים עשירים ב-HER2, הן נקשרות בחוזקה ומתמזגות עם ממברנת התא, מה שמאפשר למטען הננוזים להחליק ישירות לציטופלזמה במקום להיתפס ולהיות מעוכלים בממחזורים התאית. מיקרוסקופיה הראתה שהווסיקולות מתמהמהות על פני שטח התא בעוד שהננוזים מפוזרים לתוך הפנים, ומכינים את הקרקע להשמדה מבוקרת מבפנים.
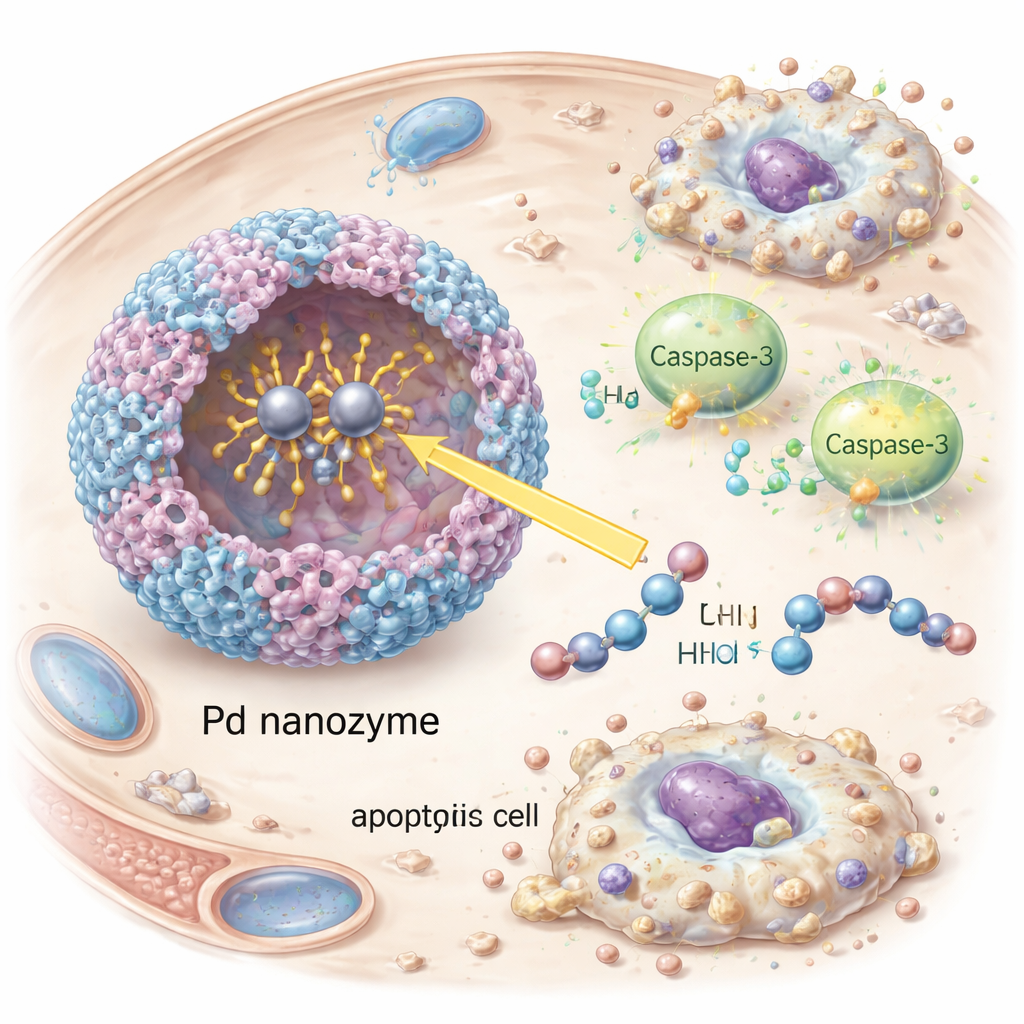
הפעלת התאבדות תאית מדוייקת של תאים סרטניים
לאחר שהננוזים נכנסו לתאי הסרטן, הם הפעילו את קסקפה-3, מבצע מרכזי בתהליך ההרג המתוכנן של התא. החוקרים צפו בהופעת קסקפה-3 פעיל ויעדיו המושפעים בהמשך כמו PARP, וכן בסימנים ברורים של אפופטוזיס — התכווצות והתפרקות תאים — בתאי גידול חיוביים ל-HER2 במנות. השתקת קסקפה-3 בעזרת התערבות RNA צמצמה באופן דרמטי את מוות התאים, ואישרה שההשפעה תלויה במסלול זה ולא בנזק לא ספציפי. בעכברים הנושאים גידולים חיוביים ל-HER2, הווסיקולות המעוטרות בנוגדנים סיבבו זמן רב יותר במחזור הדם, הצטברו ביתר עוצמה בגידולים והאטו את גדילת הגידול ביעילות רבה יותר מאשר ווסיקולות שחסרו או את הנוגדנים המכוונים או את מטען הננוזים. חשוב לציין שבעלי החיים המטופלים לא הראו איבוד משקל בולט, חריגות בדם או נזק לרקמות באיברים מרכזיים, דבר המצביע על פרופיל בטיחות מבטיח בניסויים מוקדמים אלה.
מה זה עשוי לשנות בטיפול בסרטן בעתיד
עבור הקוראים הלא-מומחים, המסר המרכזי הוא שהחוקרים בנו מתקן זעיר, לא-חי, שמתנהג כחלק מפתח ממכונת ההרג של המערכת החיסונית שלנו נגד סרטן. במקום להנדס תאי T חיים, הם הנדסו ננוזים יציב שמפעיל את אותו מתג התאבדות בתוך תאי הגידול וכיסו אותו במעטפת מסירת חכמה הפונה לסוגי סרטן ספציפיים. למרות שנותר עוד הרבה לפני שימוש בבני אדם, גישה זו מציעה פלטפורמה גמישה: מבחינה עקרונית ניתן להחליף את ציפוי הנוגדנים כדי לייעד סמנים סרטניים אחרים, ואת האנזים המלאכותי ניתן לשפר עוד. המחקר מדגים נתיב מבטיח לאימונותרפיה ללא תאים, שבו חומרים בננוסקאלה מתוכננים בקפידה, במקום תאים חיסוניים חיים, משמשים לאיתור ולהשמדת גידולים מוצקים.
ציטוט: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
מילות מפתח: ננו-רפואה לסרטן, אימונותרפיה, גרנזים B, ננוזים, גידולים חיוביים ל-HER2