Clear Sky Science · he
הרכבות מולקולריות מחזוריות להדמיית וגיוס הגולגי
להפוך את מרכז המשלוחים התאי למטרה אסטרטגית
בתוך כל תא בעלי חיים נמצא המכשיר הגולגי, תחנת מיון עמוסה שסוגרת, אורזת ושולחת אלפי חלבונים ושומנים. תאים סרטניים רבים סומכים במידה רבה על הצומת הזה כדי לשנות אותות גדילה ולהפריש גורמים שמעצבים את סביבתם. המאמר מתאר מולקולות מעודנות זעירות שמכוונות לגולגי, מוארות לצורך הדמיה מהירה, וכאשר מהונדסות מחדש — יכולות לחסום באופן בררני את פעילותו ולשבש תאים סרטניים תוך ששמירה על סוגי תאים בריאים מסוימים.
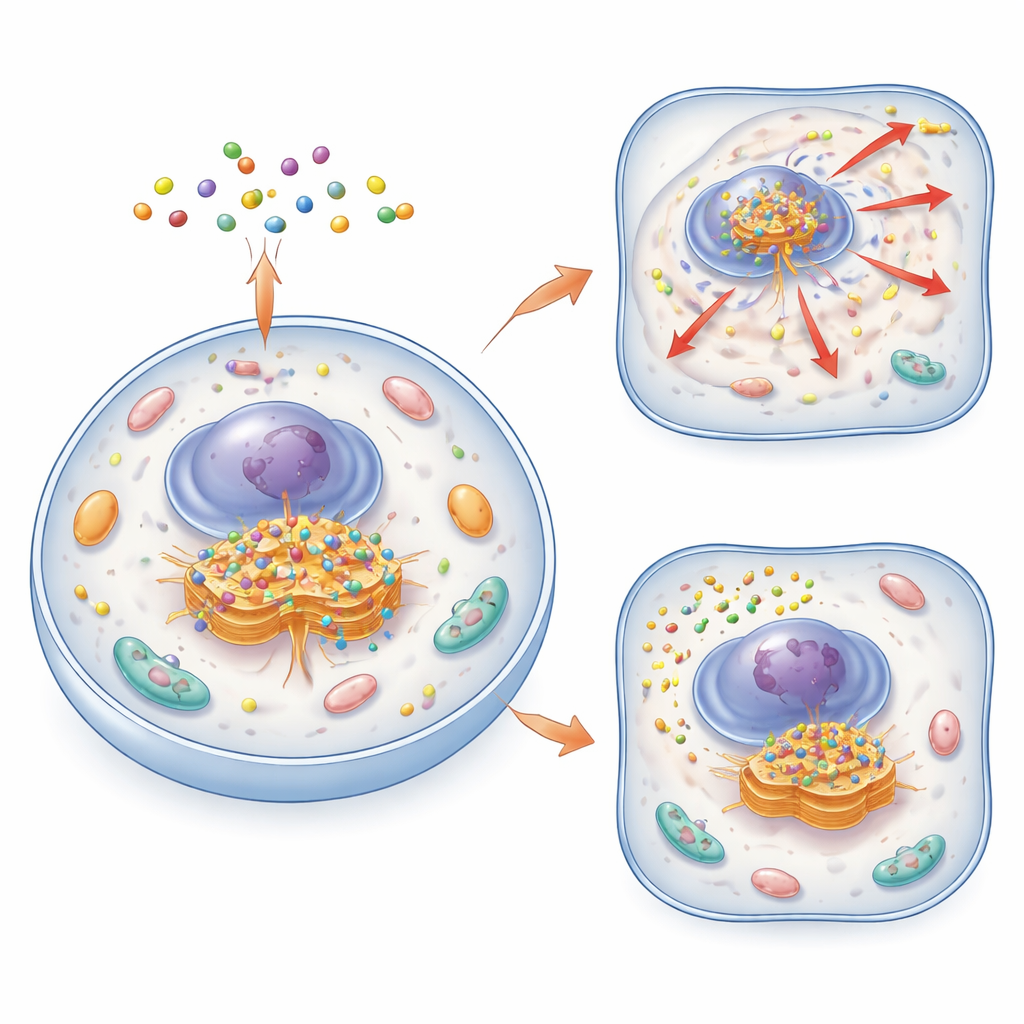
דרך חדשה לאתר ולצפות בגולגי
המחברים ייצרו משפחה של מולקולות קטנות וחכמות שנקראות הרכבות מולקולריות מחזוריות, או CyMA. מולקולות אלו בנויות מפפטידים קצרים שיכולים גם לחלחל דרך ממברנות התאים וגם להצמד זה לזה לצורך יצירת מקבצים זעירים. בגרסת ההדמיה שלהן (CyMA‑i) נושאות הפפטידים צבע זרחני שמאיר בבהירות כשהמולקולות מורכבות. לאחר כניסה לתא, אנזימים גוזרים כובע מגן ממול תקדם ה‑CyMA, חושפים ידית תגובתית. אנזימי תושבות בגולגי מצמידים אז שרשרת שומנית לידית זו, מה שהופך את המולקולות לדביקות יותר ונוטות להרכבה בדיוק בגולגי. מאחר שהתהליך מהיר ומשתמש במכונות התא הטבעיות, החוקרים יכולים לתאר את צורת הגולגי בתאים חיים בתוך דקות ובריכוזי בדיקה נמוכים מאוד.
מעגל חסר תכלית שמצמיד מולקולות לגולגי
CyMA אינן רק סימנים; הן מעוצבות להשתתף ב"מעגל חסר תכלית" בגולגי. קבוצת אנזימים מצמידה שרשראות שומן לפפטיד, בעוד שקבוצה אחרת מסירה אותן. ככל שהתא מוסיף ומסיר את השרשראות שוב ושוב, הפפטידים המועברים מידות ממשיכים להרכיב ולהתפרק במקום. התחלפות מתמדת זו לוכדת ליבת צבירה דמוית‑מוצק על ממברנות הגולגי, אך שומרת על מעבר פריטים בודדים דרך המחזור. התא חייב להמשיך להוציא את בלוקי הבניין של חומצות השומן שלו כדי לשמור על הלולאה הזו, ובפועל מספק לדצוות האנכיות את הדלק לשימורן. במקביל, אנזימים נוספים יכולים איטית לחתוך קשר אסטרי מובחן בתוך CyMA, ולהפוך אותן לשברים הידרופיליים יותר שנסחפים החוצה. מאחר שלתאים בריאים מסוימים, כמו תאי כבד ותאי מערכת חיסון מסוימים, יש שפע אנזימים כאלה שמפרקים אסטרים, הם מסוגלים לפרק CyMA ביתר קלות ולכן מושפעים מהם פחות.
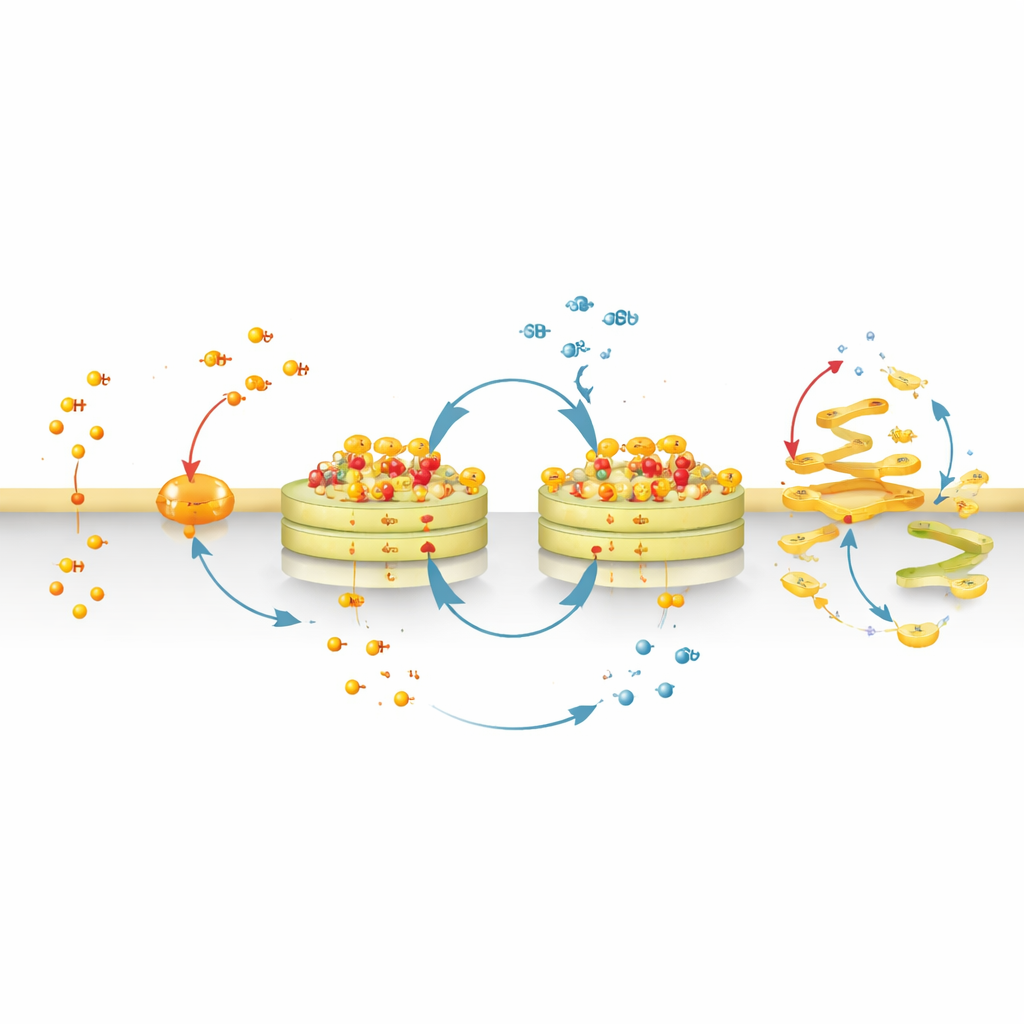
מכלי הדמיה עד מפריע לגולגי
על ידי החלפת הצבע הזרחני בקבוצת כימית שמעדיפה ממברנות באופן חזק יותר, הצוות המיר את CyMA‑i ל‑CyMA‑d, גרסה מפריעה שאינה זורחת אך עדיין עוברת מחזור ומורכבת בגולגי. הרכבות אלו משבשות פיזית את המבנה של הגולגי ואת הזרימה המתמדת של וזיקולות אליו וממנו. חלבונים שבדרך כלל עוברים מהרטיקולום האנדופלסמתי אל הגולגי ומשם אל פני התא נתקעים או נשלחים לנתיבים שגויים. מסלולים נכנסים — מהמשטח התאי חזרה לגולגי או מהגולגי לאורגנלות אחרות — גם הם נחסמים. כתוצאה מכך, קולטנים חשובים ומשכפלי אותות על פני התא אינם מגיעים ליעדם או מצטברים במקומות שגויים בתוך התא.
פירוק אותות ותיקשורת סודית של התא
הגולגי הוא המקום שבו רבים מהחלבונים מקבלים גימורים חיוניים, כגון שרשראות סוכר וזנבות ליפידיים. הרכבות CyMA‑d מצמצמות ליפידציה וגליקוזילציה תקינות של חלבונים רבים, כולל מפעילי סרטן ידועים כמו Ras וקינאזות טירוזין קולטניות מרכזיות. השינויים האלה משבשים מסלולי קידום גדילה כמו AKT ו‑mTOR. במקביל, היציאה הסקרטורית של התא מוחלשת: גורמים חשובים כמו TGF‑β1 ו‑VEGF, שבהם גידולים משתמשים כדי לדכא את החיסון ולעודד כלי דם, אינם משתחררים ביעילות. הלחץ שנגרם על ידי ההתמוטטות הזו מוביל לרשתות רטיקולום אנדופלסמתי מעוותות, מיטוכונדריות משתנות, אוטופאגיה תקועה (מערכת המיחזור של התא) ועלייה בחלבונים פגומים המסומנים באוביקויטין — כל אלה דוחפים תאים סרטניים לעבר מוות.
לחץ סלקטיבי על גידולים והבטחה לטיפול
מאחר ש‑CyMA‑d תלויות בקבוצת אנזימים ומטבוליטים שהרבה תאים סרטניים משתמשים בהם ביתר, הן מסוגלות להרוג מגוון סוגי גידול, כולל מודלים של סרטן שחלת עמידים לתרופות, במינונים נמוכים מאוד. עם זאת, תאים עם רמות גבוהות של אסטרזות ספציפיות מפרקים את CyMA‑d ביתר קלות ונפגעים פחות, מה שמעניק מסלול מובנה לברירות. בתלמיות גידול תלת‑ממדיות, בתרביות ממחקרים של מטופלים ובמודלים עכבריים, CyMA‑d מצמצמות גידולים, מקטינות גרורות ומפחיתות הצטברות נוזלים בבטן. בשילוב עם טיפולים חוסמי‑צ'קפוינט אימונולוגיים הן משפרות עוד יותר שליטה על הגידול והישרדות. במובן זה, העבודה מראה שבניית חומרים דינאמיים בתוך הגולגי — במקום לפגוע בחלבון בודד — יכולה להשבית במקביל מספר תהליכים קריטיים לסרטן.
מה זה אומר עבור טיפולים עתידיים
לעין שאיננה מומחית, הרעיון המרכזי הוא שהמחברים הפכו את הגולגי ממעורב פסיבי למטרה טיפולית פעילה. על‑ידי גיוס אנזימי התא עצמו להרכיב ולמחזר מולקולות זעירות בצומת המרכזי הזה, ניתן או להאיר אותו ללא נזק או להעמיס אותו בהדרגה עד לשיבוש פונקצייתו. פלטפורמה דו‑שימושית זו מציעה סוג חדש של טיפול: במקום לעצב תרופה אחת נגד חלבון אחד, אפשר למהנדס קודמיונים קטנים שהתא ממיר אותם לחומרים אשר מארגנים את עצמם, המסוגלים לשבש רשתות תקשורת והובלה שלמות שעליהן סרטן נשען כדי לגדול ולהתפשט.
ציטוט: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
מילות מפתח: מכשיר הגולגי, הרכבות מולקולריות, הובלת חלבונים, טיפול בסרטן, מיקוד לאורגנלות